Clear Sky Science · fr
Prise de décision alimentaire par un seul neurone via des neurotransmetteurs distincts
Comment une cellule cérébrale peut décider de manger
Chaque fois qu’un animal goûte quelque chose, il doit choisir rapidement entre avaler et recracher. Cet article explore un retournement surprenant de cette décision quotidienne chez la mouche du vinaigre : une seule paire de cellules cérébrales peut indiquer à l’animal « vas-y, mange » ou « stop, c’est mauvais », selon l’intensité de leur activation. Comprendre comment un neurone peut provoquer des comportements opposés éclaire la façon dont les cerveaux simplifient des choix complexes en utilisant des circuits très compacts.
Goûter le bon et le mauvais
Les mouches du vinaigre, comme les humains, distinguent les aliments sucrés riches en énergie des substances amères potentiellement toxiques grâce à des cellules sensorielles du goût situées sur les pièces buccales, les pattes et la gorge. Ces cellules envoient des informations vers une région cérébrale appelée zone sous-œsophagienne, qui coordonne les actions alimentaires. En général, les cellules sensibles au sucré favorisent l’alimentation, tandis que celles sensibles à l’amer déclenchent le rejet. Mais des enregistrements réalisés chez de nombreux animaux ont montré que, plus loin dans la voie du goût, certains neurones répondent à la fois au sucré et à l’amer. Comment de tels signaux mixtes sont transformés en décisions nettes reste un casse-tête de longue date.
Une paire particulière de neurones décisionnels
Les auteurs se sont concentrés sur une minuscule paire de neurones, jusque-là mystérieuse, du cerveau de la mouche qui produit une molécule de signalisation appelée leucokinine. Grâce au traçage génétique, à la microscopie électronique et à l’imagerie d’activité, ils ont montré que ces cellules, nommées SELK, se situent immédiatement en aval des cellules réceptrices du goût sucré et amer. Les SELK collectent l’information gustative provenant de plusieurs parties du corps et sont activées par les deux qualités gustatives, les signaux amers produisant en général une activité plus forte que les sucrés. Cela place les SELK à un carrefour clé où des messages gustatifs opposés convergent et doivent être résolus en un choix comportemental unique.
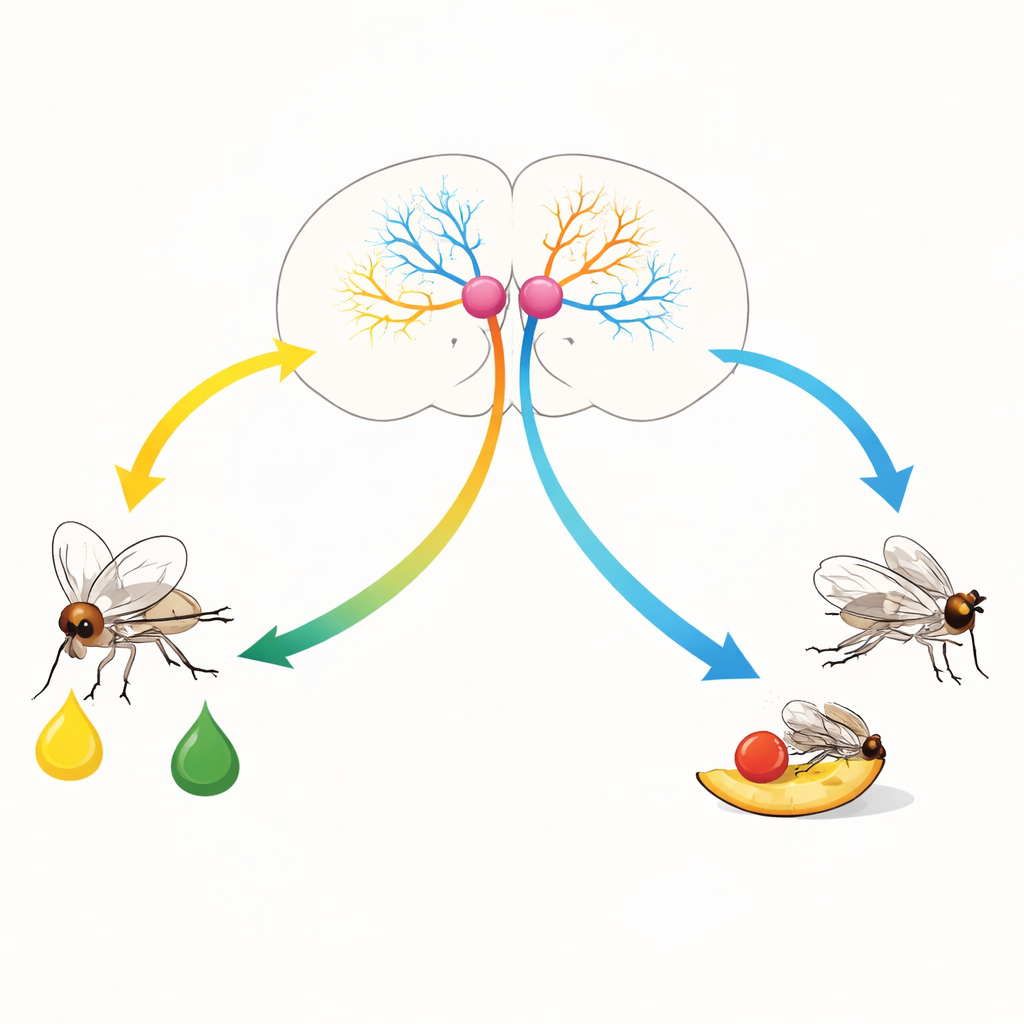
Deux messages chimiques issus d’une même cellule
Fait remarquable, les SELK envoient deux messages chimiques très différents au reste du cerveau. Lorsque les SELK sont fortement activées — par exemple par des goûts amers — leurs réserves de leucokinine sont libérées. Bloquer génétiquement la leucokinine, ou empêcher sa libération par les SELK, fait perdre aux mouches leur évitement habituel des aliments imprégnés d’amer, même lorsque ces aliments sont signalés artificiellement comme désagréables. Inversement, activer les SELK par la lumière suffit à faire éviter aux mouches une solution sucrée autrement attractive, mais seulement si la leucokinine est présente. Ces expériences montrent que l’activité intense des SELK et la libération de leucokinine poussent l’animal vers le rejet alimentaire.
Une aide à l’alimentation fournie par un signal plus rapide
Ces mêmes neurones produisent aussi de l’acétylcholine, un transmetteur chimique à action rapide. L’équipe a constaté que les SELK sont les seules cellules à leucokinine dans le cerveau de la mouche qui utilisent aussi l’acétylcholine. Lorsqu’ils ont bloqué spécifiquement la production d’acétylcholine dans les SELK, les mouches ont pris moins de gorgées de sucre et ont montré une extension moins marquée de la proboscide — la partie buccale en forme de paille qu’elles utilisent pour boire. En revanche, la suppression de la leucokinine n’altérait pas cette promotion de l’alimentation. De faibles niveaux d’activation des SELK semblent libérer principalement de l’acétylcholine à partir de petites vésicules faciles à déclencher, tandis qu’une activité plus élevée ajoute la libération de leucokinine à partir de réserves plus grosses et plus difficiles à vider. En aval, une paire de neurones de projection surnommée « Amulet » reçoit l’entrée cholinergique des SELK et, lorsqu’elle est activée, encourage aussi l’alimentation, reliant les SELK aux circuits moteurs qui commandent la prise de nourriture.
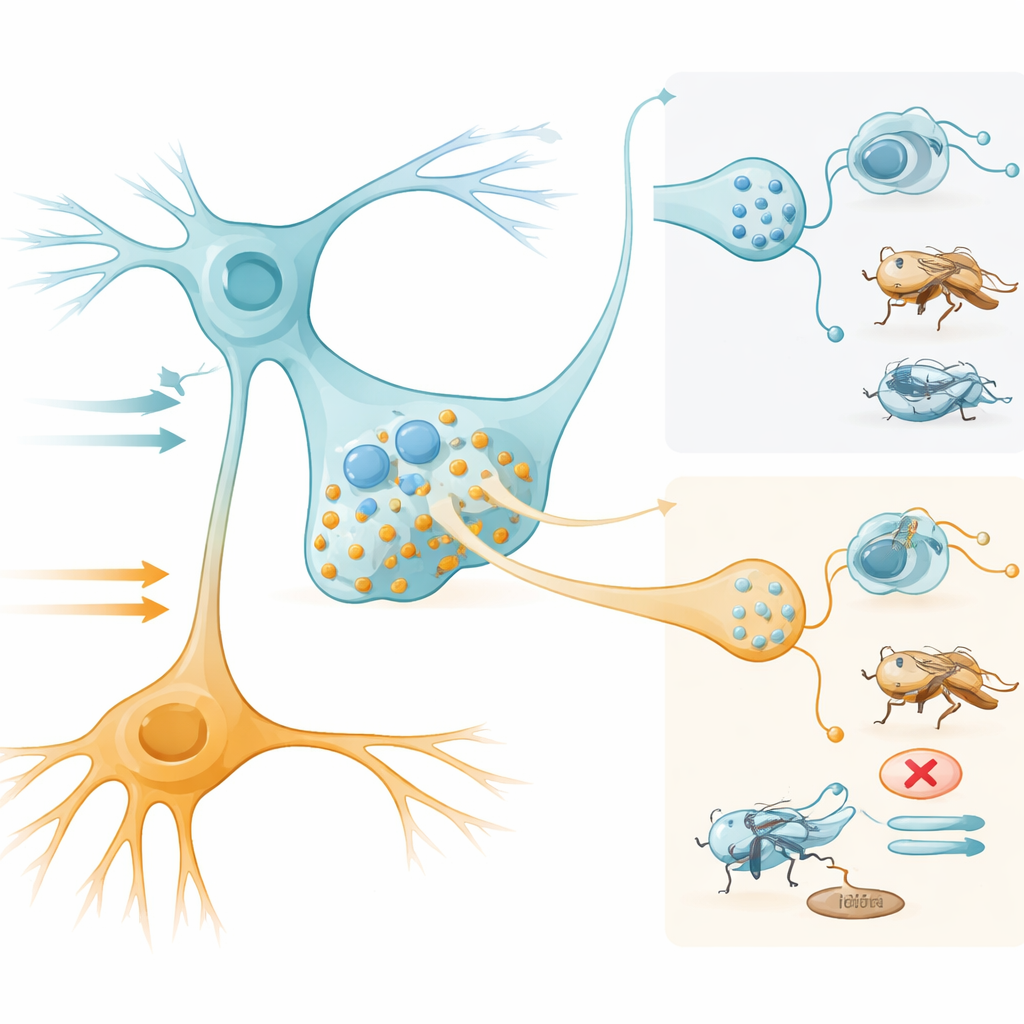
Basculer entre manger et ne pas manger
Pour tester si la seule intensité d’activité pouvait inverser la sortie des SELK, les chercheurs ont utilisé une stimulation lumineuse graduée. Une activation faible des SELK a rendu les mouches préférer l’aliment qui déclenchait les SELK, cohérent avec une promotion de l’alimentation portée par l’acétylcholine et peu ou pas de libération de leucokinine. Une activation plus forte a inversé ce comportement : les mouches évitaient l’aliment associé aux SELK, et des dosages biochimiques ont montré un appauvrissement des granules de leucokinine, indiquant une libération peptidique. Ainsi, la même paire neuronale fonctionne comme un interrupteur sensible au contexte. Une activation douce, comme celle qui peut survenir avec des goûts sucrés chez un animal affamé, aide à ouvrir la porte à l’alimentation, tandis qu’une activation forte, provoquée par l’amer ou une stimulation intense, claque cette porte.
Ce que cela signifie pour la façon dont les cerveaux choisissent
Cette étude révèle qu’une seule paire de neurones peut gouverner des comportements opposés — manger versus éviter — en emballant deux signaux chimiques dans différents types de sites de libération et en les mobilisant selon le niveau d’activité. Ce dispositif permet au cerveau de la mouche de combiner des signaux gustatifs contradictoires et des signaux internes de faim en un résultat simple et décisif sans nécessiter de nombreux circuits séparés. Une logique similaire a été observée récemment chez des cellules cérébrales de mammifères qui utilisent un transmetteur rapide pour des signaux récompensants et un peptide plus lent pour des signaux aversifs. Ensemble, ces résultats suggèrent que des « neurones décisionnels » compacts et bichemicaux peuvent être une stratégie courante utilisée par l’évolution pour rendre l’alimentation — et d’autres choix vitaux — à la fois flexibles et efficaces.
Citation: Savaş, D., Okoro, A.M., Moșneanu, R.A. et al. Feeding decision-making by a single neuron via disparate neurotransmitters. Nat Commun 17, 3596 (2026). https://doi.org/10.1038/s41467-026-69443-8
Mots-clés: comportement alimentaire, neuropeptides, Drosophile, circuits du goût, double neurotransmission