Clear Sky Science · fr
Un nouveau Pr3ZrO8-δ hautement appauvri en oxygène et cubique pour la production thermochimique d’oxygène et d’hydrogène à température intermédiaire
Transformer la chaleur en carburant propre
On appelle souvent l’hydrogène le carburant du futur, mais aujourd’hui la majeure partie est produite à partir de gaz naturel, ce qui rejette d’importantes quantités de dioxyde de carbone. Cette étude explore une voie différente : utiliser la chaleur plutôt que des combustibles fossiles ou de grandes quantités d’électricité pour extraire l’hydrogène et l’oxygène de l’eau. Les chercheurs présentent un nouveau solide capable de stocker et de libérer de l’oxygène de façon répétée à des températures relativement élevées mais modérées, ouvrant la voie à une production d’hydrogène plus propre alimentée par la chaleur solaire concentrée ou la chaleur résiduelle industrielle.
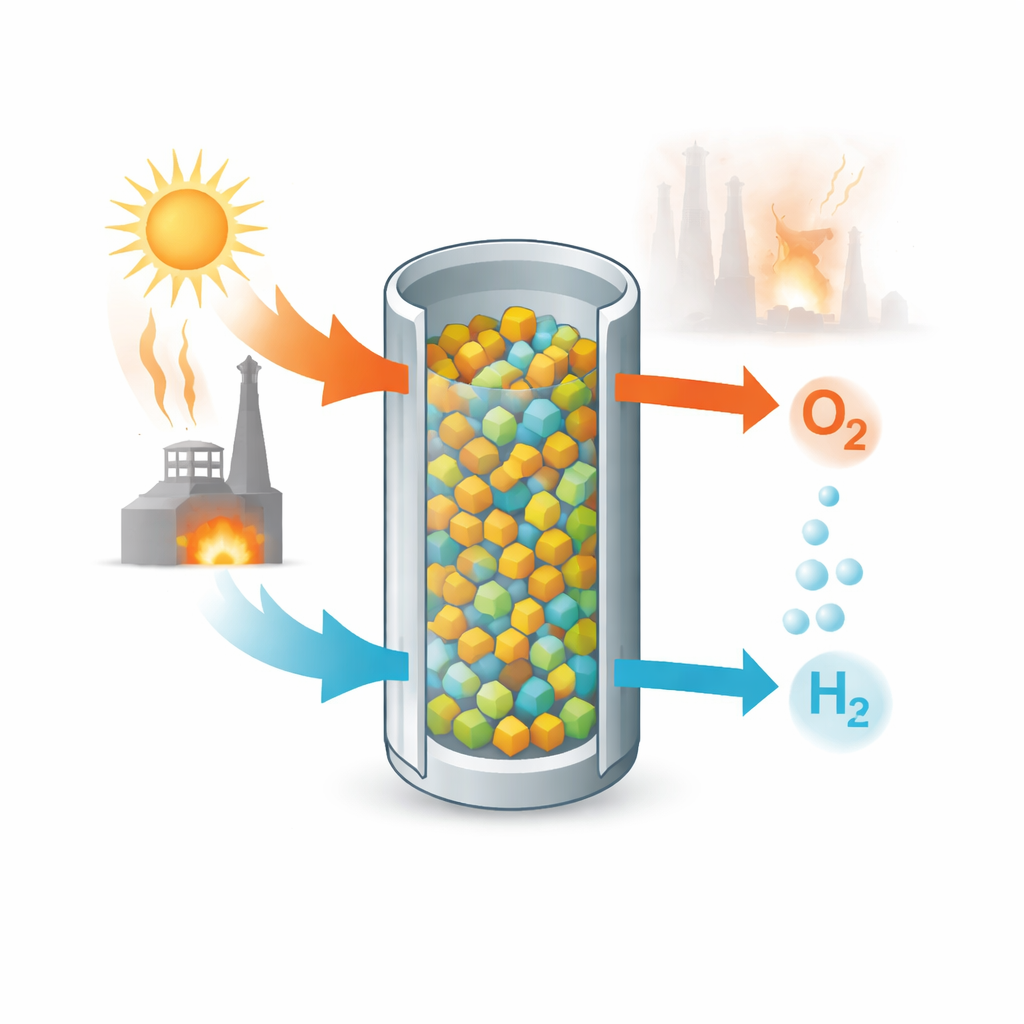
Une danse en deux étapes avec l’eau
La technologie au cœur de ce travail est un cycle thermochimique « en deux étapes ». Dans la première étape, un oxyde solide est chauffé dans un gaz pauvre en oxygène afin de céder une partie de son oxygène. Dans la seconde étape, le solide partiellement vidé est exposé à de la vapeur d’eau à une température plus basse. Les sites d’oxygène manquants dans le solide arrachent l’oxygène des molécules d’eau, laissant derrière eux du dihydrogène. En répétant ces deux étapes — libération d’oxygène à haute température puis scission de la vapeur à température plus basse — le même solide fonctionne comme une éponge réutilisable qui expire alternativement de l’oxygène puis aide à produire de l’hydrogène.
Un nouveau solide assoiffé d’oxygène
L’équipe se concentre sur un composé appelé Pr3ZrO8−δ, abrégé en PZO. À température ambiante, le PZO adopte une structure cubique simple semblable à celle de l’oxyde de cérium, matériau de référence. Toutefois, contrairement à son cousin, le PZO contient naturellement un grand nombre d’atomes d’oxygène manquants, ou vacants, même avant tout chauffage. À l’aide de diffraction de neutrons et de rayons X, les chercheurs montrent que cette structure fortement déficiente en oxygène reste intacte de la température ambiante jusqu’à 900 °C, tant en air qu’en atmosphère inerte, et ils cartographient les conditions de stabilité du matériau versus celles menant à la décomposition en phases moins utiles.
Stocker et libérer l’oxygène à des températures plus favorables
Des mesures précises des variations de masse et du comportement électrique révèlent la quantité d’oxygène que le PZO peut céder et reprendre de manière réversible selon la température et l’atmosphère gazeuse. Par rapport à l’oxyde de cérium, le PZO peut retirer et réinsérer beaucoup plus d’oxygène à une même température, surtout dans la plage 600–900 °C. Lors de tests cycliques, le matériau est chauffé à 900 °C dans de l’argon pour libérer de l’oxygène, puis refroidi à 400 °C et exposé à de la vapeur. Sur dix cycles, le PZO fournit en moyenne environ 332 micromoles d’oxygène et 70 micromoles d’hydrogène par gramme de matériau — dépassant les oxydes à base de cérium et les pérovskites de pointe, bien qu’il fonctionne à plusieurs centaines de degrés de moins que de nombreux systèmes actuels.
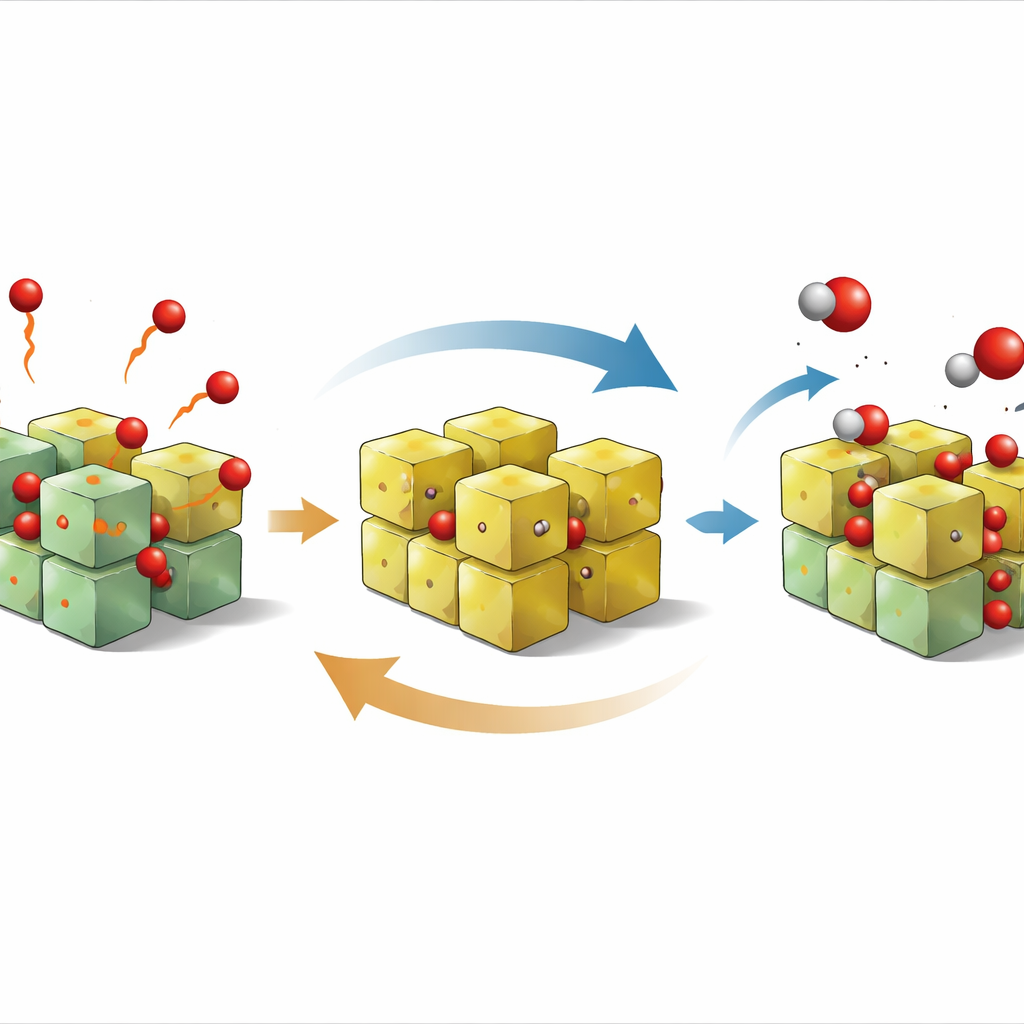
Observer la surface en action
Pour comprendre pourquoi la production d’hydrogène reste inférieure au maximum théorique permis par le nombre de vacants d’oxygène, les auteurs utilisent des simulations de mécanique quantique pour examiner comment une molécule d’eau se dissocie sur la surface la plus stable du PZO. Ils suivent une séquence d’événements : un atome d’oxygène quitte le cristal pour créer un site vacant ; l’eau se fixe à ce site ; la molécule se scinde en deux fragments hydroxyles ; et enfin les atomes d’hydrogène se regroupent et partent sous forme de dihydrogène tandis que l’oxygène comble la vacance. Les calculs montrent que l’étape la plus lente et la plus énergivore est la rupture d’une liaison O–H particulière à la surface. Ce goulot d’étranglement explique pourquoi la partie de scission de l’eau du cycle est plus lente que l’étape de libération d’oxygène.
Qu’est-ce que cela signifie pour l’hydrogène de demain
En termes clairs, l’étude présente un nouveau solide robuste capable de stocker et d’échanger l’oxygène de manière très efficace à des températures « intermédiaires » élevées. Cela en fait un candidat prometteur pour des réacteurs alimentés par le soleil concentré ou par la chaleur résiduelle des usines, plutôt que par la combustion de combustibles fossiles. Bien que le matériau dépasse déjà les normes actuelles en maniement de l’oxygène et en production d’hydrogène à température modérée, son plein potentiel ne sera atteint que si l’étape de surface lente dans la scission de l’eau est accélérée — probablement en ajoutant des catalyseurs appropriés ou en ajustant sa composition. Si ces améliorations aboutissent, des systèmes à base de PZO pourraient rendre la production d’hydrogène et d’oxygène à grande échelle et à faible émission de carbone beaucoup plus pratique.
Citation: Lu, J., Zhang, Y., Chen, L. et al. A new highly oxygen-deficient and cubic Pr3ZrO8-δ for intermediate-temperature thermochemical production of oxygen and hydrogen. Nat Commun 17, 3091 (2026). https://doi.org/10.1038/s41467-026-69235-0
Mots-clés: hydrogène thermochimique solaire, matériaux de stockage d’oxygène, oxydes à activité redox, énergie à température intermédiaire, cycles de scission de l’eau