Clear Sky Science · fr
Phénotypes migratoires différentiels des neutrophiles humains et des cellules du cancer du sein dans une plateforme sans fil à champ électrique unidirectionnel
Guider les cellules par des forces invisibles
Nos corps sont remplis de petits voyageurs : des cellules immunitaires qui accourent aux infections et des cellules cancéreuses qui parfois s’échappent et se propagent. Cette étude explore une manière surprenante d’orienter ces cellules en utilisant des forces électriques invisibles, sans les toucher avec des électrodes ni faire circuler de courant dans leur milieu. Le travail montre que les cellules immunitaires et les cellules du cancer du sein perçoivent et répondent très différemment à ces champs électriques « sans fil », ouvrant la voie à des méthodes futures pour diriger les cellules utiles et éventuellement ralentir les nocives.

Une méthode sans fil pour façonner le mouvement cellulaire
On sait déjà que les champs électriques peuvent influencer de nombreux types de cellules, des cellules de la peau qui ferment une plaie aux cellules tumorales en mouvement. Mais presque toutes les expériences précédentes s’appuyaient sur des électrodes plongées directement dans le liquide, ce qui fait aussi passer un courant à travers l’échantillon. Ce courant peut changer involontairement la chimie autour des cellules, par exemple en modifiant l’acidité. Les auteurs voulaient répondre à une question fondamentale : le courant lui‑même est‑il nécessaire, ou les cellules peuvent‑elles percevoir uniquement le champ électrique ? Pour tester cela proprement, ils ont conçu un nouvel appareil « champ électrique unidirectionnel sans fil » (Wi‑uEF) basé sur une idée simple — la même physique qui gouverne un condensateur à plaques parallèles.
Une plateforme adaptée au microscope sur mesure
L’équipe a mis au point deux plaques de cuivre planes positionnées au‑dessus et au‑dessous d’une boîte de culture standard, maintenues par un support entièrement imprimé en 3D. Lorsqu’une tension est appliquée, un champ électrique stable apparaît à travers la boîte sans que des électrodes n’entrent jamais en contact avec le liquide. Des simulations numériques ont montré que le champ dans une région centrale d’observation est assez uniforme et peut être ajusté à des intensités similaires à celles que l’on trouve naturellement dans les tissus, par exemple autour des plaies en cours de cicatrisation. Des supports interchangeables acceptent soit des boîtes simples, soit des chambres microfluidiques plus complexes, transformant l’appareil en une plateforme flexible pour observer des cellules vivantes au microscope pendant l’application du champ.
Les cellules immunitaires suivent le champ, les cellules cancéreuses errent
Les chercheurs ont testé deux types cellulaires : des neutrophiles du sang périphérique humain, cellules immunitaires à déplacement rapide, et les cellules MDA‑MB‑231 du cancer du sein, une lignée tumorale très agressive. Les neutrophiles ont reçu un léger signal chimique pour les stimuler, puis ont été exposés à différentes intensités de champ sans fil. Le suivi précis de centaines de cellules a révélé qu’en moyenne les neutrophiles avaient tendance à se diriger vers le côté « cathode » du champ. Leurs trajectoires sont devenues plus organisées et moins aléatoires à mesure que le champ augmentait, surtout pour les cellules les plus mobiles, même si leur vitesse globale n’a pas beaucoup changé. En revanche, les cellules du cancer du sein ont réagi très différemment. Sous les mêmes champs sans fil elles se déplaçaient un peu plus vite, mais leurs trajectoires devenaient moins rectilignes et ne montraient pas de préférence nette pour l’un ou l’autre côté. Autrement dit, le champ les rendait plus agitées sans les rendre plus dirigées.
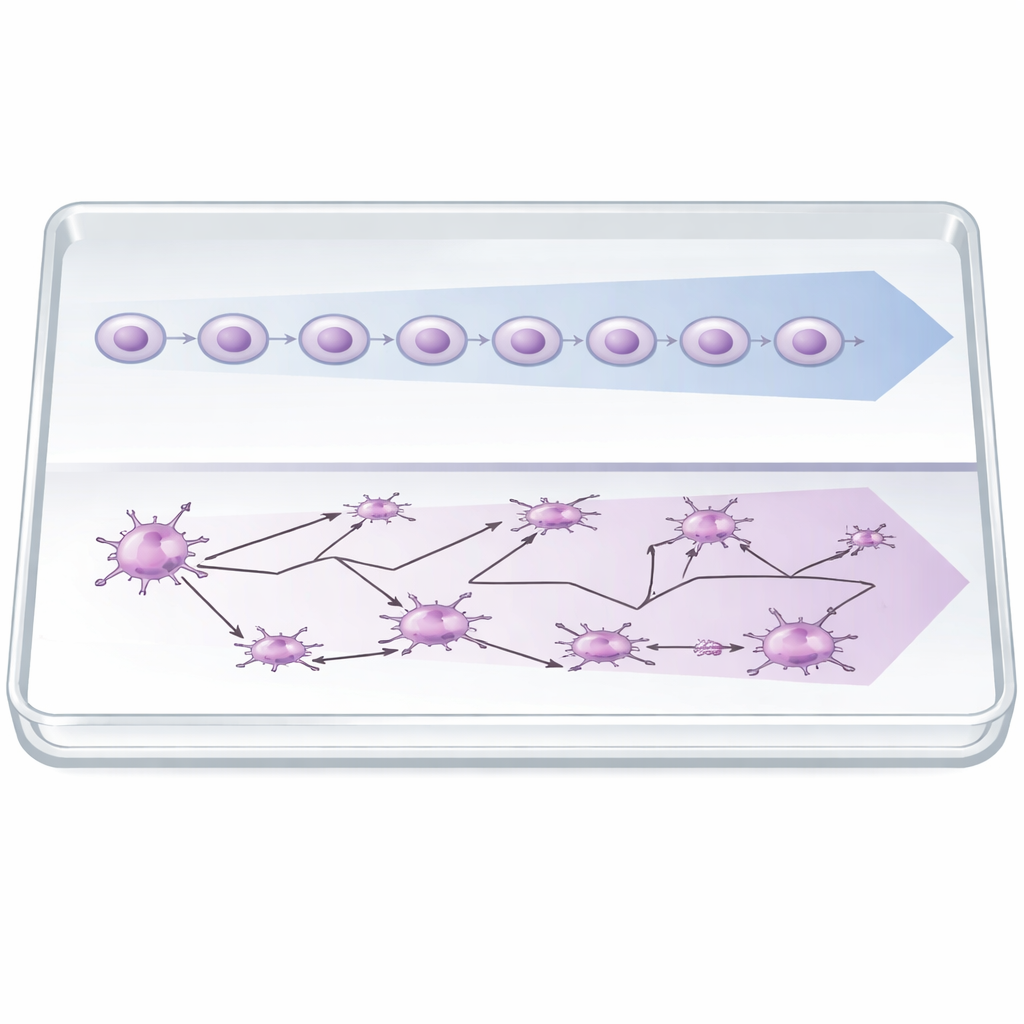
Comprendre les motifs avec une marche aléatoire
Pour expliquer comment le même signal physique pouvait produire des comportements opposés, l’équipe a utilisé un modèle simple de « marche aléatoire », une manière courante de décrire un mouvement composé de nombreux petits pas partiellement imprévisibles. Ils ont imaginé chaque cellule comme choisissant à plusieurs reprises une nouvelle direction, mais avec deux tendances ajustables : l’une à s’aligner sur le champ, l’autre à poursuivre globalement la même direction qu’auparavant. En ajustant ces deux tendances, le modèle a pu reproduire le comportement observé des neutrophiles — un alignement modéré sur le champ associé à un mouvement relativement stable — et celui des cellules cancéreuses — un alignement faible combiné à des changements de direction fréquents et à une persistance réduite. Le modèle a aussi rendu compte de l’observation selon laquelle les neutrophiles effectuant les plus longues distances étaient ceux les plus fortement guidés par le champ.
Quelles implications pour la médecine future
Dans l’ensemble, l’étude montre que les cellules peuvent percevoir et répondre à un champ électrique purement sans fil, même lorsque très peu ou pas de courant traverse leur environnement. Les neutrophiles considèrent le champ comme un indice directionnel, tandis que ces cellules du cancer du sein voient surtout leurs modes d’errance remodelés. Cette différence suggère que des champs sans fil soigneusement conçus pourraient un jour être utilisés pour attirer les cellules immunitaires vers les tumeurs ou les tissus enflammés tout en réduisant la migration dommageable des cellules cancéreuses. La plateforme Wi‑uEF, associée à un modèle simple mais puissant, ouvre la voie à l’exploration de la façon dont une large gamme de cellules immunitaires et tumorales réagissent à une guidance électrique douce et sans contact dans le corps.
Citation: Palmerley, N., Liu, Y., Stefanson, A. et al. Differential migratory phenotypes of human neutrophils and breast cancer cells in a wireless unidirectional electric field platform. Microsyst Nanoeng 12, 139 (2026). https://doi.org/10.1038/s41378-026-01267-4
Mots-clés: électrotaxie, neutrophiles, cellules du cancer du sein, champs électriques sans fil, migration cellulaire