Clear Sky Science · fr
Une puce micro-valée ouverte révèle des états d’invasion cellulaire du glioblastome induits à long terme par la viscosité
Pourquoi l’épaisseur des fluides cérébraux compte
Le glioblastome est l’un des cancers du cerveau les plus meurtriers, en partie parce que ses cellules excellent à s’infiltrer dans le tissu cérébral sain. Des travaux récents ont montré que le milieu liquide entourant ces cellules n’est pas uniforme : il devient plus épais et plus résistant à l’écoulement au niveau de la bordure invasive de la tumeur. Cette étude présente une petite puce ouverte qui imite cet environnement confiné et visqueux et suit la manière dont les cellules tumorales s’y adaptent progressivement. En observant les cellules sur des semaines plutôt que sur des heures, les chercheurs montrent comment certaines cellules de glioblastome deviennent plus petites, plus flexibles et plus invasives lorsqu’elles vivent dans un fluide plus épais, fournissant des indices sur la difficulté à contenir ces tumeurs.
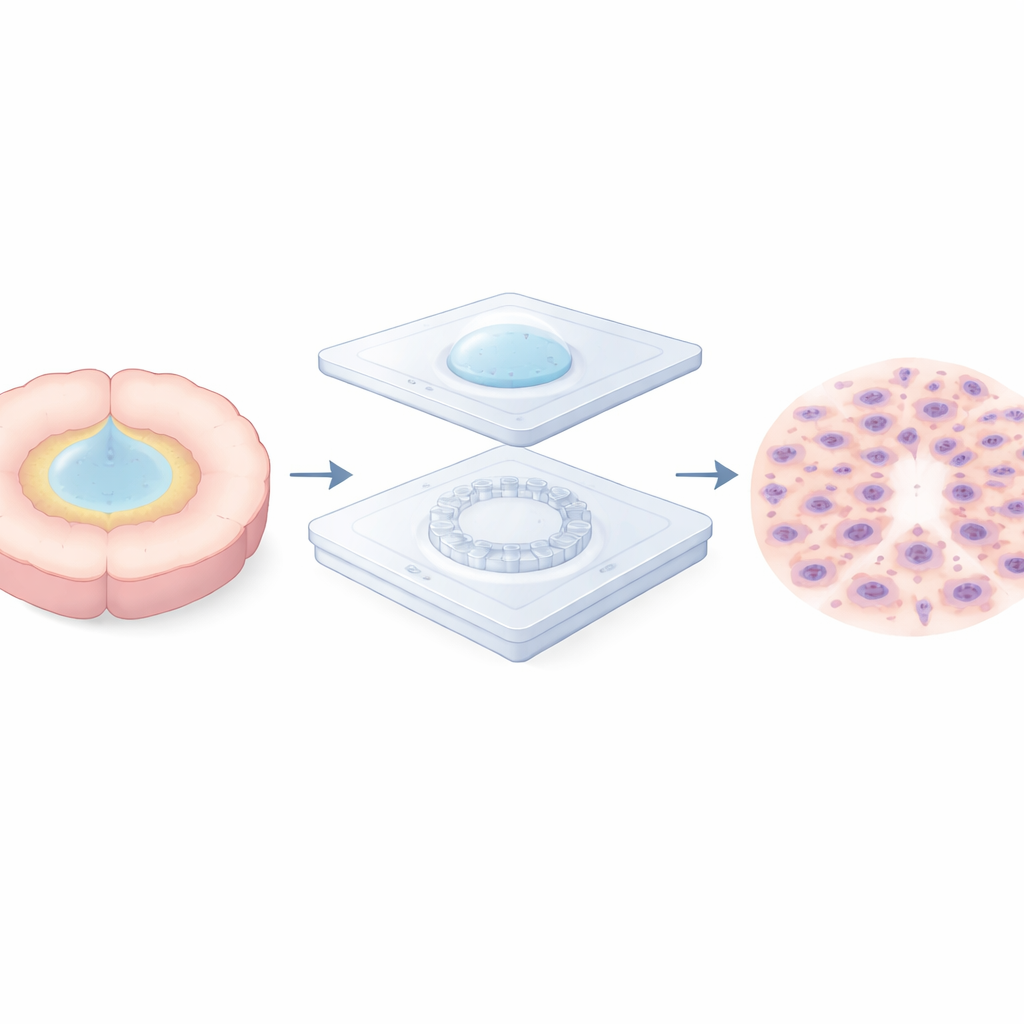
Un petit paysage pour modéliser le bord encombré d’une tumeur
Pour explorer ce problème, l’équipe a construit une puce microfluidique « micro-valée » à deux couches. La couche inférieure est une membrane mince et transparente, structurée par un anneau circulaire de micropiliers, laissant des vallées étroites entre eux. Un couvercle amovible sur le dessus emprisonne une petite gouttelette de cellules directement au-dessus de cet anneau, les maintenant en cercle serré pendant qu’elles se déposent et s’attachent. Après plusieurs heures, le couvercle et la gouttelette sont retirés et l’appareil est inondé de milieu frais, libérant les cellules pour qu’elles migrent vers l’extérieur à travers l’anneau de piliers. Cette simple opération de mise en place puis de retrait du capuchon permet aux chercheurs de lancer la migration cellulaire à un temps et en un lieu précisément définis, tout en gardant la surface ouverte à l’air et aux nutriments pour une observation à long terme.
Comment des passages étroits déforment et stressent les cellules tumorales
Une fois libérées, les cellules de glioblastome se propagent radialement dans l’anneau de piliers. L’espacement entre les piliers s’avère crucial. Quand l’écart est extrêmement étroit, les cellules tendent à franchir les sommets des piliers, évitant les espaces les plus exigus qui comprimeraient fortement leurs noyaux. Quand l’écart est plus large, les cellules s’insinuent entre les piliers, s’allongeant et déformant leurs noyaux pour s’adapter aux vallées. Ces petits changements de forme sont importants : dans la zone de la micro-valée, les cellules présentent des noyaux plus déformés et une augmentation d’activité de YAP, une protéine qui migre vers le noyau lorsque la cellule ressent un stress mécanique. Même si la puce est ouverte et non un tunnel fermé, le seul motif de surface suffit à comprimer le noyau et à activer cette voie de signalisation mécanique.
Des fluides plus épais entraînent les cellules à mieux envahir
Le cerveau autour d’un glioblastome n’est pas seulement confiné géométriquement, il est aussi inhabituellement visqueux : son liquide est plusieurs fois plus épais que l’eau. Pour reproduire cela, les chercheurs ont cultivé deux lignées cellulaires humaines de glioblastome dans un milieu épaissi avec de la méthylcellulose, ajustant sa viscosité pour correspondre aux mesures prises à la bordure invasive de la tumeur. Les cellules ont été maintenues dans ce milieu épaissi pendant environ un mois, leur laissant le temps de s’adapter. Lorsque ces cellules « pré-conditionnées » ont ensuite été placées sur la puce micro-valée, elles ont migré plus loin et plus vite que les cellules cultivées dans un milieu normal et fluide, surtout lorsqu’elles faisaient de nouveau face à un environnement plus épais. Les cellules adaptées étaient plus petites, avec des noyaux plus compacts, et elles traversaient les écarts entre piliers plus efficacement, envoyant souvent une ligne de tête de petites cellules très mobiles qui déblayaient le chemin pour des suiveuses plus grandes. Un test d’invasion standard utilisant des membranes poreuses a confirmé que les cellules pré-conditionnées franchissaient mieux les barrières, renforçant l’idée que l’exposition chronique à une viscosité élevée les rend plus invasives.
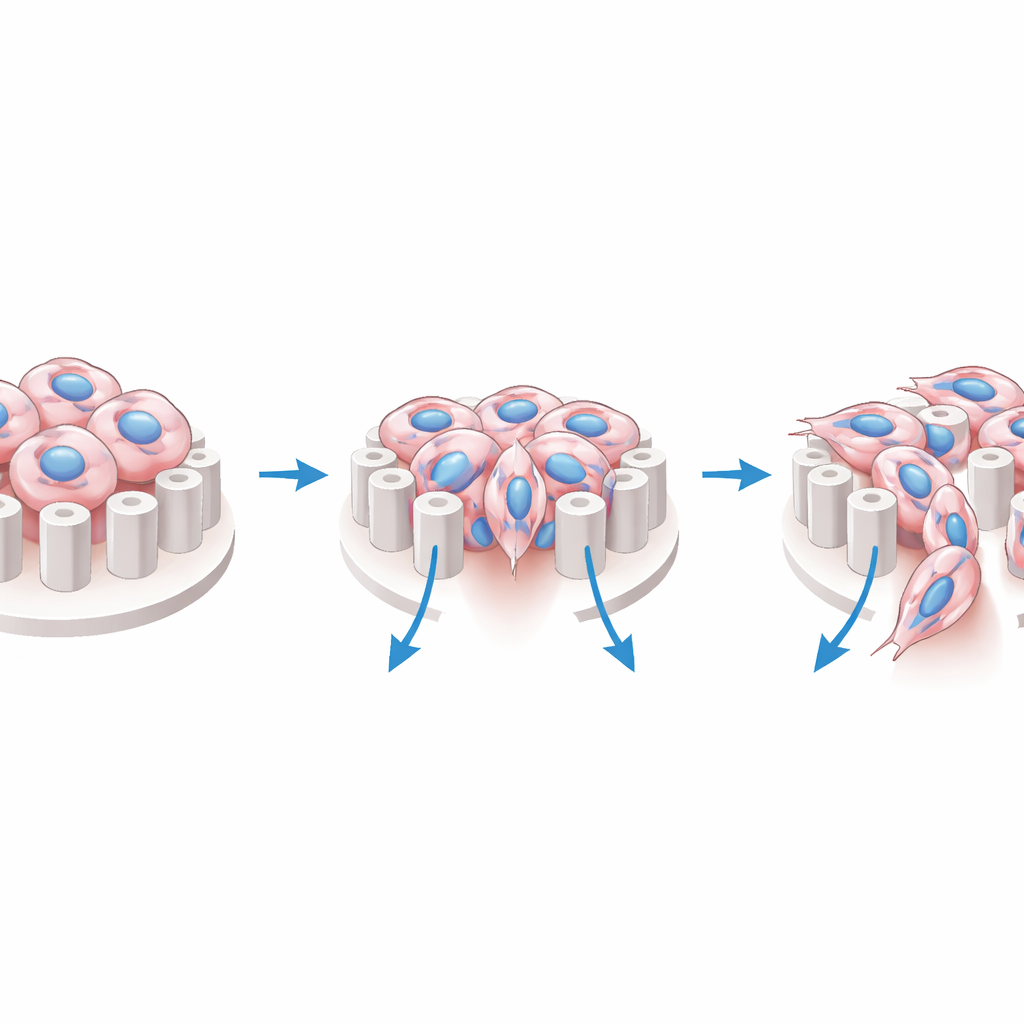
Des cellules tumorales différentes, des modes d’adaptation différents
Toutes les cellules de glioblastome ne réagissent pas de la même façon. Au microscope, les deux lignées testées ont remanié leur échafaudage interne et leurs points d’attache après une culture viscosa à long terme, montrant des ajustements structurels globalement similaires. Mais l’examen de l’activité génique a révélé une divergence. Une lignée, U-251, a reconduit son expression génique vers un état de type mésenchymateux — un profil associé à des cellules mobiles, capables de changer de forme et de remodeler leur environnement. L’autre, LN-229, a modifié son comportement et sa structure sans un changement génétique aussi marqué, conservant une identité plus stable. Les mesures de protéines clés ont corroboré ce tableau, et les modifications observées chez U-251 ont persisté même lorsque les cellules ont été replacées dans un milieu de viscosité normale, suggérant que l’exposition à un fluide épais peut verrouiller un état plus agressif plutôt que de simplement provoquer une réponse passagère.
Ce que cela signifie pour la compréhension et le traitement du glioblastome
Dans l’ensemble, l’étude montre que l’épaisseur du fluide entourant les cellules de glioblastome n’est pas un détail de fond ; c’est un signal puissant qui peut pousser de manière durable certaines cellules vers des états hautement invasifs. La puce micro-valée ouverte capture à la fois la compression physique et la traînée induite par un environnement visqueux, révélant comment ces forces déforment les noyaux, activent des protéines de signalisation mécanique comme YAP, et, au fil du temps, sélectionnent des cellules plus petites, plus déformables et plus mobiles. Parce que l’appareil est ouvert et compatible avec l’imagerie courante et les essais moléculaires, il pourrait servir à tester des médicaments visant à bloquer l’invasion ou à perturber les voies de mécanosensation dans des conditions qui ressemblent davantage au cerveau réel. Pour les patients, ce travail souligne que des thérapies efficaces devront prendre en compte non seulement le profil génétique de la tumeur, mais aussi le paysage physique particulier dans lequel ses cellules évoluent.
Citation: Jiang, H., Xu, C., Zeng, C. et al. Open micro-valley chip reveals long-term viscosity-induced glioblastoma cellular invasion states. Microsyst Nanoeng 12, 130 (2026). https://doi.org/10.1038/s41378-026-01241-0
Mots-clés: invasion du glioblastome, microenvironnement tumoral, mécanique cellulaire, puce microfluidique, viscosité extracellulaire