Clear Sky Science · fr
Définir les réponses synoviales subcellulaires au début de l’arthrose de l’ATM via des modèles de stress mécanique et de dérangement du disque articulaire
Pourquoi l’usure de l’articulation mandibulaire compte
L’articulation de la mâchoire, ou articulation temporo‑mandibulaire (ATM), permet de mastiquer, parler et bâiller. Lorsqu’elle commence à se dégrader — une affection appelée arthrose de l’ATM — les personnes peuvent souffrir de douleurs chroniques, de difficultés à s’alimenter et d’une baisse de la qualité de vie. Pourtant, comparée au genou ou à la hanche, cette petite articulation complexe a été beaucoup moins étudiée. Cet article utilise des outils de cartographie génétique de pointe sur des modèles murins pour révéler, avec un niveau de détail sans précédent, ce qui se passe à l’intérieur de la fine membrane articulaire lorsque l’arthrose de l’ATM débute.
Deux façons de surcharger une articulation mandibulaire
Pour reproduire des problèmes courants observés chez les patients, les chercheurs ont créé deux types de lésions de l’ATM chez la souris. Dans l’un, ils ont modifié l’occlusion dentaire de façon que la mâchoire se ferme de travers, surchargeant ainsi à répétition l’articulation — cela représente le stress mécanique dû à un mauvais alignement de la morsure. Dans l’autre, ils ont chirurgicalement avancé et fixé de façon anormale le disque amortisseur de l’articulation, imitant un disque déplacé souvent associé à la douleur d’ATM. Les deux modèles ont été comparés à des animaux témoins sains sur trois semaines, pendant que la structure osseuse et les modifications tissulaires étaient évaluées par tomographie 3D et microscopie. 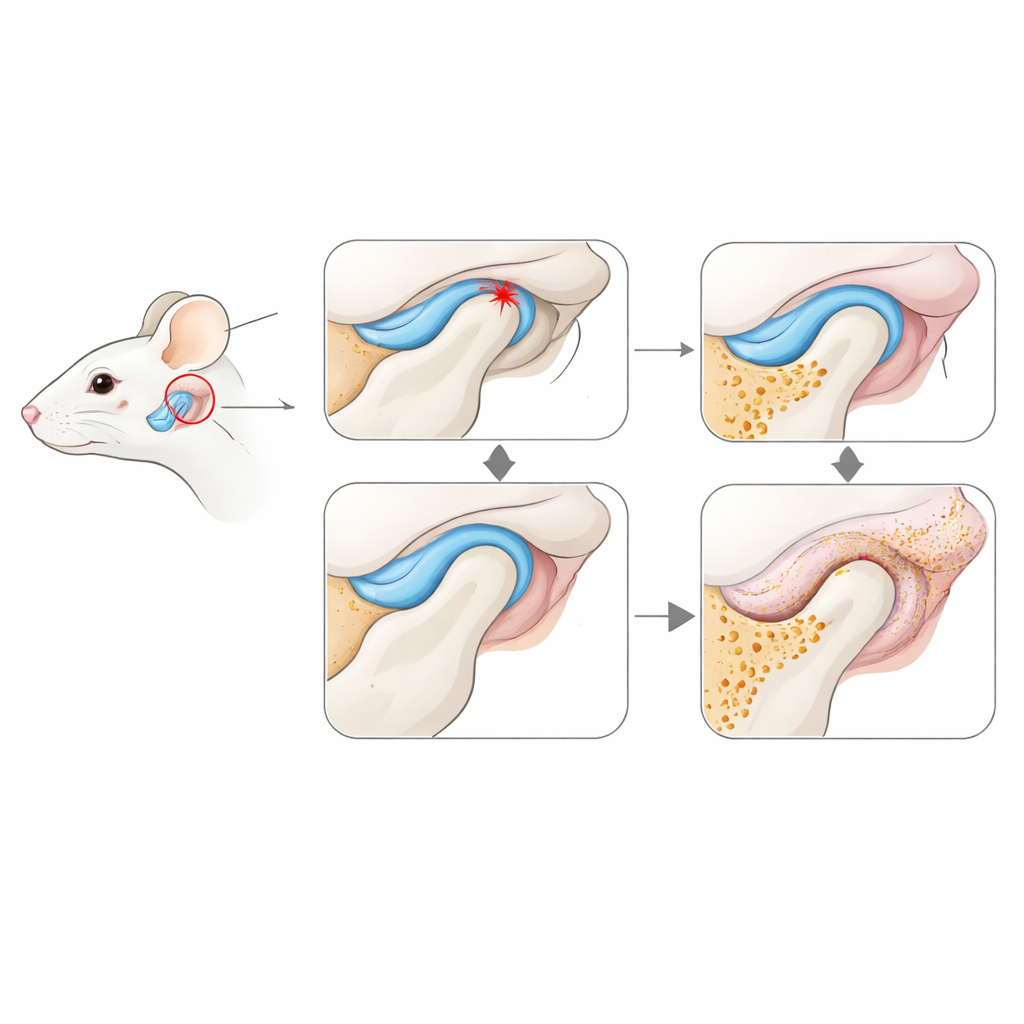
Dommages précoces de l’os, du cartilage et de la membrane articulaire
Les articulations soumises au stress et celles avec disque déplacé ont rapidement montré des signes caractéristiques d’arthrose débutante. La tête osseuse de la mâchoire a perdu de la densité minérale et développé des puits, des excroissances osseuses et une activité accrue des ostéoclastes, indiquant un remodelage trop rapide de l’armature interne de l’articulation. Le cartilage, qui fournit normalement une surface glissante, a commencé à s’amincir, à se fissurer et à perdre des molécules protectrices, notamment dans le modèle de déplacement du disque. Parallèlement, la synoviale — la fine muqueuse qui nourrit l’articulation — s’est épaissie, s’est enrichie en cellules et est devenue localement adipeuse ou fibreuse. Ces changements structurels suggèrent que la membrane articulaire n’est pas un simple spectateur, mais un acteur clé du déclenchement de la dégénérescence articulaire.
Lire les signaux moléculaires de l’articulation cellule par cellule
Pour dépasser l’anatomie et voir ce que faisaient les cellules individuelles, l’équipe a examiné quels gènes étaient activés à l’échelle de milliers de cellules en utilisant le séquençage ARN en vrac, le séquençage ARN unicellulaire et la transcriptomique spatiale à haute résolution. Ces méthodes leur ont permis de préciser quand et où différents types cellulaires modifiaient leur comportement. À l’extrémité osseuse de l’articulation, les gènes qui maintiennent normalement la santé du cartilage étaient réprimés, tandis que les gènes liés à la dégradation tissulaire et à l’activité ostéoclastique étaient augmentés, surtout dans le modèle de déplacement du disque. Dans la synoviale, les cellules ont amplifié la production de médiateurs inflammatoires, d’enzymes digestives tissulaires et de molécules associées à la cicatrisation et à la fibrose. Un point chaud particulièrement important était la partie postérieure de la membrane du disque, où inflammation, accumulation lipidique et épaississement fibreux se sont conjugués précocement.
Communication cellulaire et nouvelle cartographie de l’articulation mandibulaire
En analysant l’activité génique cellule par cellule et en replaçant ces cellules à leur position exacte dans le tissu, les auteurs ont identifié des quartiers distincts de fibroblastes (cellules de soutien), de cellules immunitaires et de cellules endothéliales (formatrices de vaisseaux) au sein de la synoviale. Ces types cellulaires semblent dialoguer via des voies de signalisation sensibles à la déformation mécanique et à l’inflammation. Par exemple, les signaux de la voie Notch — connue pour réguler les vaisseaux et le remodelage tissulaire — étaient particulièrement actifs dans les cellules endothéliales des articulations lésées, probablement sous l’influence des fibroblastes voisins. Les mêmes régions présentaient aussi des niveaux élevés d’enzymes destructrices de cartilage et des marqueurs de fibrose, renforçant l’idée que des cellules synoviales stressées peuvent promouvoir la perte de cartilage et la douleur. 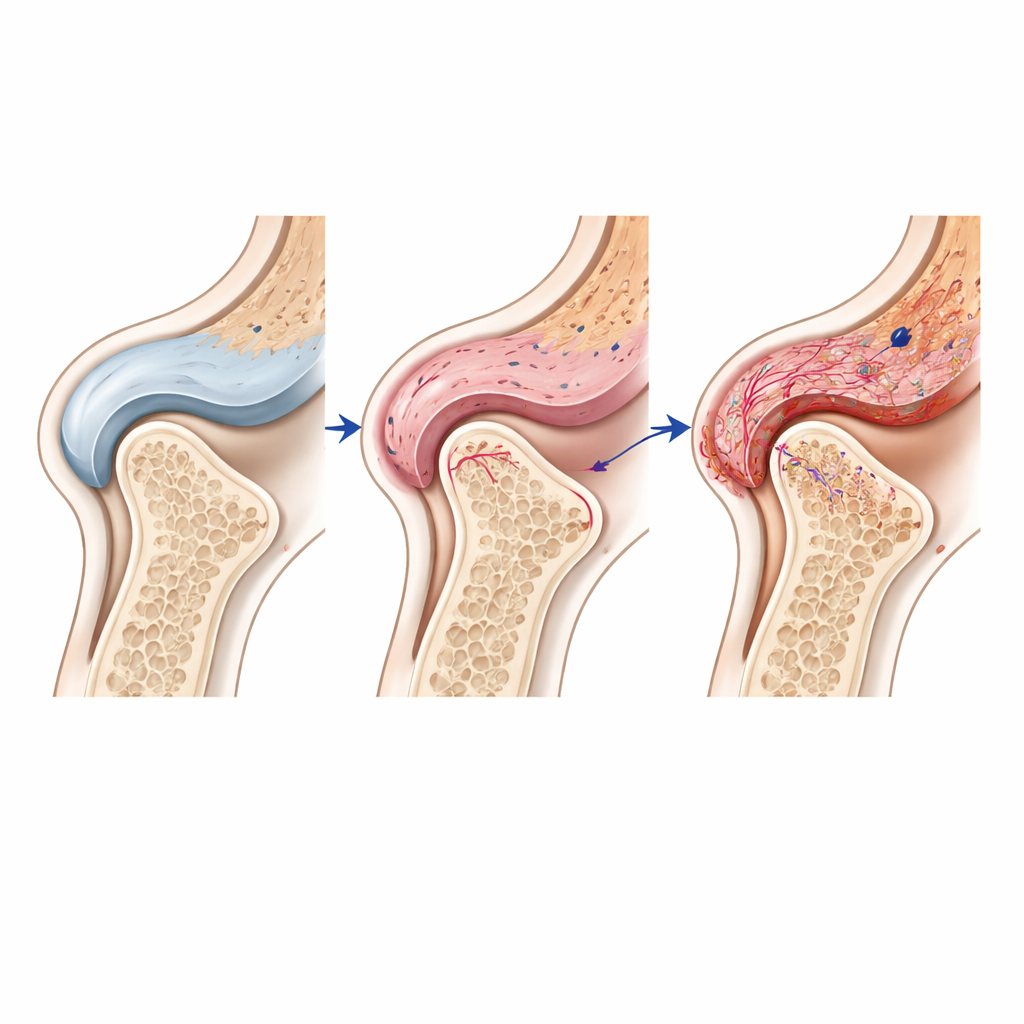
Comment ce travail peut orienter les traitements futurs
Plutôt que de tester un médicament précis, cette étude fournit une atlas détaillé des réponses de la membrane synoviale et du cartilage de l’ATM aux forces nocives dès les premiers stades de la maladie. Elle montre que l’arthrose précoce de l’ATM se caractérise par des changements coordonnés dans l’os, le cartilage et surtout les cellules synoviales, qui deviennent inflammatoires et fibreuses tout en émettant des signaux délétères vers l’articulation. En reliant ces modifications à des types cellulaires et des localisations précises, le travail met en lumière de nouvelles cibles thérapeutiques potentielles — comme les voies de signalisation Notch, les voies des chimiokines et les enzymes dégradant la matrice — qui pourraient être bloquées avant que les lésions articulaires ne deviennent irréversibles. En bref, l’article fournit une feuille de route puissante pour comprendre et éventuellement interrompre la chaîne d’événements qui transforme les mouvements quotidiens de la mâchoire en douleur chronique d’ATM.
Citation: Shibusaka, K., Negishi, S., Terashima, A. et al. Defining subcellular synovial responses in TMJ osteoarthritis onset via mechanical stress and articular disk derangement models. Int J Oral Sci 18, 28 (2026). https://doi.org/10.1038/s41368-025-00411-6
Mots-clés: articulation temporo‑mandibulaire, arthrose, synoviale, stress mécanique, transcriptomique unicellulaire