Clear Sky Science · fr
Une cartographie multi-omique unicellulaire de la peau périnatale de la souris trace la spécification des lignées et révèle des dynamiques communes dans la peau fœtale humaine
Pourquoi la peau du nourrisson recèle des indices pour la réparation
La peau du nouveau-né peut faire pousser des poils et se réparer d’une manière que la peau adulte ne peut plus égaler. En examinant de près le développement de la peau de souris autour de la naissance, puis en le comparant à la peau fœtale humaine, les chercheurs mettent au jour des programmes cellulaires qui pourraient un jour être exploités pour améliorer la cicatrisation et la régénération pilaire.
Observer la peau cellule par cellule
Pour comprendre en détail la peau en développement, les scientifiques ont utilisé des méthodes unicellulaires qui mesurent à la fois les gènes actifs et la compaction de l’ADN dans chaque cellule. Ils se sont concentrés sur la peau dorsale de la souris de la fin de la gestation jusqu’aux premiers jours après la naissance et ont combiné leurs nouvelles données à plusieurs jeux de données publics. Cela leur a permis de suivre de nombreux types cellulaires cutanés, y compris les cellules superficielles, les cellules formatrices de poils et différents fibroblastes des couches profondes, au fil du temps. Ils ont aussi utilisé des techniques spatiales qui préservent la position de chaque cellule dans le tissu, ajoutant une perspective cartographique du paysage cutané. 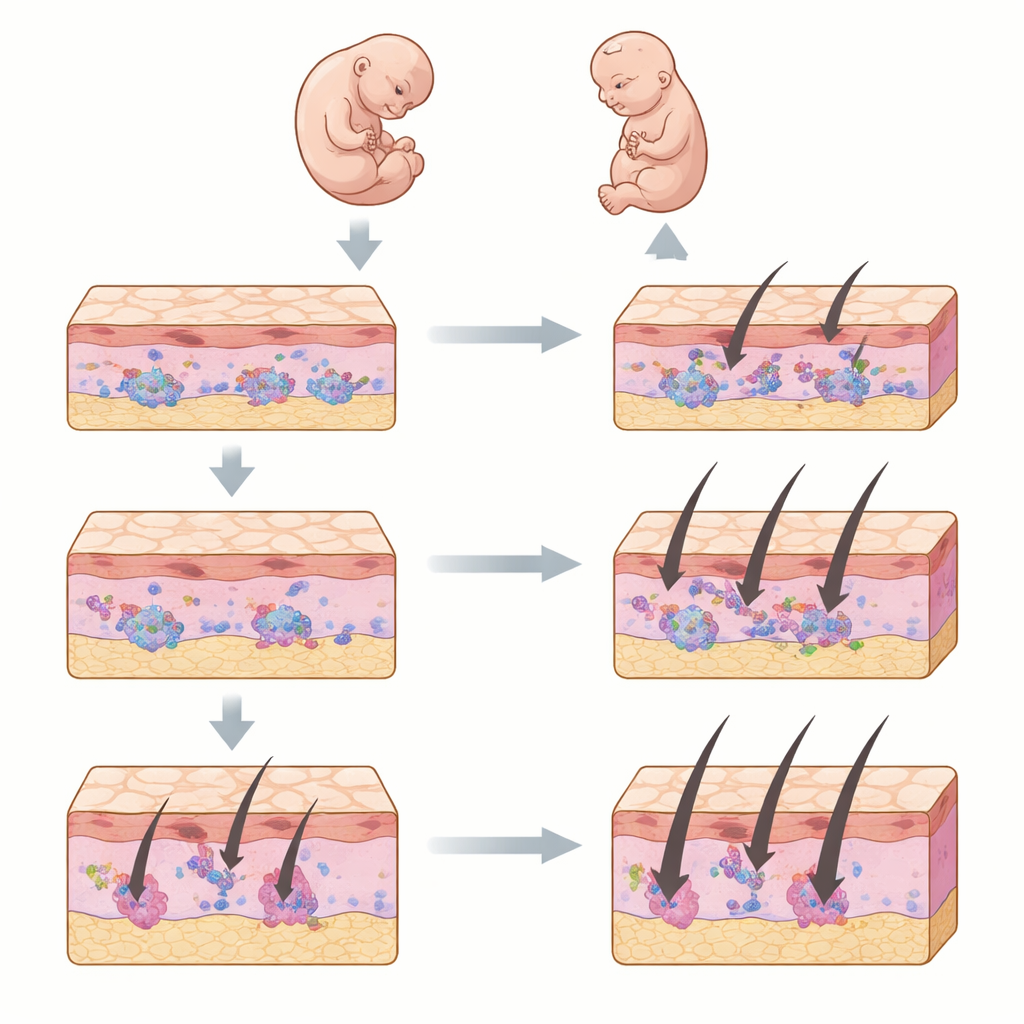
Un paysage changeant à l’intérieur de la peau néonatale
L’équipe a observé que l’« ouverture » de l’ADN dans les cellules cutanées évolue rapidement pendant la période périnatale. Ces modifications, qui contrôlent quels gènes peuvent être activés, suivent de près les changements d’identité cellulaire. Les premières cellules superficielles ont donné naissance aux cellules des follicules pileux et aux couches qui forment la barrière cutanée. En profondeur, les fibroblastes précoces se sont scindés en plusieurs trajectoires, incluant des cellules qui soutiennent les racines des poils, des cellules adipeuses, ainsi que des fibroblastes distincts des compartiments supérieurs et inférieurs. Certains gènes marqueurs présentaient une accessibilité de l’ADN dans plusieurs groupes de fibroblastes alors qu’ils n’étaient exprimés que dans quelques-uns, ce qui suggère que les fibroblastes jeunes conservent des potentialités avant de se spécialiser définitivement.
Identifier l’origine des petits muscles cutanés
Un point clé portait sur le muscle arrecteur pili, le petit muscle lisse qui redresse les poils et aide à soutenir les cellules souches folliculaires. Ses origines durant le développement restaient floues. En combinant les profils d’accessibilité de l’ADN, l’activité génique et les cartes spatiales, les chercheurs ont identifié un groupe de fibroblastes du compartiment supérieur de la peau de souris exprimant le gène Mef2c comme précurseurs probables de ce muscle. Un second gène, Myocd, se comportait comme un noyau régulateur fort dans ces cellules. Des simulations informatiques ont prédit que la suppression de Mef2c gênerait l’émergence à la fois de ces fibroblastes et du muscle arrecteur pili. Des expériences en laboratoire ont soutenu cette hypothèse : la réduction des niveaux de Mef2c dans des fibroblastes en culture diminuait l’activité de Myocd et d’un marqueur musculaire connu. 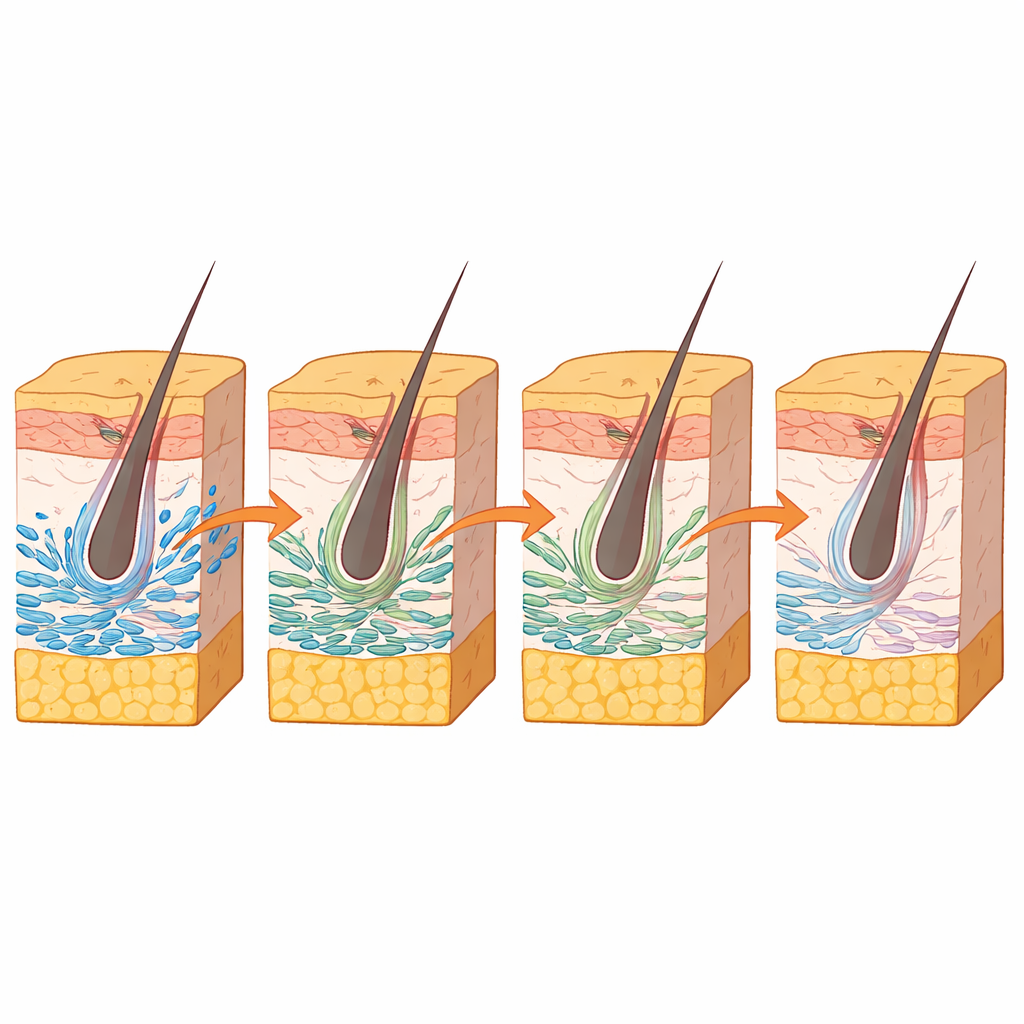
La souris et l’humain partagent un scénario développemental commun
Pour tester la transposabilité des résultats de la souris à l’humain, l’équipe a comparé leurs cartographies cellulaires de la souris à un atlas récemment publié de la peau fœtale humaine. Une approche computationnelle a aligné les types cellulaires entre espèces et stades de développement. Malgré des différences de chronologie, les composantes cutanées de souris et d’humain présentaient de fortes correspondances, en particulier parmi les fibroblastes. Les chercheurs ont identifié un groupe de fibroblastes humains MEF2C-positifs ressemblant à la population précurseure de la souris et ont établi le moment d’apparition du muscle arrecteur pili humain et des structures dermiques associées. L’ordre d’apparition des différents types de fibroblastes était similaire dans les deux espèces, ce qui indique un scénario développemental partagé.
Ce que cela implique pour la réparation cutanée future
Dans l’ensemble, l’étude offre une vue détaillée et multi-couches de la manière dont les types cellulaires cutanés et leurs systèmes de contrôle génétique se déploient au début de la vie. Pour le grand public, l’idée principale est que certains fibroblastes néonatals semblent conserver un état flexible et régénératif, à partir duquel des structures comme les petits muscles pilaires peuvent encore se former. Puisque des types cellulaires et des chronologies similaires existent dans la peau fœtale humaine, ces cartes fournissent un point de départ pour concevoir des thérapies susceptibles d’inciter la peau adulte à retrouver des états plus juvéniles et favorables à la réparation, sans reproduire directement le développement précoce.
Citation: Lee, H., Lee, S., Jo, S.J. et al. A multi-omic single-cell landscape of perinatal mouse skin maps lineage specification and reveals shared dynamics in human fetal skin. Exp Mol Med 58, 1269–1283 (2026). https://doi.org/10.1038/s12276-026-01692-5
Mots-clés: développement cutané, fibroblastes, follicule pileux, analyse unicellulaire, muscle arrecteur pili