Clear Sky Science · es
Dos modos distintos de regulación Tead mediada por Vgll4 controlan el tamaño del órgano en pez cebra
Cómo los órganos diminutos saben cuándo dejar de crecer
Nuestros cuerpos están llenos de órganos y tejidos pequeños que, de algún modo, crecen hasta el tamaño adecuado y luego se detienen. Este equilibrio es crucial: si hay muy poco crecimiento, los órganos no pueden funcionar; si hay demasiado, aumenta el riesgo de cáncer. Este estudio utiliza un embrión de pez cebra transparente y uno de sus sistemas sensoriales para desentrañar cómo las células regulan finamente el crecimiento, revelando una pugna interna entre señales que fomentan la expansión y otras que aplican el freno.
Una cadena móvil de sensores en un pez bebé
Para investigar el control del tamaño del órgano, los investigadores se centraron en la línea lateral posterior, una hilera de diminutos órganos sensoriales a lo largo del costado del pez que detectan el movimiento del agua. Estos órganos se originan a partir de un grupo compacto de unas 120 células, llamado primordio, que brota de un parche de tejido cercano al oído y luego se desplaza por la piel dejando grupos sensoriales atrás. Debido a que esta estructura es pequeña, está expuesta en la superficie y se desarrolla de manera predecible, es un laboratorio vivo ideal para observar cómo se regula el crecimiento célula por célula. Utilizando microscopía de alta resolución y recuento celular tridimensional automatizado, el equipo pudo medir con precisión cuántas células contiene el primordio, cuál es su tamaño y si su arquitectura interna permanece intacta cuando se activan o desactivan genes. 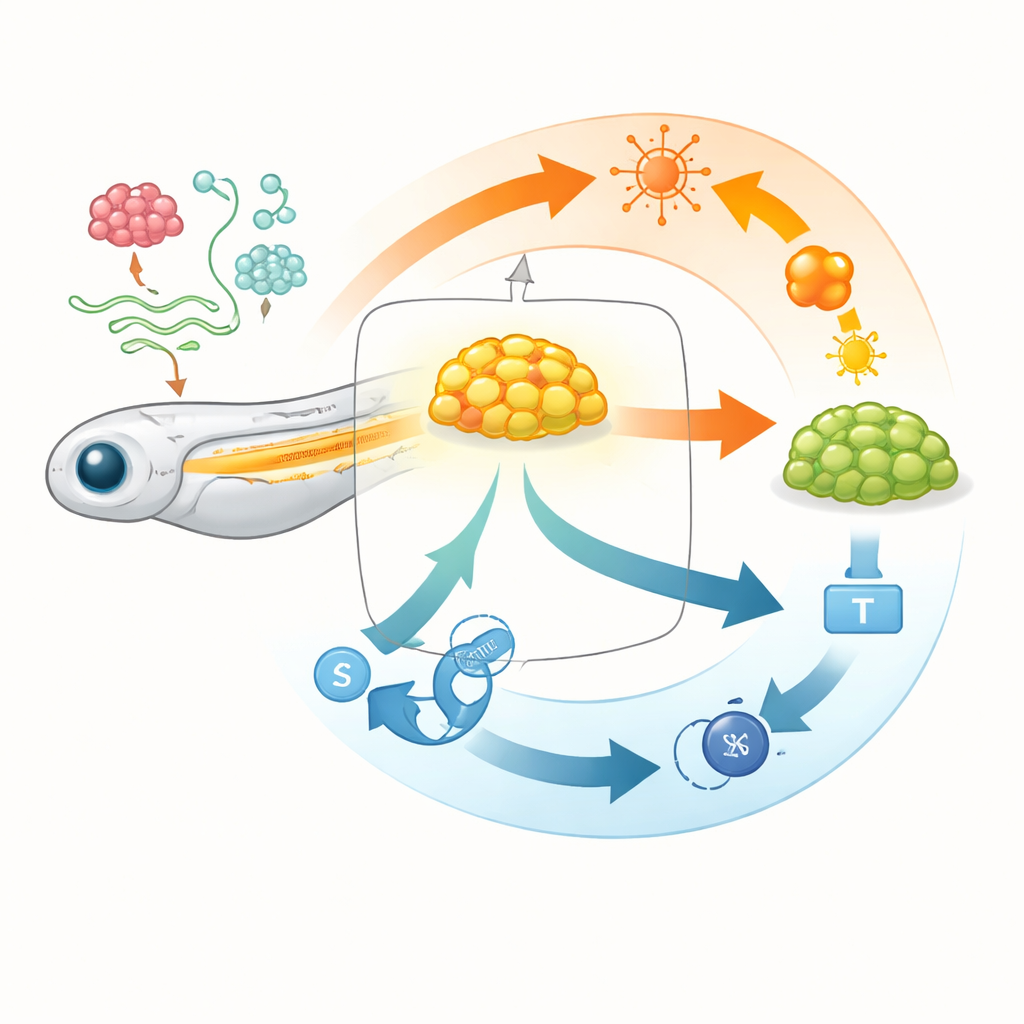
Un interruptor de crecimiento que necesita un compañero
Trabajos anteriores habían mostrado que una proteína llamada Yap1, parte de la vía de señalización Hippo, fomenta la multiplicación celular. Aquí los autores demuestran que la capacidad de Yap1 para promover el crecimiento en el primordio depende absolutamente de otra familia de proteínas conocidas como Teads, que se asocian al ADN y ayudan a controlar la actividad génica. Cuando se eliminó Yap1, o cuando se usó una forma mutante que ya no puede unirse a Tead, el primordio quedó más pequeño y más redondeado, con aproximadamente un cinco por ciento menos de células. Suministrar Yap1 normal restauró el número de células, pero la versión deficiente en unión a Tead no pudo hacerlo, lo que muestra que la asociación Yap1–Tead es el interruptor clave que promueve el crecimiento en este tejido.
El freno incorporado: dos versiones de un supresor tumoral
Sin embargo, el crecimiento no se activa y se deja funcionando sin más. El equipo examinaron Vgll4, una proteína conocida previamente por actuar como supresor tumoral en mamíferos al contrarrestar señales similares a Yap1. El pez cebra posee dos versiones relevantes, Vgll4b y Vgll4l, que están ambas activas en el primordio. Cuando se desactivaron estos genes, el primordio llegó a contener hasta un 50 por ciento más células y se hizo más grande, aunque su patrón interno de agrupamiento celular se mantuvo. Por el contrario, añadir Vgll4b extra redujo el número de células en torno a un 20 por ciento. Vgll4l también pudo compensar, pero solo cuando estaba presente en niveles más altos, lo que indica que Vgll4b es el freno más potente. La disección molecular mostró que una región específica de Vgll4b, conocida como TDU2, es especialmente importante para conectarse con Tead y hacer cumplir este límite de crecimiento.
Dos maneras de contener el crecimiento
Combinando cruces genéticos, sobreexpresión artificial y un reportero fluorescente que se enciende cuando Yap1–Tead está activo, los investigadores revelaron un papel dual de Vgll4. Primero, Vgll4 compite directamente con Yap1 por el acceso a Tead, impidiendo la formación de complejos que promueven el crecimiento y atenuando la señal que impulsa la división celular. En embriones sin Vgll4, aumentar Yap1 tuvo un efecto mucho más fuerte sobre el número de células que en peces normales, coherente con esta competencia. Segundo, incluso cuando Yap1 estaba ausente, el exceso de Vgll4 podía seguir provocando defectos marcados y un comportamiento anómalo del primordio, lo que implica que Vgll4 puede asociarse con Tead para apagar genes activamente, en lugar de limitarse a bloquear a Yap1. Así, Vgll4 actúa tanto como rival físico de Yap1 como socio por derecho propio que empuja a las células hacia la contención. 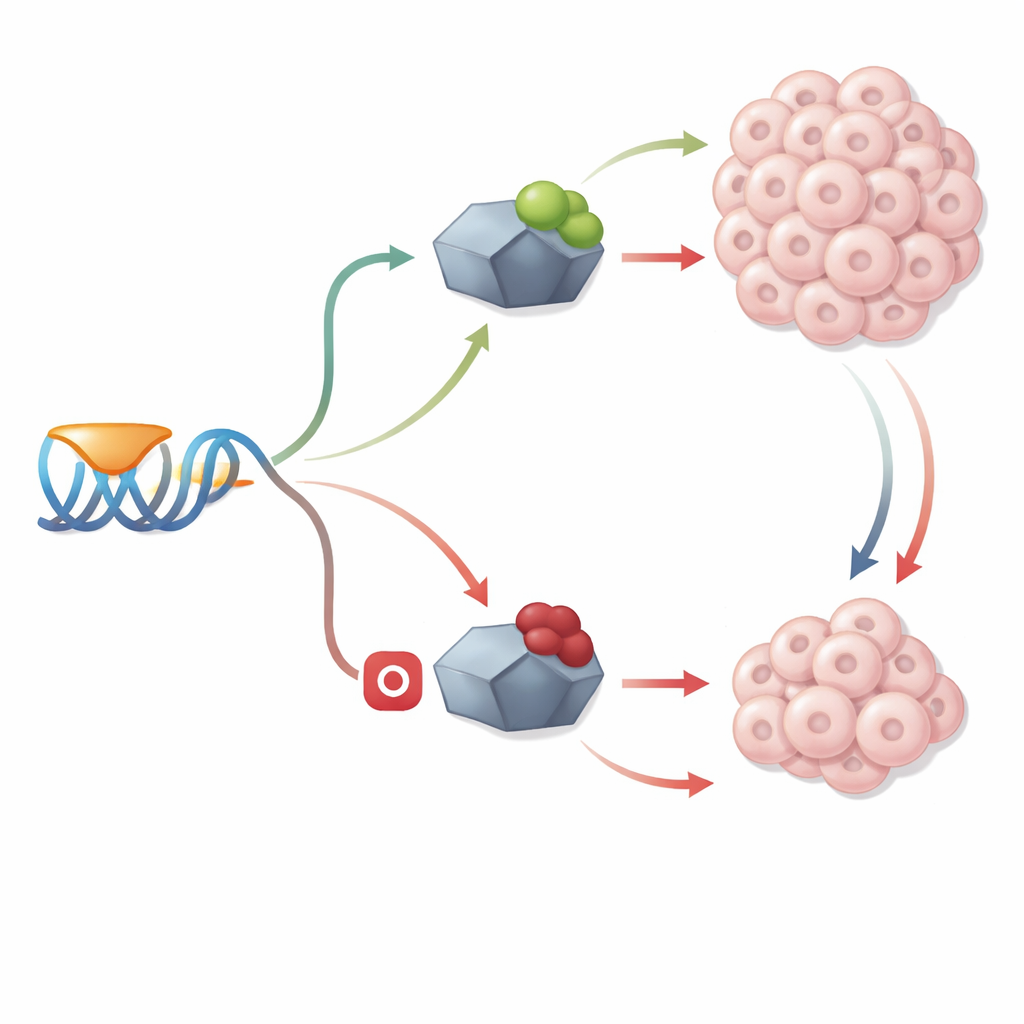
Temporizar el empuje y el tirón sobre el tamaño del órgano
El control del crecimiento también depende de cuándo actúan estas fuerzas moleculares. Usando un fármaco que bloquea selectivamente que proteínas similares a Yap1 se unan a Tead, el equipo identificó una ventana temprana crítica: entre aproximadamente 14 y 19 horas tras la fertilización, cuando el primordio se está formando desde la placoda original de tejido cerca del oído. En ese intervalo, la actividad de Yap1 es necesaria para acumular una reserva suficiente de células para la migración posterior. Después de esta etapa, bloquear Yap1–Tead tiene poco efecto sobre el tamaño final del primordio, y otras vías ayudan a mantener el crecimiento mientras el primordio viaja y deja atrás los órganos sensoriales.
Por qué esto importa para la salud y la enfermedad
En conjunto, estos hallazgos dibujan una imagen clara de cómo un órgano en desarrollo puede alcanzar el tamaño “justo”. Una señal pro‑crecimiento (Yap1 trabajando con Tead) expande el primordio en las primeras etapas, mientras que un conjunto opuesto de proteínas (Vgll4b y Vgll4l) tanto compite con Yap1 como reprime activamente los genes dirigidos por Tead para contener ese crecimiento. Este control dual hace que el sistema sea robusto: los tejidos pueden crecer lo suficiente para formarse correctamente y, al mismo tiempo, estar protegidos contra una expansión descontrolada. Debido a que los mismos actores moleculares operan en muchos órganos de vertebrados, incluidos los humanos, entender este equilibrio en el pez cebra ofrece pistas sobre cómo los órganos se moldean normalmente y cómo el desequilibrio podría contribuir al cáncer o a terapias regenerativas destinadas a reconstruir tejidos dañados de forma segura.
Cita: Lardennois, A., Duda, V., Dingare, C. et al. Two distinct modes of Vgll4-mediated Tead regulation control organ size in zebrafish. Commun Biol 9, 574 (2026). https://doi.org/10.1038/s42003-026-10098-y
Palabras clave: control del tamaño del órgano, señalización Hippo, Yap1 Tead, supresor tumoral VGLL4, línea lateral del pez cebra