Clear Sky Science · es
JanusDDG: una red neuronal informada por la física para la estabilidad de proteínas basada en la secuencia mediante atención de doble frente
Por qué esta investigación importa
Las proteínas son las pequeñas máquinas que mantienen vivas a nuestras células, y hasta un solo cambio en sus bloques constructores puede hacer que funcionen mejor, peor o que dejen de funcionar. Poder predecir cómo tales cambios afectan la estabilidad de una proteína es crucial para comprender enfermedades genéticas y para diseñar mejores fármacos y enzimas industriales. Este artículo presenta JanusDDG, un nuevo modelo de inteligencia artificial que predice cómo las mutaciones alteran la estabilidad proteica usando solo la secuencia de la proteína, al mismo tiempo que respeta las reglas físicas básicas que gobiernan el plegamiento proteico.
El problema de las máquinas proteicas frágiles
Cuando una proteína se pliega en su forma tridimensional, equilibra muchas fuerzas, como una tienda sostenida por muchas cuerdas. Las mutaciones pueden tensar algunas cuerdas o aflojar otras, haciendo la estructura más o menos estable. Las pruebas experimentales de estos efectos son lentas y costosas, por lo que los investigadores dependen en gran medida de modelos informáticos para estimar los cambios en estabilidad, conocidos como ΔΔG. Las herramientas existentes a menudo funcionan mejor cuando tienen acceso a estructuras 3D detalladas, y pueden, sin notarlo, incumplir las leyes de la termodinámica, lo que conduce a predicciones que parecen precisas sobre el papel pero que son físicamente inconsistentes o difíciles de confiar para proteínas nuevas.
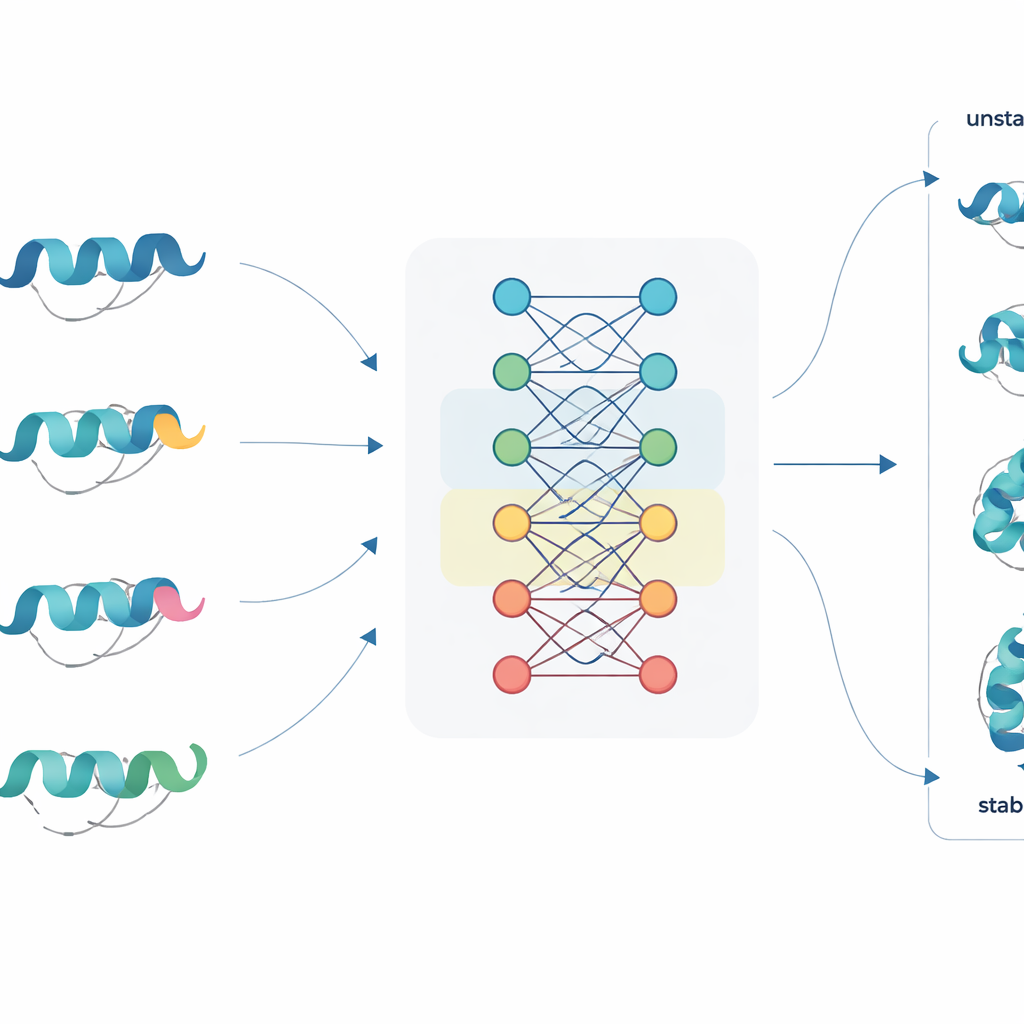
Una nueva forma de leer secuencias proteicas
JanusDDG aborda este reto partiendo de modelos de lenguaje para proteínas, una clase de grandes redes neuronales entrenadas con millones de secuencias proteicas, de manera análoga a cómo los modelos de lenguaje aprenden a partir de texto. Estos modelos convierten cada aminoácido en una representación numérica rica que captura patrones de la evolución y del comportamiento de plegamiento típico. JanusDDG toma la secuencia de la proteína original y la de su variante mutante, compara sus representaciones aprendidas y utiliza un mecanismo de atención especializado que se centra en cómo la mutación perturba el contexto circundante. Al necesitar solo secuencias, JanusDDG puede aplicarse a proteínas cuyas estructuras 3D son desconocidas o difíciles de determinar.
Incorporando la física en la inteligencia artificial
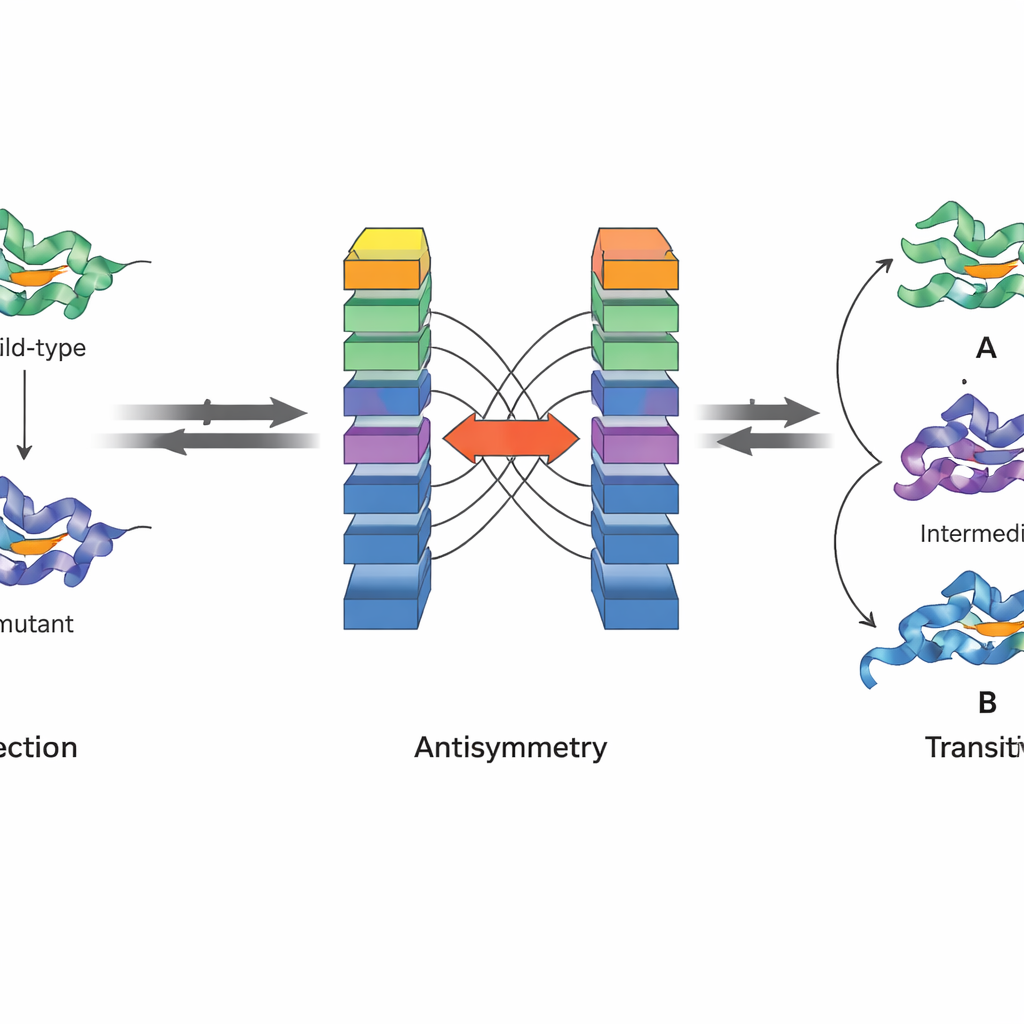
Una innovación clave de JanusDDG es que está diseñado para respetar principios físicos fundamentales. Los autores se centran en dos propiedades de la energía libre de Gibbs, la magnitud que subyace a la estabilidad proteica. Primero, la antisimetría significa que si pasar de una variante a otra cambia la estabilidad en cierta cantidad, el cambio inverso debe deshacer ese efecto. Segundo, la transitividad significa que el efecto total de pasar de una variante a una segunda y luego a una tercera debe ser igual al salto directo de la primera a la tercera. La arquitectura de JanusDDG hace cumplir la antisimetría ejecutando dos copias espejadas de la red con entradas intercambiadas y combinando sus salidas para que las predicciones hacia adelante y hacia atrás sean exactamente opuestas. La transitividad se fomenta durante el entrenamiento añadiendo un término de pérdida especial que empuja al modelo a hacer predicciones coherentes cuando las rutas mutacionales se descomponen en pasos.
Evaluación del rendimiento en muchos tipos de mutaciones
Los investigadores entrenaron JanusDDG con un conjunto de datos curado de miles de mutaciones con cambios de estabilidad medidos y luego lo probaron en varios bancos de prueba independientes donde la superposición de secuencias con los datos de entrenamiento se mantuvo muy baja. Este diseño cuidadoso reduce el riesgo de que el modelo esté simplemente memorizando proteínas familiares. En tres colecciones ampliamente usadas de mutaciones simples, JanusDDG igualó o superó tanto a otras herramientas basadas en secuencias como a muchos métodos que se basan en estructuras 3D. También manejó mutaciones múltiples simultáneas, un escenario más difícil donde las interacciones entre cambios pueden ser no aditivas. De manera notable, su precisión no disminuyó para pares de mutaciones cercanas en el espacio, donde modelos anteriores a menudo flaqueaban.
De números a etiquetas de estabilidad útiles
En aplicaciones prácticas, los investigadores a menudo quieren saber no solo cuánto cambia la estabilidad, sino si una mutación es claramente estabilizadora o desestabilizadora. Los autores probaron JanusDDG en un conjunto de datos centrado en distinguir variantes estabilizadoras de desestabilizadoras. Aunque el modelo alcanzó un rendimiento sólido, esta tarea siguió siendo más difícil que predecir valores numéricos crudos, especialmente en el límite entre categorías donde el ruido experimental y la ambigüedad biológica son mayores. Aun así, JanusDDG se comparó favorablemente con otros métodos de primer nivel, lo que sugiere que su diseño consciente de la física y el uso de incrustaciones ricas de secuencia le ayudan a manejar esta incertidumbre mejor que muchos competidores.
Qué significa esto para el diseño futuro de proteínas
En conjunto, JanusDDG demuestra que es posible combinar las fortalezas de la IA moderna basada en secuencias con las firmes restricciones de la ley física. Tratando a las proteínas como secuencias que pueden leerse como un lenguaje, pero exigiendo que las predicciones cumplan la antisimetría y la transitividad, el modelo produce estimaciones de estabilidad que son a la vez precisas y termodinámicamente consistentes. Para los no especialistas, la conclusión es que nos estamos acercando a herramientas fiables y sin dependencia de estructura que pueden revisar innumerables mutaciones posibles, destacando las más propensas a estabilizar una proteína o señalando cambios riesgosos asociados a enfermedades, todo ello manteniéndose anclado en las reglas de la física en lugar de meros atajos estadísticos.
Cita: Barducci, G., Rossi, I., Codicé, F. et al. JanusDDG: a physics-informed neural network for sequence-based protein stability via two-fronts attention. Commun Biol 9, 494 (2026). https://doi.org/10.1038/s42003-026-09632-9
Palabras clave: estabilidad de proteínas, mutaciones genéticas, diseño de proteínas, aprendizaje automático, termodinámica