Clear Sky Science · es
Análisis personalizado de vías de señalización en tumores gastrointestinales para la estratificación de pacientes y la evaluación de dianas farmacológicas mediante biopsias centrales derivadas clínicamente
Por qué esta investigación importa a los pacientes
Los oncólogos intentan cada vez más adaptar los tratamientos a la biología única del tumor de cada persona. Para los cánceres del sistema digestivo —como los de páncreas, colon, hígado o vías biliares— esto es particularmente urgente, porque son frecuentes, a menudo se diagnostican en estadios avanzados y son difíciles de tratar. Este estudio explora un nuevo método de laboratorio capaz de leer la actividad de muchas proteínas relacionadas con el cáncer a partir de pequeñas muestras de biopsia, con el objetivo de ayudar a los médicos a elegir terapias más precisas para pacientes individuales.
De las listas de ADN a las señales vivas
Hoy, la mayor parte de la atención personalizada contra el cáncer se basa en detectar cambios en el ADN del tumor. Aunque potente, el ADN por sí solo no muestra qué señales dentro de la célula están realmente activadas y conduciendo el crecimiento. Esas señales las transmiten las proteínas, muchas de las cuales pueden dirigirse directamente con fármacos. Los investigadores usaron una técnica de alto rendimiento llamada DigiWest, una versión moderna del clásico Western blot, para medir alrededor de 130–200 proteínas y sus formas activadas a la vez. De forma importante, este método requiere apenas la cantidad de material de una biopsia con aguja, por lo que es adecuado para su uso clínico real.
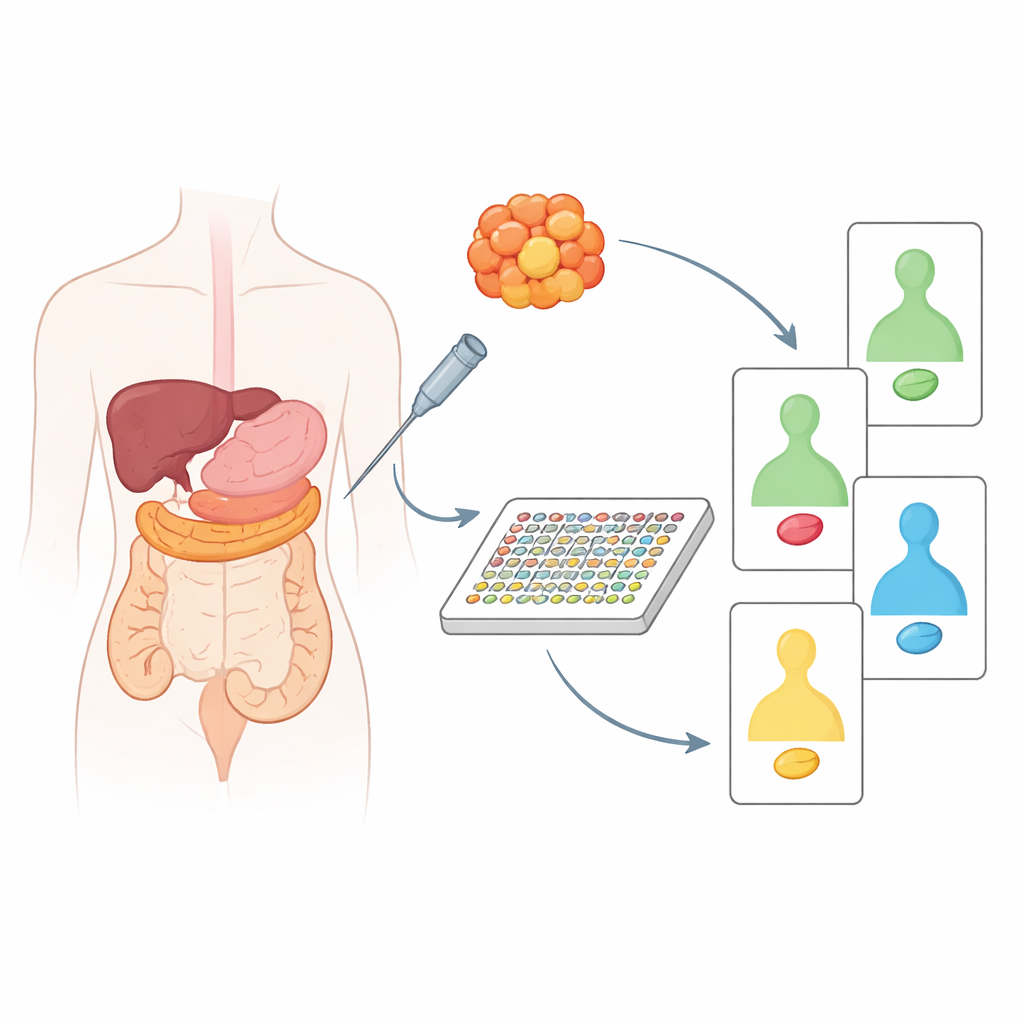
Comparar el tejido tumoral con su tejido sano vecino
El equipo analizó primero tejido archivado de 20 pacientes con cáncer de páncreas o colorrectal, siempre emparejado con tejido no canceroso cercano del mismo paciente. Al comparar los tumores con sus propios tejidos sanos, pudieron ver qué proteínas estaban realmente alteradas por el cáncer y no solo reflejaban diferencias normales entre órganos. Esto reveló contrastes claros en el comportamiento de guardianes y motores del cáncer bien conocidos, como p53, Ras, PTEN y otros. Los tumores pancreáticos, por ejemplo, tendían a mostrar señales potenciadoras del crecimiento y pérdida de proteínas protectoras, mientras que los tumores de colon presentaban su propio patrón distinto de vías alteradas. Cuando los investigadores agruparon las muestras según estos cambios proteicos, pudieron dividir los cánceres de páncreas en dos grupos biológicamente diferentes y detectar diferencias significativas entre cánceres de colon relacionadas con la edad del paciente y la ubicación del tumor en el intestino.
“Códigos de barras” individuales de la actividad de señalización tumoral
Más allá de los promedios de grupo, los científicos construyeron un perfil proteico detallado para cada tumor. Estos perfiles destacaron qué rutas de señalización —como las que implican mTOR, MAPK/Erk, Wnt o factores relacionados con la inmunidad— estaban especialmente activas o inactivadas. Muchas de las proteínas medidas son dianas directas de fármacos existentes, o se sitúan justo aguas abajo de dichas dianas, lo que permitió al equipo inferir qué medicamentos podrían interferir con los principales motores de crecimiento del tumor. En tres cuartas partes de los casos retrospectivos pudieron señalar una o más vías que probablemente impulsaban la progresión tumoral. También identificaron tumores con abundantes marcadores de células inmunitarias, sugiriendo cánceres “calientes” que podrían responder a inmunoterapia, y casos inusuales con firmas sorprendentemente únicas.
Poner el método a trabajar en pacientes reales
Para probar su utilidad en la práctica clínica, los investigadores aplicaron luego DigiWest a biopsias con aguja frescas de 14 pacientes con diversos cánceres gastrointestinales cuyos casos estaban siendo revisados por una Junta Molecular de Tumores. Estos pacientes tenían historiales de enfermedad complejos y, con frecuencia, tratamientos previos. Como no había tejido sano emparejado disponible, los niveles proteicos de cada tumor se compararon con la mediana del grupo para definir qué se consideraba anormalmente alto o bajo. Incluso con este planteamiento más estricto, 12 de los 14 tumores mostraron patrones claros de actividad de vías relevantes para el tratamiento. En dos ejemplos detallados, los datos proteicos confirmaron una amplificación a nivel de ADN del gen FGFR2 en un cáncer de colon y la pérdida de un freno de mTOR en un cáncer de hígado, apoyando con fuerza la consideración por parte de la Junta de fármacos que bloqueen FGFR o mTOR. En general, los hallazgos de DigiWest coincidieron con los impulsores genéticos clave y sugirieron dianas farmacológicas en la mayoría de los casos evaluables.
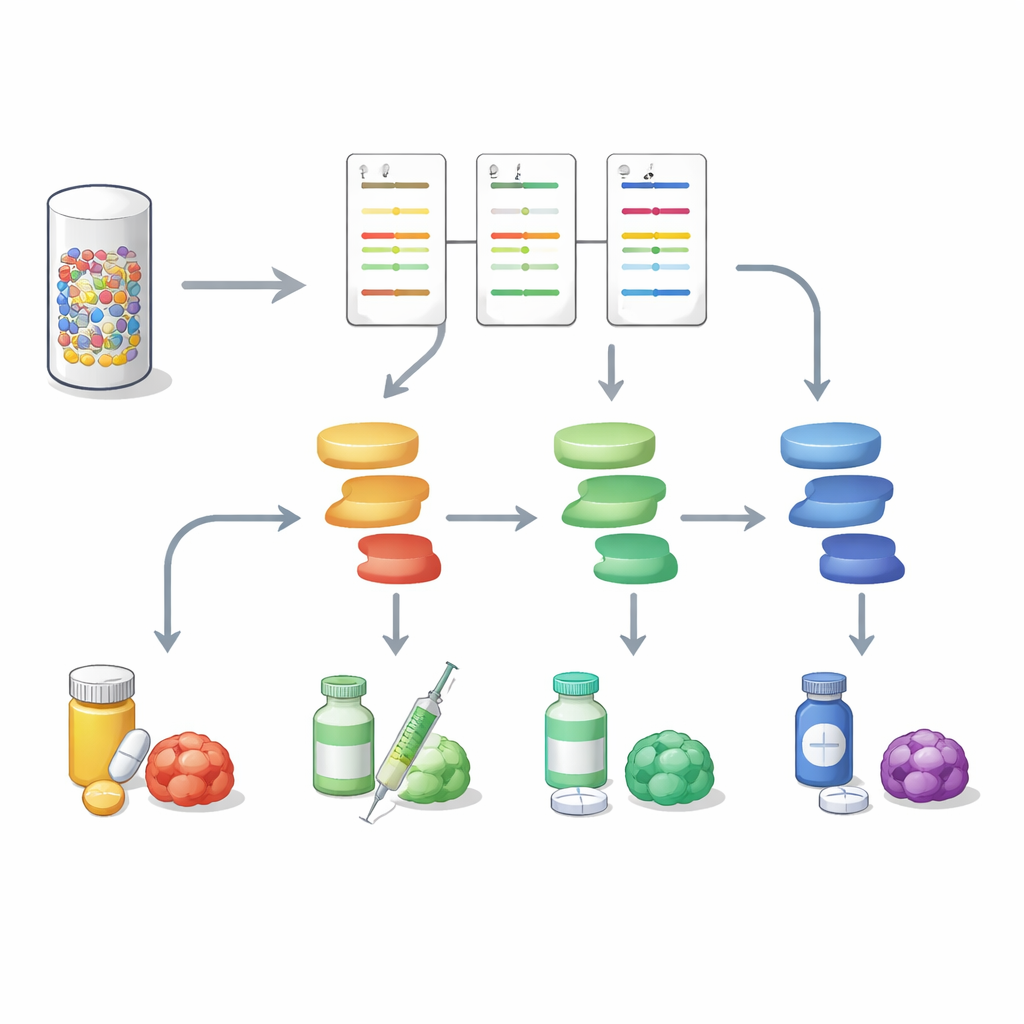
Hacia retratos tumorales más completos
Este trabajo muestra que analizar la señalización proteica en paralelo con la secuenciación del ADN puede ofrecer una imagen más rica y accionable de los tumores gastrointestinales. Al convertir una pequeña biopsia en un mapa de actividad multi‑vía, DigiWest ayuda a distinguir qué interruptores moleculares están realmente encendidos en un cáncer dado y qué fármacos podrían atacarlos mejor, y también puede señalar rutas emergentes de resistencia. Aunque se necesitan estudios más amplios, el enfoque ofrece una forma práctica de incorporar el perfilado proteico de alto contenido a la oncología de precisión cotidiana y avanzar hacia planes de tratamiento adaptados al tumor vivo de cada paciente, no solo a su plano genético.
Cita: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Palabras clave: oncología de precisión, cáncer gastrointestinal, proteómica, perfilado de biopsias, terapia dirigida