Clear Sky Science · es
Inhibición de la corrosión del hierro dúctil en ácido clorhídrico mediante 5-amino-1,3,4-tiadiazol-2-tiol: estudios electroquímicos y computacionales
Por qué importa proteger los metales del día a día
Desde tuberías y válvulas urbanas hasta piezas de automóviles y maquinaria agrícola, muchas estructuras comunes dependen del hierro dúctil, una forma de hierro colado resistente y económica. Sin embargo, cuando estas piezas metálicas entran en contacto con líquidos ácidos, como soluciones de limpieza o ácidos industriales, pueden disolverse lentamente, debilitarse y finalmente fallar. Este estudio explora cómo una pequeña molécula orgánica, llamada 5-ATT, puede formar una película protectora sobre el hierro dúctil en ácido clorhídrico, ralentizando notablemente este daño oculto y ayudando a alargar la vida de infraestructuras críticas.
Cómo el ácido corroe silenciosamente el hierro dúctil
En ambientes agresivos con cloruros y ácido, los iones hidrógeno cargados positivamente y los iones cloruro cargados negativamente atacan átomos metálicos expuestos en la superficie del hierro. Debido a que el hierro dúctil tiene una microestructura especial, con nódulos de grafito incrustados en una matriz metálica, puede desarrollar pequeñas baterías locales que aceleran la corrosión en puntos concretos. Cuando los investigadores colocaron muestras pulidas de hierro dúctil en ácido clorhídrico, midieron una pérdida de masa constante y una alta tasa de corrosión, lo que muestra cuán rápido la superficie puede rugosarse y adelgazar si se deja sin protección.
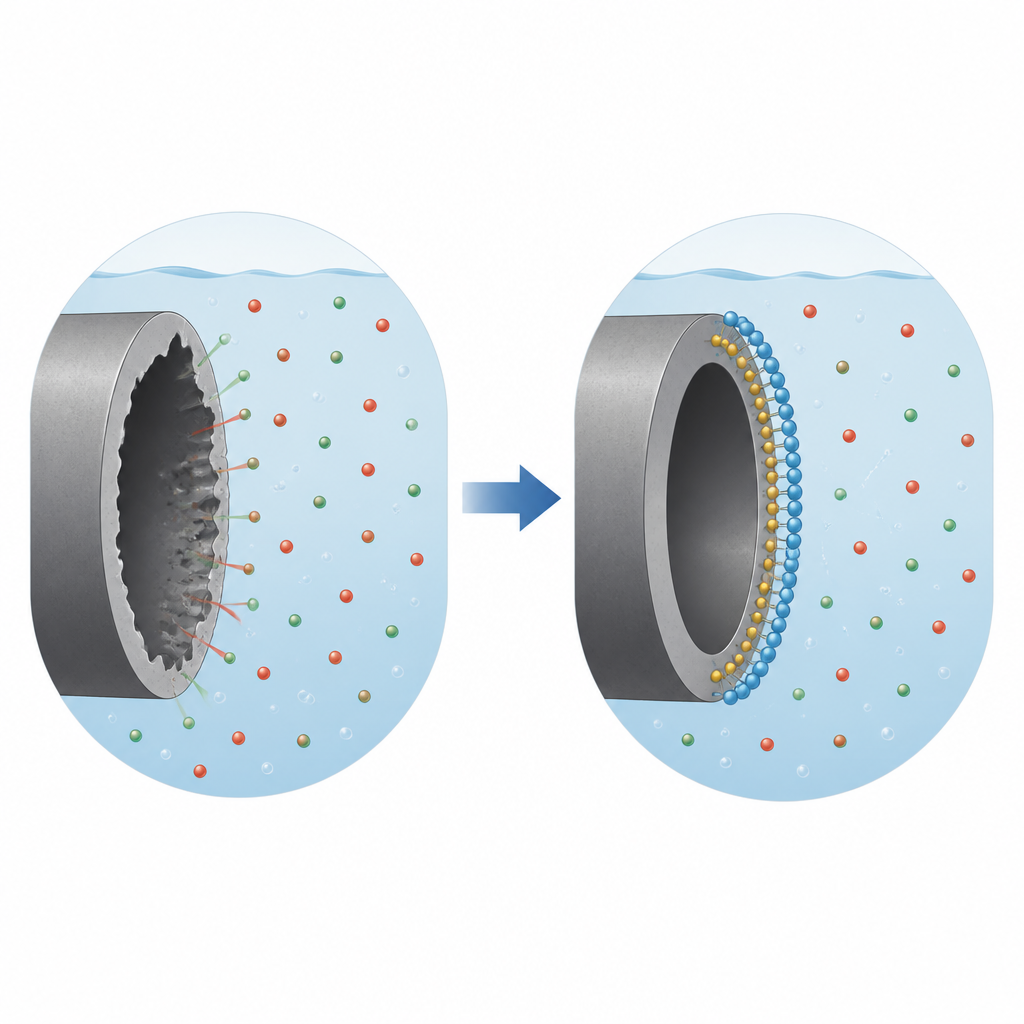
Una pequeña molécula que construye un escudo protector
El equipo probó 5-ATT, un compuesto orgánico rico en átomos de nitrógeno y azufre, como aditivo en la solución ácida. A medida que aumentaron la concentración de 5-ATT, el hierro perdió menos masa y la tasa de corrosión calculada disminuyó notablemente, alcanzando una protección de alrededor del 70–80 % en las dosis más elevadas. Las pruebas electroquímicas, que registran pequeñas corrientes eléctricas ligadas a la disolución del metal, mostraron que la corriente de corrosión cayó y la resistencia a la transferencia de carga aumentó al añadir más 5-ATT. En conjunto, estos resultados indican que las moléculas de 5-ATT se extienden por la superficie del hierro y actúan como un delgado escudo que bloquea el acceso de iones agresivos al metal.
Sondeando cómo se forma y se mantiene el escudo
Para ver este escudo directamente, los investigadores examinaron las superficies de hierro con y sin 5-ATT mediante microscopía electrónica. En el ácido puro, el metal aparecía áspero, agrietado y marcado por ataques locales. Cuando estaba presente 5-ATT, la superficie se mostró más lisa y uniforme, con menos defectos visibles. El análisis químico de la superficie detectó carbono, nitrógeno y azufre procedentes del inhibidor, confirmando que las moléculas de 5-ATT se adherían efectivamente al metal. Al analizar qué modelos matemáticos ajustaban mejor la cobertura de 5-ATT, el equipo concluyó que las moléculas no forman una capa única perfectamente ordenada. En cambio, ocupan múltiples sitios, interaccionan entre sí y desplazan agua de forma más compleja y realista.
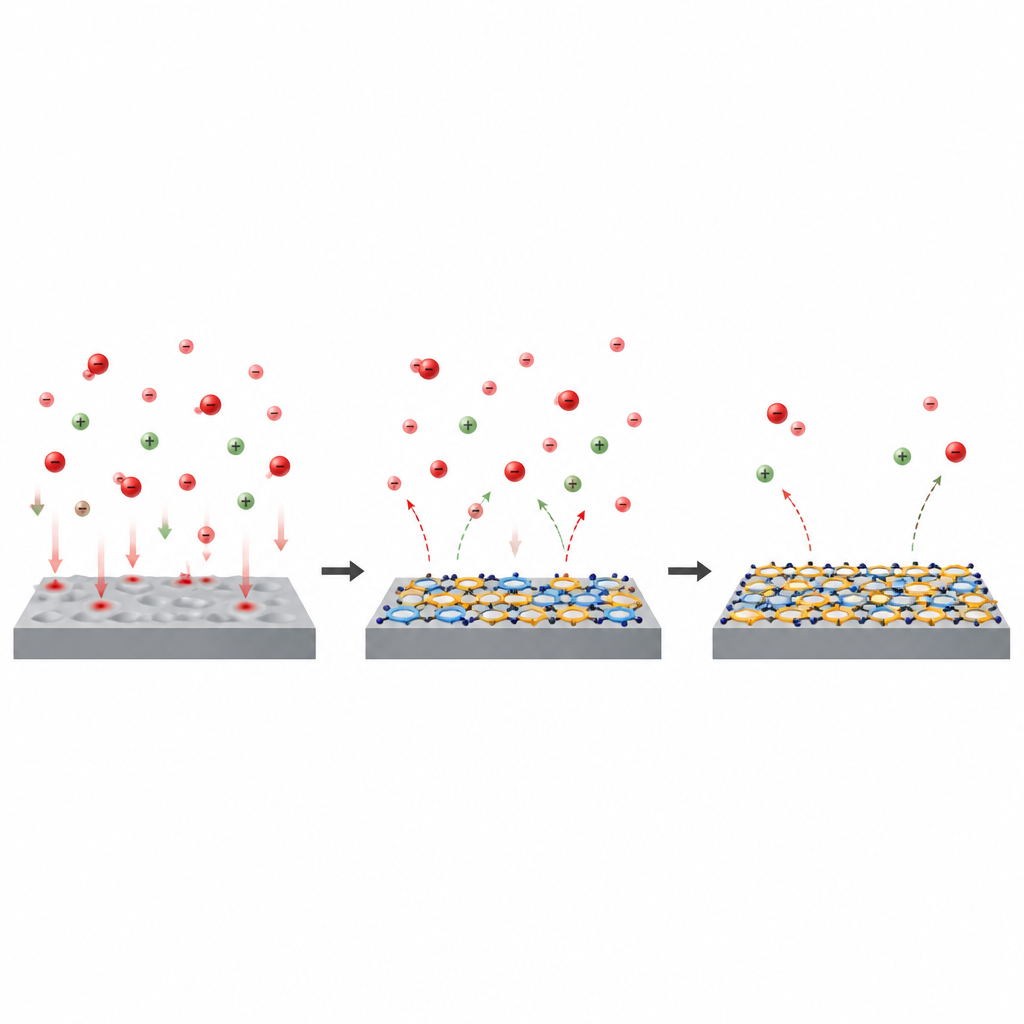
Mirando dentro de la molécula con herramientas digitales
Además de las mediciones de laboratorio, el estudio utilizó cálculos de química cuántica y simulaciones por ordenador para entender por qué 5-ATT funciona tan bien. La molécula puede existir en dos formas estrechamente relacionadas, llamadas tiol y tiona, que difieren en la disposición de un átomo de hidrógeno y un doble enlace. Los cálculos mostraron que ambas formas tienen regiones de alta densidad electrónica en sus átomos de azufre y nitrógeno, lo que hace que estos puntos sean ideales para enlazarse con átomos de hierro. Simulaciones de la molécula sobre una superficie de hierro en un entorno acuoso y ácido revelaron que 5-ATT tiende a adoptar una postura casi plana, maximizando el contacto con el metal y con iones cercanos. En agua y ácido, la forma tiol en particular interactúa fuertemente, ayudando a estabilizar una película protectora compacta que desplaza a las especies corrosivas.
Qué significa esto para la protección de metales en el mundo real
En pocas palabras, este trabajo demuestra que una molécula pequeña cuidadosamente escogida puede actuar como un “impermeable” autoensamblado para el hierro dúctil en ambientes ácidos. 5-ATT se adsorbe de forma espontánea sobre el metal, utilizando tanto atracción física como enlaces químicos para construir una barrera ajustada y con múltiples puntos de contacto. Esta barrera ralentiza tanto la pérdida de átomos de hierro como la reacción que libera gas hidrógeno, reduciendo la tasa de corrosión hasta en aproximadamente cuatro quintas partes bajo las condiciones probadas. Al vincular medidas experimentales detalladas con modelos computacionales de cómo 5-ATT se fija al hierro a escala atómica, el estudio ofrece una imagen clara de cómo estos inhibidores pueden diseñarse y mejorarse para proteger tuberías, accesorios y otros componentes a base de hierro que funcionan en entornos ácidos.
Cita: Helmy, M., El-Zomrawy, A.A., Mogoda, A.S. et al. Corrosion inhibition of ductile iron in hydrochloric acid using 5-amino-1,3,4-thiadiazole-2-thiol: electrochemical and computational studies. Sci Rep 16, 14740 (2026). https://doi.org/10.1038/s41598-026-51250-2
Palabras clave: corrosión, hierro dúctil, ácido clorhídrico, inhibidor de corrosión, película superficial