Clear Sky Science · es
Investigación numérica del correntaje acústico inducido por ultrasonidos y la tensión por corte para la manipulación de coágulos sanguíneos
Por qué importa romper coágulos sin fármacos
Los coágulos en venas y vasos cerebrales pueden bloquear la circulación y causar ictus, infarto de miocardio o trombos pulmonares peligrosos. Los tratamientos actuales se basan principalmente en fármacos anticoagulantes o trombolíticos, que pueden salvar vidas pero también aumentan el riesgo de hemorragias graves y no son adecuados para todos los pacientes. Este estudio explora una alternativa no farmacológica y no invasiva: usar ultrasonidos afinados para agitar el fluido alrededor de un coágulo con suficiente intensidad como para que el propio coágulo comience a fragmentarse.
Usar el sonido para empujar un bloqueo oculto
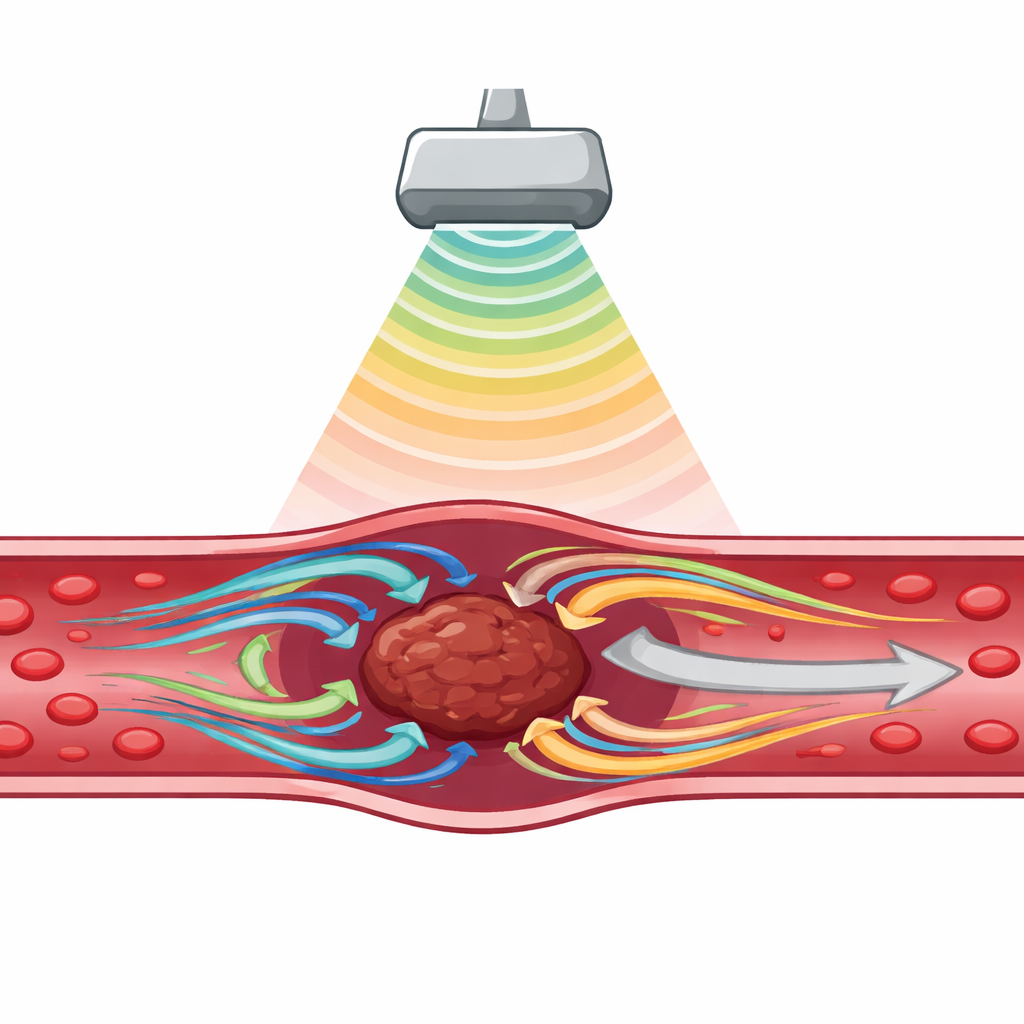
Los investigadores se centraron en un efecto sutil llamado correntaje acústico. Cuando un haz de ultrasonidos atraviesa un fluido, no solo transmite ondas; también puede generar un flujo lento pero constante, como un suave viento submarino. Cerca de una obstrucción como un coágulo, ese flujo puede formar pequeños vórtices que arrastran la superficie del coágulo y generan una fuerza lateral conocida como tensión por corte. Si esa tensión supera la resistencia mecánica del coágulo, las fibras internas pueden romperse y la masa comienza a fragmentarse. En lugar de añadir fármacos para debilitar el coágulo, el equipo preguntó si el correntaje por sí solo, creado por ajustes de ultrasonido realistas, podría alcanzar esos niveles de tensión.
Construyendo un vaso sanguíneo digital
Para responder, los autores construyeron un modelo informático detallado de un vaso sanguíneo con un coágulo en su interior, usando el software de simulación COMSOL Multiphysics. Representaron el vaso como un tubo bidimensional y el coágulo como una región elíptica con comportamiento viscoso y denso similar a un fluido espeso. Una fuente de ultrasonido, modelada como un transductor recto situado por encima del coágulo, emitía ondas sonoras continuas hacia el vaso. Acoplando dos conjuntos de ecuaciones —una que describe la propagación de ondas sonoras y otra que describe el flujo de fluidos— calcularon cómo el campo ultrasónico generaba correntaje alrededor del coágulo y cuánta tensión por corte aparecía en su superficie en diferentes condiciones.
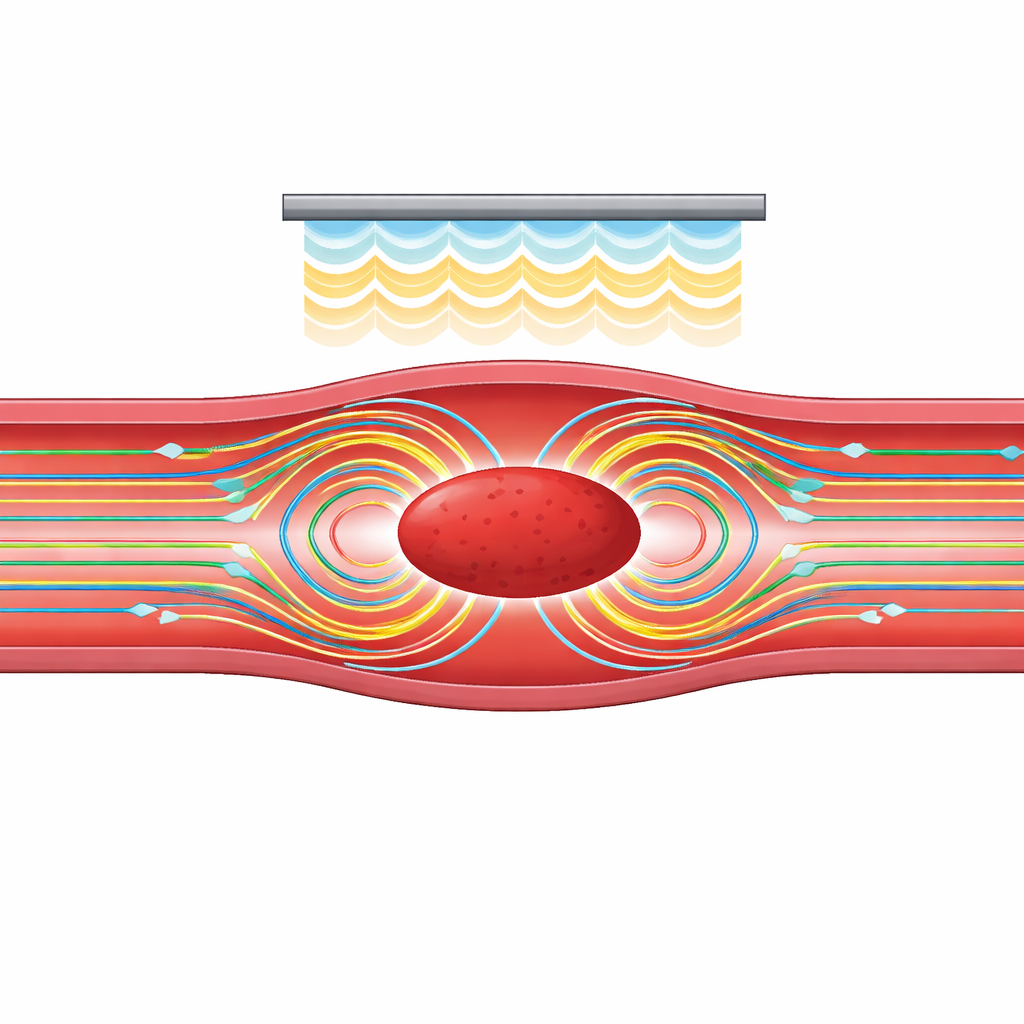
Encontrar los ajustes sonoros adecuados
El equipo varió sistemáticamente tres factores clave: la posición del coágulo respecto al transductor, la frecuencia del ultrasonido y la intensidad (presión) de las ondas sonoras. Encontraron que el correntaje y la tensión por corte cambiaban de forma compleja y no lineal a medida que el coágulo se desplazaba a lo largo del vaso, una señal de los patrones de ondas estacionarias formados por el sonido incidente y el reflejado. En ciertas posiciones se formaban vórtices fuertes a ambos lados del coágulo y se generaban tensiones intensas; en otras, el flujo era mucho más débil. La frecuencia también importó. Frecuencias muy bajas penetraban bien pero podían provocar efectos no deseados como actividad de burbujas incontrolada, mientras que frecuencias muy altas se absorbían rápidamente y se convertían principalmente en calor. Alrededor de 2 MHz, el modelo predijo un punto óptimo en el que el correntaje permanecía intenso sin una absorción excesiva, lo que lo hace especialmente atractivo para la terapia.
Cuánto debe empujar el sonido
Aumentando gradualmente la presión acústica, los investigadores mostraron que la tensión por corte en la superficie del coágulo aumentaba de forma sostenida y luego comenzaba a estabilizarse cuando la resistencia viscosa del fluido equilibraba la fuerza impulsora. Bajo condiciones optimizadas —aproximadamente 2 MHz y 2 MPa de presión acústica con el coágulo en una ubicación favorable— la tensión por corte calculada alcanzó un pico de aproximadamente 10,9 pascales, más del doble de un umbral estimado de 4,1 pascales necesario para empezar a romper la red interna del coágulo. El modelo también exploró un escenario más realista con una pared vascular más gruesa, como podría ocurrir en enfermedad. En ese caso, más sonido se perdía antes de alcanzar el coágulo, y la tensión inicial cayó hasta unos 2,7 pascales. Aumentar moderadamente la presión podría elevarla hasta unos 3,0 pascales, pero aún por debajo del umbral de ruptura, lo que subraya cómo los tejidos entre la piel y el vaso pueden atenuar el efecto.
Siguientes pasos hacia un tratamiento de coágulos más seguro
En conjunto, las simulaciones sugieren que el correntaje inducido por ultrasonidos puede, en principio, generar suficiente esfuerzo mecánico para fragmentar coágulos sin usar fármacos trombolíticos, siempre que los ajustes de sonido y la geometría sean favorables. Al mismo tiempo, el trabajo destaca salvedades importantes: el modelo actual emplea estructuras simplificadas de vaso y coágulo, asume ausencia de flujo sanguíneo de fondo e incluso sitúa el transductor dentro del vaso en lugar de sobre la piel. Los autores sostienen que se necesitan modelos tridimensionales más realistas, paredes vasculares deformables, sangre en movimiento y pruebas experimentales. Aun así, sus resultados delinean rangos prometedores de frecuencia, presión y posicionamiento, y señalan al correntaje acústico como un posible elemento básico para futuras terapias por ultrasonidos más seguras contra coágulos.
Cita: Hisham, A., Hassan, M.A. & Wahba, A.A. Numerical investigation of ultrasound-induced acoustic streaming and shear stress for blood clot manipulation. Sci Rep 16, 12891 (2026). https://doi.org/10.1038/s41598-026-44521-5
Palabras clave: terapia de coágulos con ultrasonidos, corriente acústica, trombo sanguíneo, tensión por corte, modelado computacional