Clear Sky Science · es
Efecto protector del hierro frente a las lesiones inducidas por cadmio en el testículo de la rata mediante la regulación a la baja de NQO1/Nrf2 y NF-κB
Por qué importa la presencia de metales en el agua para la salud masculina
Metales pesados como el cadmio pueden filtrarse al agua potable por contaminación industrial y acumularse en el organismo con el tiempo. Un órgano particularmente sensible es el testículo, que produce tanto espermatozoides como la hormona testosterona. Este estudio en ratas plantea una pregunta práctica con implicaciones reales: cuando hay cadmio presente, ¿puede el hierro —otro metal común en la dieta y en el agua—mitigar el daño a la salud reproductiva masculina?

Qué se propusieron probar los investigadores
Los científicos se centraron en cómo el cadmio daña los testículos y si el hierro puede atenuar ese efecto. Se sabe que el cadmio desencadena estrés químico dentro de las células y altera los niveles hormonales, mientras que el hierro puede competir con el cadmio por rutas de entrada al organismo a través de transportadores comunes en el intestino. Para explorar esto, el equipo dividió a ratas jóvenes macho en cuatro grupos durante cuatro semanas: un grupo recibió agua limpia, otro agua contaminada con cadmio, un tercero solo hierro y un cuarto bebió agua con ambos metales. Tras la exposición, los investigadores midieron marcadores sanguíneos estándar, hormonas reproductivas y la actividad de interruptores protectores e inflamatorios clave dentro de las células testiculares. También examinaron cortes finos de tejido testicular al microscopio para ver cómo había cambiado la estructura.
Qué ocurrió con las hormonas y las defensas celulares
Las ratas expuestas solo al cadmio mostraron signos claros de alteración reproductiva. Los niveles sanguíneos de hormona luteinizante (LH) y hormona estimulante del folículo (FSH), señales del cerebro que impulsan la función testicular, aumentaron notablemente, mientras que la testosterona disminuyó. La estradiol, una forma de estrógeno, se incrementó, lo que indica un desequilibrio hormonal que puede afectar la fertilidad. Al mismo tiempo, la actividad de la catalasa, una enzima antioxidante clave, se redujo, señalando una defensa debilitada frente a moléculas reactivas dañinas. Cuando se administró hierro por sí solo, alteró algunas de estas medidas de forma distinta y el hierro a la dosis elegida pudo causar cierto estrés leve. Pero cuando se dieron hierro y cadmio juntos, varios de los cambios inducidos por el cadmio se atenuaron: la actividad antioxidante en sangre se restauró parcialmente, los niveles de estradiol se acercaron a la normalidad y algunos marcadores de estrés se comportaron de forma menos intensa.
Cómo el hierro modifica las señales dentro de las células testiculares
El equipo analizó más a fondo los interruptores genéticos que controlan cómo responden las células a insultos tóxicos. El cadmio por sí solo aumentó la actividad de Nrf2 y NF-κB, dos controladores centrales que activan genes implicados en las defensas antioxidantes y la inflamación. También incrementó los niveles del ARNm de NQO1, una enzima protectora regulada por Nrf2. Sorprendentemente, otro gen relacionado con el estrés, HO-1, se redujo en lugar de aumentar. Cuando el hierro estuvo presente junto con el cadmio, estos picos inducidos por cadmio en Nrf2, NF-κB y NQO1 se redujeron, lo que sugiere que el hierro reprimió tanto la señalización oxidativa como la inflamatoria. El hierro también modificó genes vinculados al manejo del hierro y la producción de glóbulos rojos, como el receptor de transferrina y la eritropoyetina, mostrando que el equilibrio metálico en el organismo está estrechamente ligado a cómo las células afrontan exposiciones tóxicas.
Cómo se veía el tejido testicular
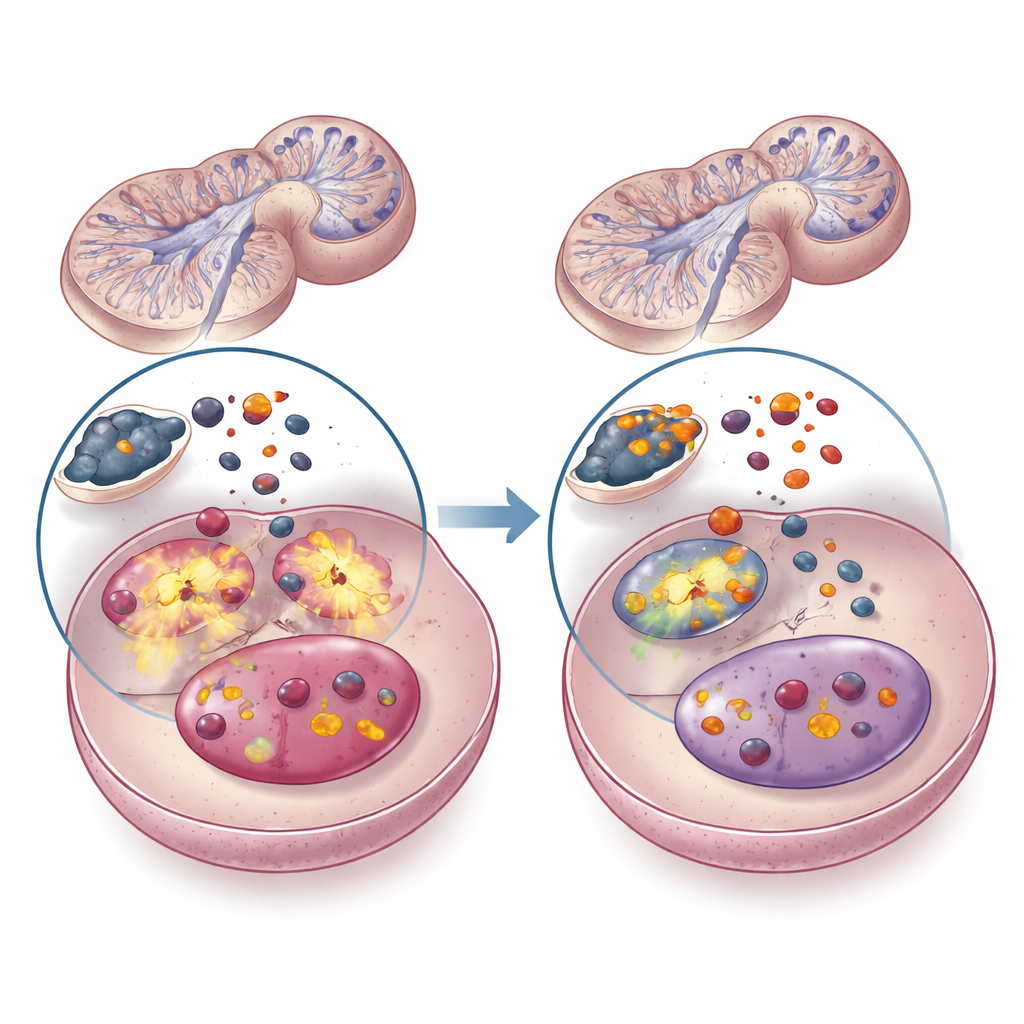
Las imágenes microscópicas proporcionaron una confirmación visual de estos cambios moleculares. En las ratas control sanas, los túbulos seminíferos —las pequeñas estructuras donde se producen los espermatozoides— eran redondeados, ordenados y estaban llenos de células espermatogénicas en desarrollo, con abundantes células de Leydig productoras de hormonas entre ellos. En las ratas expuestas al cadmio, muchos túbulos estaban distorsionados y obstruidos, las capas celulares presentaban vacuolización y adelgazamiento, y las células de Leydig se encontraban reducidas, todos signos de producción de esperma y secreción hormonal deterioradas. Las ratas tratadas solo con hierro también mostraron algunos cambios degenerativos. De forma llamativa, en las ratas que recibieron cadmio y hierro conjuntamente, la mayoría de los túbulos recuperaron un contorno más regular, con membranas basales más delgadas y una serie más completa de células espermatogénicas, lo que indica que la coexposición al hierro ayudó a preservar una estructura testicular cercana a la normalidad en comparación con el cadmio solo.
Qué significa esto para la protección de la fertilidad masculina
En conjunto, los hallazgos sugieren que el hierro puede proteger en parte al sistema reproductor masculino del daño por cadmio en las condiciones ensayadas. Mientras que el cadmio por sí solo alteró las hormonas, debilitó las defensas antioxidantes, activó vías de estrés e inflamación y lesionó visiblemente el tejido testicular, la adición de hierro redujo parte de esta alteración, especialmente a nivel de la señalización celular y la estructura tisular. Sin embargo, el hierro no corrigió todos los cambios hormonales y puede ser perjudicial en determinadas dosis, por lo que no es un antídoto simple. Para quienes no son especialistas, la conclusión principal es que el equilibrio de metales que ingerimos importa: la exposición a un metal tóxico como el cadmio puede verse modulada por metales esenciales como el hierro, que podrían ofrecer cierta protección a órganos sensibles como los testículos. Serán necesarios más estudios para entender niveles seguros y para traducir estos hallazgos en ratas a la salud humana.
Cita: Ogunbiyi, O.J., Okolie, N.P., Obi, F.O. et al. Protective effect of iron against cadmium-induced lesions in rat testis via downregulation of NQO1/Nrf2 and NF-κB. Sci Rep 16, 13613 (2026). https://doi.org/10.1038/s41598-026-43876-z
Palabras clave: toxicidad por cadmio, suplementación con hierro, fertilidad masculina, estrés oxidativo, alteración endocrina