Clear Sky Science · es
ACSL4 media la ferroptosis para promover la progresión de la nefropatía por inmunoglobulina A: análisis scRNA-seq
Por qué importa este estudio renal
La enfermedad renal crónica puede progresar silenciosamente durante años antes de que aparezcan los síntomas, llevando en última instancia a algunos pacientes a diálisis o trasplante renal. Uno de los culpables más comunes es la nefropatía por inmunoglobulina A (IgAN), un trastorno autoinmune que cicatriza los filtros del riñón. Este estudio examina el problema a nivel microscópico—hasta las células individuales—para plantear una cuestión urgente: ¿está un tipo de muerte celular recién reconocido contribuyendo a que la IgAN avance hacia la insuficiencia renal, y podría ofrecer un nuevo objetivo para el tratamiento?
Una mirada más cercana a una enfermedad renal común
La IgAN es una afección renal extendida en la que proteínas inmunitarias se acumulan en los pequeños filtros que limpian la sangre. Con el tiempo, esta acumulación puede inflamar y dañar el tejido renal, y hasta un 40 % de los pacientes puede llegar finalmente a enfermedad renal terminal. Aunque los investigadores saben que la genética, los anticuerpos anormales y los desencadenantes ambientales están implicados, los tipos celulares exactos y los procesos internos que empujan a la IgAN del daño inicial a la cicatrización persistente han permanecido poco claros. Entender qué células fallan y cómo es esencial para diseñar terapias que puedan ralentizar o detener la progresión de la enfermedad.
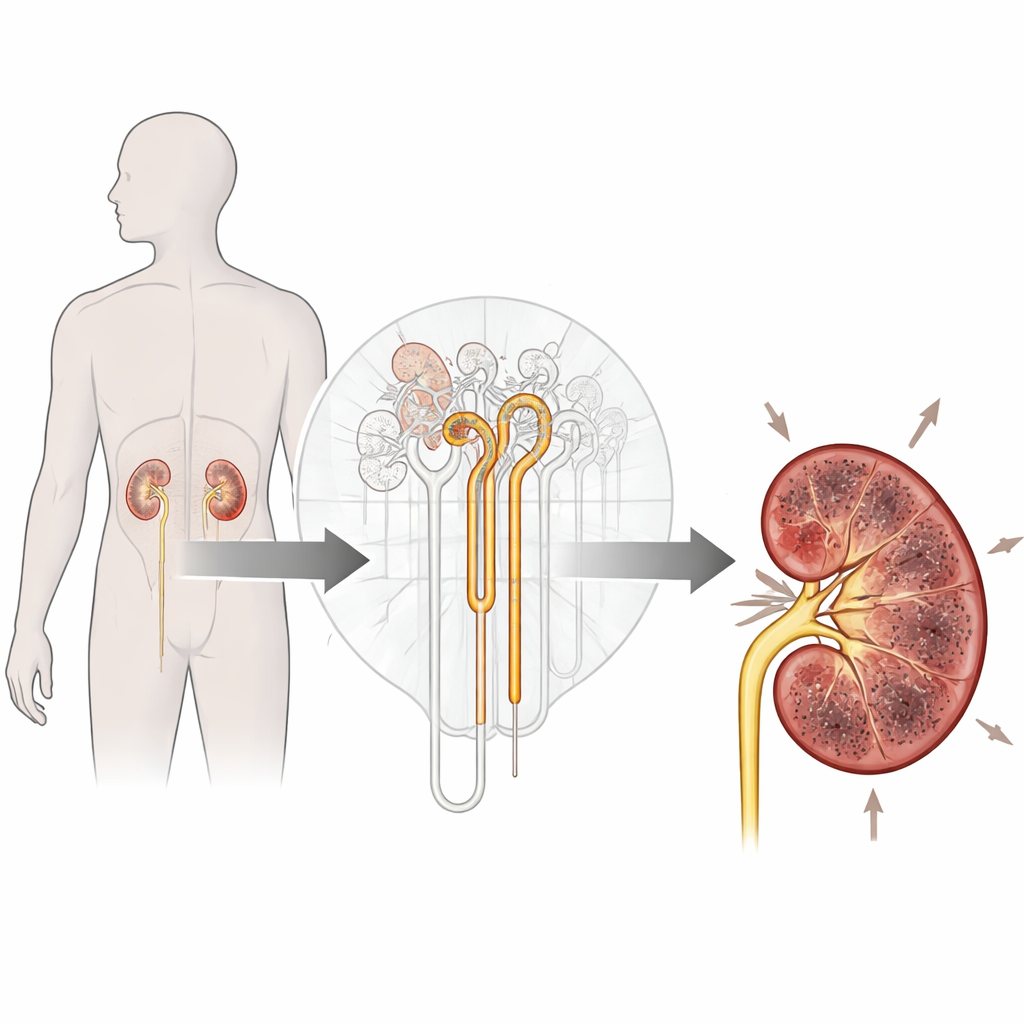
Un nuevo tipo de muerte celular en el centro de atención
En años recientes, los científicos han descubierto un tipo de muerte celular distinto llamado ferroptosis. A diferencia de formas más conocidas como la apoptosis, la ferroptosis depende del hierro y de la degradación tóxica de los lípidos en las membranas celulares. Cuando este proceso se acelera, puede hacer que las células se rompan y liberen moléculas irritantes en el tejido circundante, alimentando la inflamación. Un actor clave en este proceso es una enzima llamada ACSL4, que ayuda a incorporar ciertos lípidos en las membranas celulares, haciéndolas especialmente vulnerables al daño inducido por el hierro. Dado que la ferroptosis se ha relacionado con lesión renal en otras condiciones, los autores se preguntaron si la ferroptosis impulsada por ACSL4 también podría estar implicada en el empeoramiento de la IgAN.
Acercándose a un tipo celular renal específico
Para responder a esto, el equipo analizó un conjunto de datos público de secuenciación de ARN unicelular de riñones de pacientes con IgAN y de un control sano. Esta tecnología lee qué genes están activos en miles de células individuales, lo que permite a los investigadores clasificarlas en tipos distintos. Los autores identificaron doce poblaciones celulares principales, incluidas células de vasos sanguíneos, células inmunitarias y distintos túbulos que afinan la composición de la orina. Un tipo celular destacó: las células del asa de Henle, un segmento clave que ayuda a concentrar la orina y a equilibrar las sales. Estas células eran más abundantes en los riñones con IgAN que en la muestra sana, y mostraron un aumento notable de la actividad de ACSL4, mientras que los genes protectores contra la ferroptosis estaban reducidos, apuntando hacia una fuerte inclinación a favor de la muerte celular ferroptótica.
Cómo las células estresadas pueden comunicarse con sus vecinas
El estudio hizo más que catalogar qué genes estaban activados. Usando herramientas computacionales, los investigadores modelaron cómo las células del asa de Henle podrían comunicarse con las células circundantes a través de moléculas señalizadoras. Encontraron que las células del asa con alta expresión de ACSL4 mostraban interacciones predichas más fuertes con células vasculares, células de soporte en los filtros renales y túbulos cercanos. Muchas de estas señales implicaban al mensajero inflamatorio interleucina-6. Esto sugiere que una vez que las células del asa se inclinan hacia la ferroptosis, pueden no morir en silencio; en cambio, podrían enviar señales de alarma que amplifiquen la inflamación y el estrés oxidativo en el tejido renal, fomentando más daño y cicatrización.
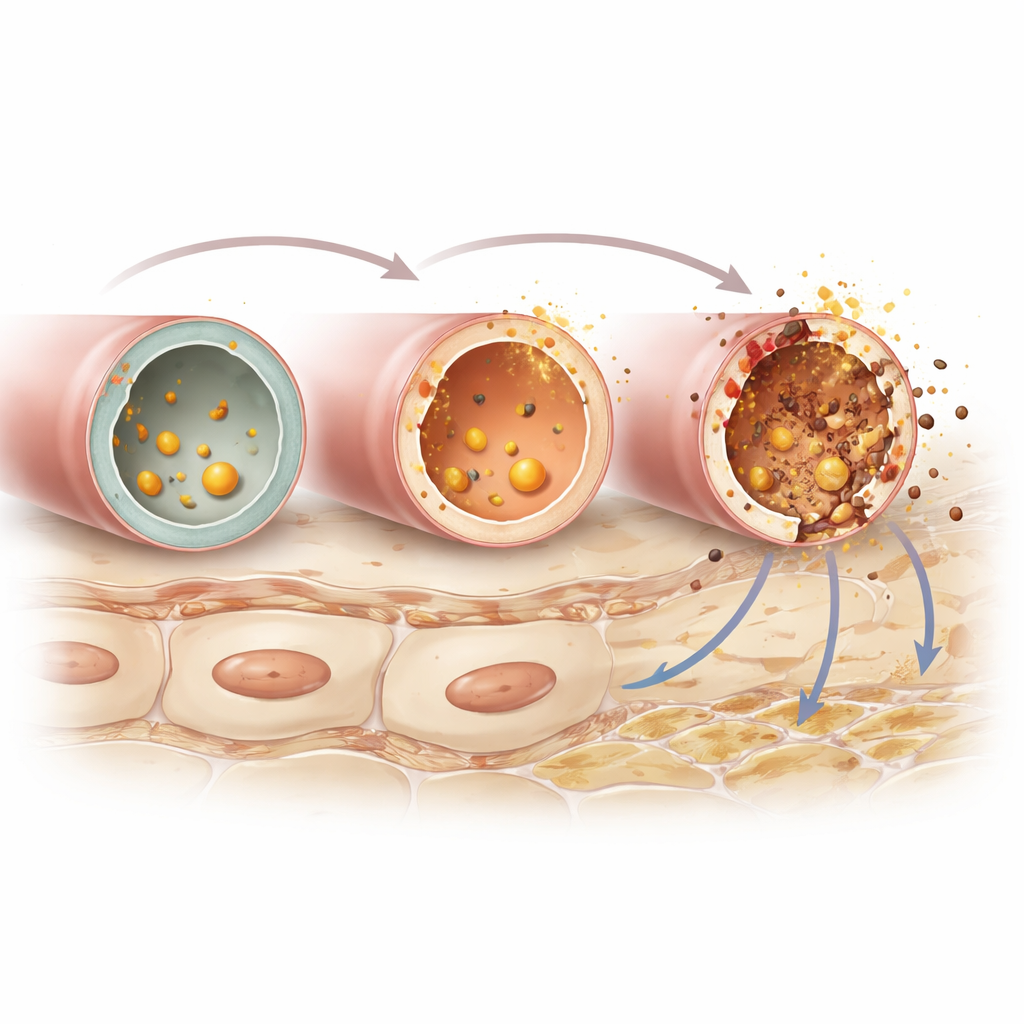
Evidencia a partir de tejido renal real
Para respaldar sus hallazgos computacionales, los autores examinaron tejido renal de pacientes con IgAN y de personas sin la enfermedad. Las tinciones estándar mostraron signos clásicos de IgAN: sobrecrecimiento de ciertas células del filtro, acumulación de células inflamatorias entre estructuras y aumento de fibras de colágeno que señalan cicatrización. Cuando marcaron ACSL4 específicamente, vieron que las células del asa de Henle en riñones sanos tenían muy poca enzima, mientras que las de riñones con IgAN se iluminaban intensamente, confirmando el fuerte aumento sugerido por los datos de actividad génica. En conjunto, estas imágenes respaldan la idea de que las células del asa se expanden en número y se vuelven más propensas al daño por ferroptosis a medida que progresa la IgAN.
Qué significa esto para tratamientos futuros
En conjunto, el estudio propone que en la IgAN, las células del asa de Henle cambian a un estado de alta expresión de ACSL4 y mayor propensión a la ferroptosis que tanto sufre daño como desencadena señales inflamatorias como la interleucina-6. Esta combinación podría acelerar la cicatrización y la pérdida de función renal. Si bien el trabajo se apoya en gran medida en análisis computacionales y tinciones de tejido—y aún necesita experimentos de seguimiento en células y animales—pone de relieve a ACSL4 y a la ferroptosis como dianas prometedoras. Si investigaciones futuras confirman que bloquear esta vía puede proteger las células del asa y calmar la señalización dañina, podría abrir una nueva vía hacia terapias que ayuden a los pacientes con IgAN a mantener sus riñones más sanos durante más tiempo.
Cita: Shao, N., Tan, K., Chen, P. et al. ACSL4 mediates ferroptosis to promote immunoglobulin A nephropathy progression: scRNA-seq analysis. Sci Rep 16, 12543 (2026). https://doi.org/10.1038/s41598-026-43023-8
Palabras clave: nefropatía por IgA, ferroptosis, ACSL4, células del túbulo renal, secuenciación de ARN unicelular