Clear Sky Science · es
Investigación sobre las características metabólicas de la esclerosis múltiple
Por qué el intestino importa en una enfermedad cerebral
La esclerosis múltiple (EM) suele concebirse como una enfermedad que ataca el cerebro y la médula espinal, sin embargo este estudio sugiere que pistas importantes pueden esconderse mucho más al sur: en nuestro intestino. Al analizar con detalle los restos químicos en muestras de heces, los investigadores exploraron cómo las sustancias relacionadas con el intestino difieren entre personas con EM y voluntarios sanos. Estas pequeñas moléculas, producidas por los alimentos, nuestro propio organismo y trillones de microbios intestinales, podrían ayudar a explicar por qué el sistema inmunitario falla en la EM y, en última instancia, orientar tratamientos más suaves y precisos.
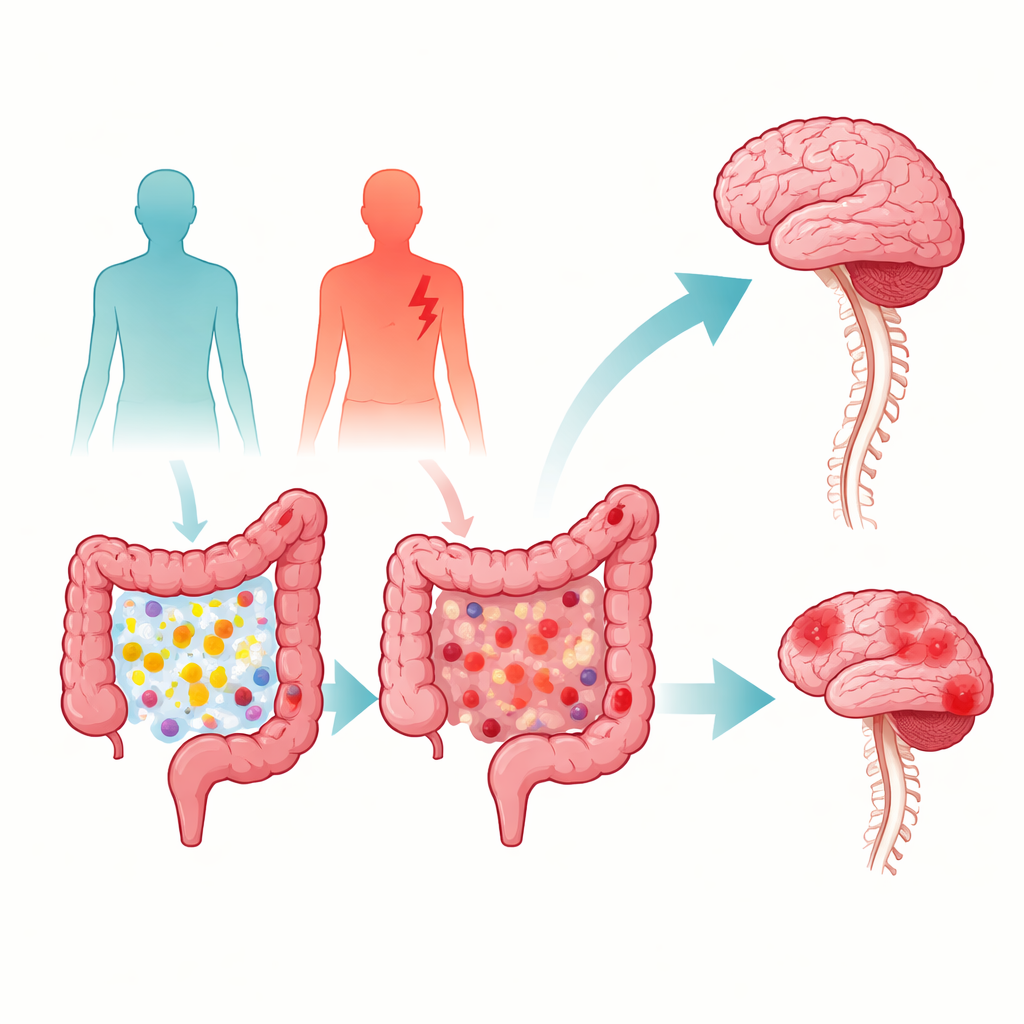
Mirando la enfermedad a través de las heces
El equipo recogió muestras fecales de 37 adultos con EM, en su mayoría con la forma remitente‑recurrente, y 30 adultos similares sin la enfermedad, todos del norte de China. Las heces son una ventana atractiva hacia la salud: son fáciles de obtener, no invasivas y reflejan directamente la actividad de los microbios intestinales y la digestión del huésped. Usando una tecnología muy sensible que separa y pesa miles de pequeñas moléculas a la vez, los investigadores construyeron huellas químicas detalladas para cada muestra. Luego emplearon estadística avanzada para comprobar la estabilidad de sus mediciones y ver si los patrones metabólicos generales podían distinguir a pacientes con EM de individuos sanos.
Miles de moléculas, docenas que destacan
De 552 moléculas identificadas, 56 mostraron diferencias claras entre el grupo con EM y el grupo sano. Solo ocho de ellas estaban elevadas en la EM, mientras que la gran mayoría—48—estaban reducidas. Muchas de las moléculas alteradas pertenecían a dos grandes familias: aminoácidos, los bloques constructores de las proteínas, y ácidos grasos, que incluyen importantes fuentes de energía y lípidos señalizadores. Los ácidos grasos de cadena corta, producidos cuando las bacterias intestinales digieren fibra, estaban notablemente disminuidos. También lo estaban los aminoácidos ramificados y ciertas grasas insaturadas que a menudo se asocian con funciones antiinflamatorias o protectoras. Estos cambios generales dibujan el panorama de un entorno intestinal en la EM que es menos rico químicamente y potencialmente menos capaz de apoyar respuestas inmunitarias equilibradas.
Conectando metabolitos con vías corporales
Los investigadores se preguntaron entonces en qué parte de la red de reacciones químicas del cuerpo encajaban estas moléculas cambiadas. Mapearon los 56 metabolitos clave en vías biológicas conocidas y encontraron 20 que parecían perturbadas, con siete destacadas. Estas implicaban cómo el cuerpo digiere y absorbe proteínas, sintetiza nuevos aminoácidos, los activa para la producción proteica y procesa la niacina y moléculas afines importantes para la energía celular. También observaron cambios en vías relacionadas con transportadores de membrana que desplazan sustancias a través de barreras, en un sistema mayor de detección del crecimiento y la energía llamado mTOR, y en el metabolismo central del carbono, que está en el núcleo de cómo las células queman combustible y construyen componentes. En conjunto, estos cambios sugieren que la EM puede implicar un reajuste generalizado de cómo las células usan la energía y ensamblan proteínas, influido en parte por lo que sucede en el intestino.
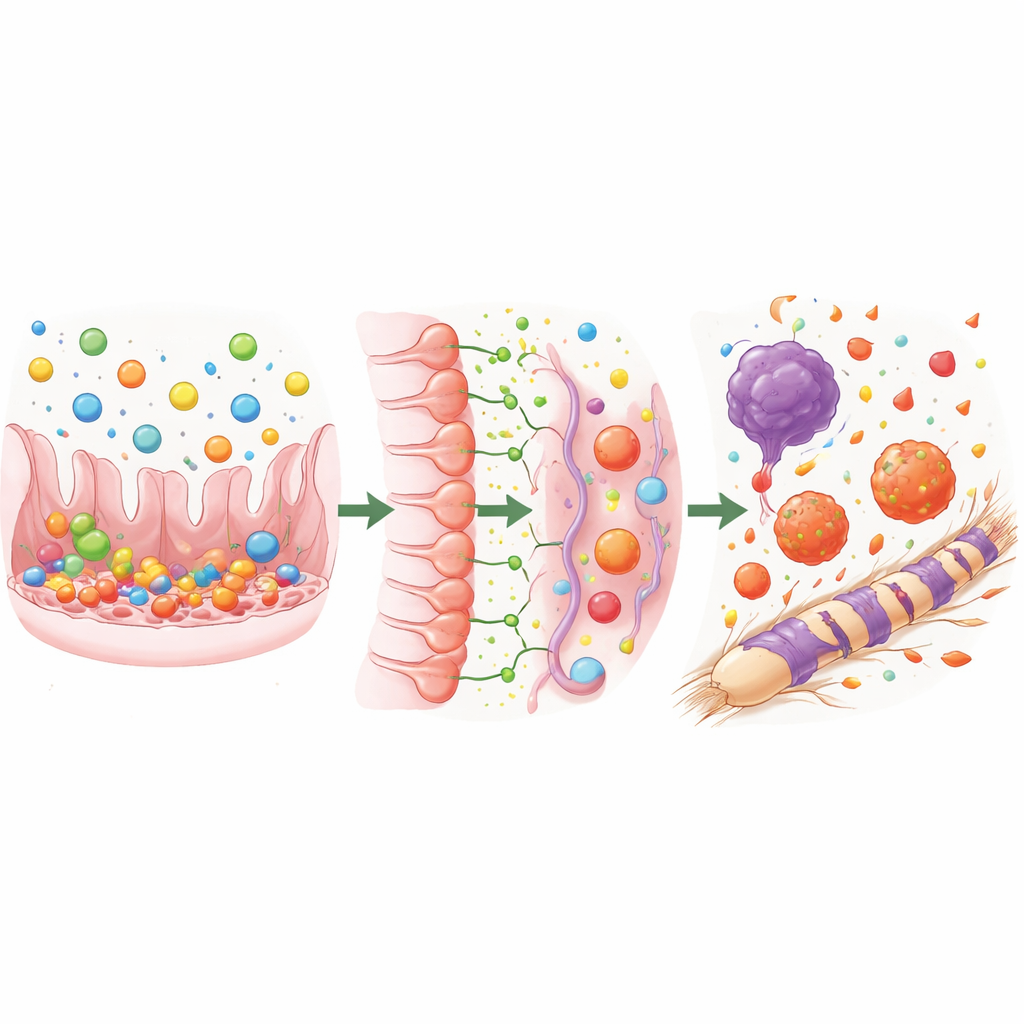
De moléculas ausentes a una inmunidad desajustada
¿Cómo podrían afectar estas moléculas ausentes o alteradas a una persona con EM? Los ácidos grasos de cadena corta producidos por bacterias intestinales normalmente contribuyen a calmar la inflamación y a apoyar células inmunitarias regulatorias que evitan daños por fuego amigo contra los propios tejidos. Su pérdida, junto con la reducción de aminoácidos como la arginina y los aminoácidos ramificados, puede privar a las células inmunes y neuronales de combustibles y mensajeros clave. Las vías mTOR y de transporte alteradas podrían a su vez orientar a las células inmunitarias hacia comportamientos más agresivos e inflamatorios e interferir con el mantenimiento y la reparación del aislamiento graso alrededor de las fibras nerviosas. El aumento de ciertas moléculas relacionadas con el estrés sugiere que el daño oxidativo—esencialmente el desgaste bioquímico—podría estar aumentado en personas con EM.
Qué significa esto para los pacientes
El estudio no prueba que estos cambios químicos relacionados con el intestino causen la EM, pero sugiere con fuerza que el ambiente intestinal y sus subproductos metabólicos están estrechamente ligados a la enfermedad. El patrón distintivo de aminoácidos, ácidos grasos y otras pequeñas moléculas en las heces podría servir como una huella no invasiva para ayudar a rastrear la actividad de la enfermedad o la respuesta al tratamiento. Más en general, apoya la idea de que ajustar la dieta, los microbios intestinales o metabolitos específicos podría algún día complementar los fármacos dirigidos al sistema inmunitario. En términos sencillos, lo que ocurre en el intestino no se queda en el intestino: su química puede influir en cómo se ataca o protege el cerebro en la esclerosis múltiple.
Cita: Wang, D., Feng, W., Wang, H. et al. Research on metabolic characteristics of multiple sclerosis. Sci Rep 16, 12526 (2026). https://doi.org/10.1038/s41598-026-42501-3
Palabras clave: esclerosis múltiple, microbioma intestinal, metabolómica, ácidos grasos de cadena corta, biomarcadores fecales