Clear Sky Science · es
El Factor VIII restaura parámetros óseos y modula el proteo-metaboloma muscular en ratones machos knockout para el Factor VIII
Por qué una proteína de la coagulación importa para huesos y músculos
Las personas con hemofilia A son conocidas por sus problemas de sangrado, pero muchos también desarrollan huesos frágiles y músculos débiles. Este estudio plantea una pregunta simple pero importante: ¿la proteína de la coagulación ausente en la hemofilia, denominada Factor VIII, moldea directamente cómo crecen y se mantienen sanos los huesos y los músculos? Usando ratones que carecen por completo de Factor VIII y administrando a algunos de ellos una versión recombinante de la proteína, los investigadores trazan cómo esta única molécula puede influir en el esqueleto, en los vasos sanguíneos dentro del hueso e incluso en la química de las células musculares.
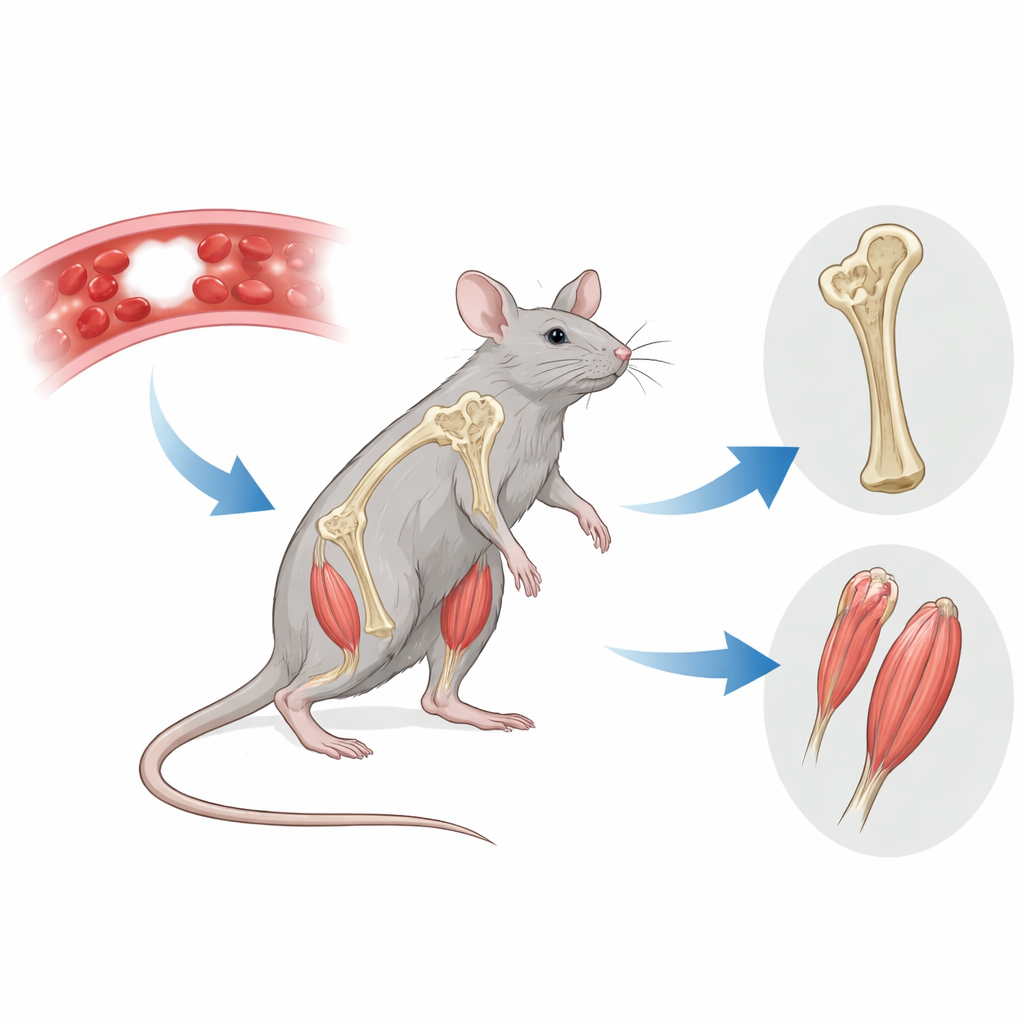
Huesos débiles en ausencia de una proteína clave
El equipo examinó primero los huesos de ratones machos jóvenes y jóvenes-adultos que carecen de Factor VIII. Mediante escaneos de rayos X de alta resolución, hallaron que estos animales presentaban un patrón óseo similar al de la osteoporosis: menor volumen de hueso esponjoso, menos travesaños finos de sostén dentro del hueso y espacios vacíos mayores. La densidad mineral ósea tendía también a ser más baja. Al observar más detenidamente bajo el microscopio, vieron que la fina red de pequeños vasos sanguíneos cerca de los extremos en crecimiento de los huesos estaba reducida, especialmente las venas y los capilares que nutren el tejido óseo. Al mismo tiempo, el número de células formadoras de hueso (osteoblastos) disminuyó claramente en los animales jóvenes, lo que sugiere que el esqueleto tiene dificultades para depositar suficiente hueso nuevo durante el periodo crítico de crecimiento.
Restaurar el Factor VIII reconstruye hueso y vasos sanguíneos
Para averiguar si este daño podía revertirse, los científicos trataron a ratones deficientes en Factor VIII con infusiones semanales de una proteína recombinante de Factor VIII durante varias semanas. Tras el tratamiento, la estructura interna de los huesos largos mejoró notablemente: hubo más hueso esponjoso, más de los pequeños travesaños de sostén y huecos más pequeños entre ellos. La red de pequeños vasos en la médula ósea también se recuperó hacia la normalidad, en particular las venas y los capilares. Las células formadoras de hueso aumentaron, mientras que las células que reabsorben hueso se redujeron. Es importante que se observaron beneficios similares tanto con versiones pegiladas como no pegiladas de la proteína, lo que indica que los efectos positivos provienen del propio Factor VIII y no de modificaciones químicas del fármaco. En conjunto, estos resultados sugieren que el Factor VIII ayuda a mantener un equilibrio saludable entre la formación ósea, la degradación ósea y el aporte sanguíneo dentro del esqueleto.
Cambios musculares sorprendentes y química celular alterada
El panorama en el músculo fue más complejo. Los ratones jóvenes deficientes en Factor VIII tenían de hecho músculos de las patas más pesados con fibras más grandes de lo normal, pero conforme maduraban, sus tipos de fibra se desplazaron hacia una forma que favorece contracciones rápidas y potentes pero que se fatigan con facilidad. Los análisis detallados de proteínas y metabolitos revelaron que los músculos sin Factor VIII mostraban una actividad atenuada en las centrales energéticas (mitocondrias) y en la maquinaria que sintetiza nuevas proteínas, junto con cambios en moléculas relacionadas con la energía y en los antioxidantes. Estos cambios apuntan a músculos que demandan más combustible y operan con peor “economía metabólica”, lo que en última instancia podría traducirse en fatiga prematura y debilidad, reflejando lo que se observa en muchas personas con hemofilia.
Rescate parcial de la respuesta muscular e inmune
Cuando los ratones recibieron Factor VIII recombinante, parte de la química muscular anómala volvió hacia la normalidad, y las fibras musculares se hicieron algo más pequeñas y homogéneas. Sin embargo, la mezcla básica de tipos de fibras no revirtió por completo, y los cambios estructurales del músculo solo se corrigieron parcialmente. En un experimento separado, los investigadores lesionaron músculos de las patas con una toxina para imitar un daño severo. Los ratones carentes de Factor VIII mostraron un reclutamiento temprano reducido de macrófagos proinflamatorios—células inmunitarias que ayudan a limpiar los desechos e iniciar la reparación—pero este defecto se corrigió en parte con el tratamiento con Factor VIII. Aun así, los músculos completamente regenerados en los ratones tratados seguían difiriendo de los de animales normales, lo que sugiere que una vez que se han producido cambios vasculares o durante el desarrollo temprano, no pueden deshacerse por completo más adelante en la vida.
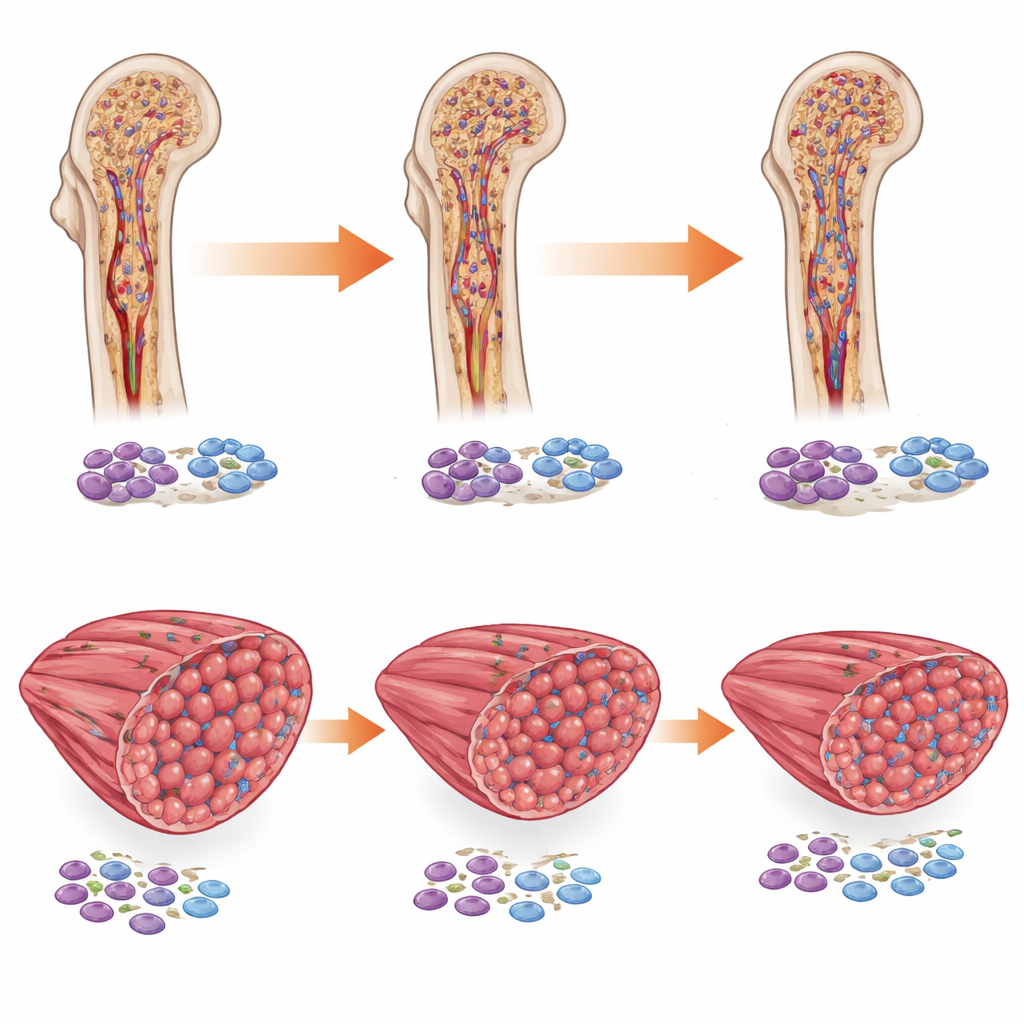
Qué significa esto para las personas con hemofilia
En conjunto, el estudio muestra que el Factor VIII es más que un ayudante de la coagulación: contribuye a moldear la estructura ósea, sostiene los pequeños vasos sanguíneos que alimentan el hueso en crecimiento e influye en cómo los músculos usan la energía y se recuperan de las lesiones. Reponer el Factor VIII en ratones puede reparar en gran medida la debilidad ósea y mejorar el suministro de sangre al hueso, mientras que solo normaliza parcialmente las propiedades musculares. Para las personas con hemofilia A, estos hallazgos respaldan la reposición temprana y consistente de Factor VIII para proteger la salud ósea, y sugieren que podrían necesitarse estrategias adicionales para abordar plenamente la debilidad muscular y la fragilidad de aparición temprana.
Cita: Babuty, A., Muñoz-Garcia, J., Christophe, O.D. et al. Factor VIII restores bone parameters and modulates muscle proteo-metabolome in Factor VIII knockout male mice. Bone Res 14, 30 (2026). https://doi.org/10.1038/s41413-025-00485-2
Palabras clave: hemofilia A, Factor VIII, salud ósea, músculo esquelético, terapia recombinante