Clear Sky Science · de
Chemische Ansätze zur kontrollierten Freisetzung von Kohlenmonoxid: Fokus auf organische molekulare Donoren
Vom tödlichen Dampf zum nützlichen Signal
Kohlenmonoxid ist am bekanntesten als lautloser Killer durch defekte Heizungen und Autoabgase, doch in unserem Körper wird dasselbe Gas in winzigen Mengen gebildet und hilft dort stillschweigend, Zellen zu schützen. Dieser Übersichtsartikel untersucht, wie Chemiker Kohlenmonoxid in intelligente „Donor“-Moleküle verpacken, die es wie ein Arzneimittel transportieren und freisetzen können. Indem man ein gefährliches Gas in ein kontrollierbares Medikament verwandelt, hoffen Forschende, Probleme wie Entzündungen, Organverletzungen nach Schlaganfall oder Herzinfarkt und hartnäckige Infektionen zu behandeln — ohne Vergiftungsrisiken.
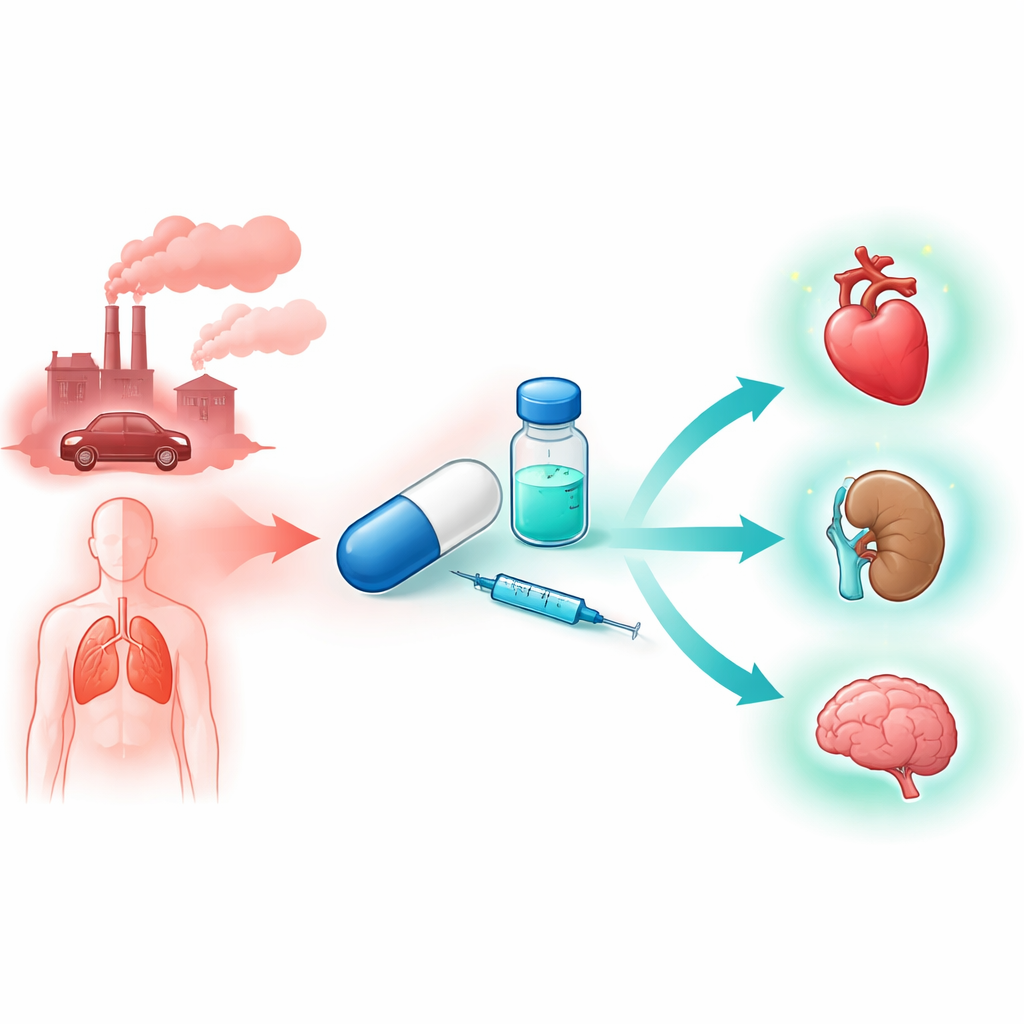
Warum der Körper ein Gift absichtlich nutzt
Kohlenmonoxid ist ein einfaches Gas aus einem Kohlenstoff- und einem Sauerstoffatom, hat aber eine gespaltene Persönlichkeit. In hohen Konzentrationen bindet es stark an den Sauerstoffträger im Blut und erstickt Gewebe. In sehr geringen Mengen jedoch produzieren unsere Zellen es als Botenstoff, ähnlich dem bekannteren Stickstoffmonoxid. In diesem sanften Bereich kann es Entzündungen dämpfen, Zellsterben reduzieren und Blutgefäße entspannen. Das Problem ist, dass das Einatmen des Gases oder das Einarbeiten in Flüssigkeiten kaum Kontrolle über Dosis, Ort oder Zeitpunkt erlaubt. Benötigt wird statt dessen eine Methode, Kohlenmonoxid sicher durch den Körper zu schleusen und es nur dort und dann freizusetzen, wo es nützlich ist.
Tabletten und Prodrugs: Ein Gas in Flaschen
Um dieses Problem zu lösen, entwerfen Chemiker CO-freisetzende Moleküle, sogenannte CORMs. Frühe Versionen basierten auf Metallen, die CO stark binden, doch Bedenken wegen Metallakkumulation und Nebenwirkungen haben das Feld zu metallfreien, rein organischen Designs getrieben. Diese organischen Donoren halten CO in einem größeren kohlenstoffbasierten Gerüst, das unter ausgewählten Bedingungen zerfällt und das Gas freisetzt. Die Übersicht ordnet sie in drei Haupttypen: offene Kettenmoleküle, Einring-Systeme und steifere bicyclische oder überbrückte Strukturen. Über diese Familien hinweg ist eine einigende Idee, CO in einem „gespannten“ Zustand zu behalten, der während der Lagerung stabil ist, aber bei Reizung durch den richtigen Auslöser — etwa Wasser, Licht, Wärme oder chemische Veränderungen im erkrankten Gewebe — freigegeben wird.
Mit Form, Spannung und Licht spielen
Offenkettige Donoren umfassen modifizierte Säuren, bor- und siliziumhaltige Fragmente sowie spezielle Aldehyde. Clevere Änderungen machen sie in der Flasche stabil, aber im Körper leicht aktivierbar — zum Beispiel durch Enzyme oder milde Säure —, sodass ein stetiger, kontrollierbarer CO-Stoß zusammen mit überwiegend harmlosen Rückständen entsteht. Ringförmige Donoren fügen eine weitere Kontrollschicht hinzu, indem sie CO in gespannte Drei-, Vier-, Fünf- oder Sechsring-Schleifen einbauen. Die Spannung im Ring wirkt wie eine verbogene Feder: Sobald ein Auslöser einwirkt, schnellt der Ring auf und stößt CO aus. Kleinere Ringe setzen tendenziell schnell frei, während größere so konstruiert werden können, dass sie auf Signale wie reaktive Sauerstoffspezies reagieren, die in entzündetem oder gestresstem Gewebe vorkommen. Viele Designs sind mit fluoreszierenden Farbstoffen gekoppelt, sodass dasselbe Molekül sowohl CO freisetzt als auch aufleuchtet, wodurch Ärzte und Wissenschaftler beobachten können, wann und wo das Gas erscheint.
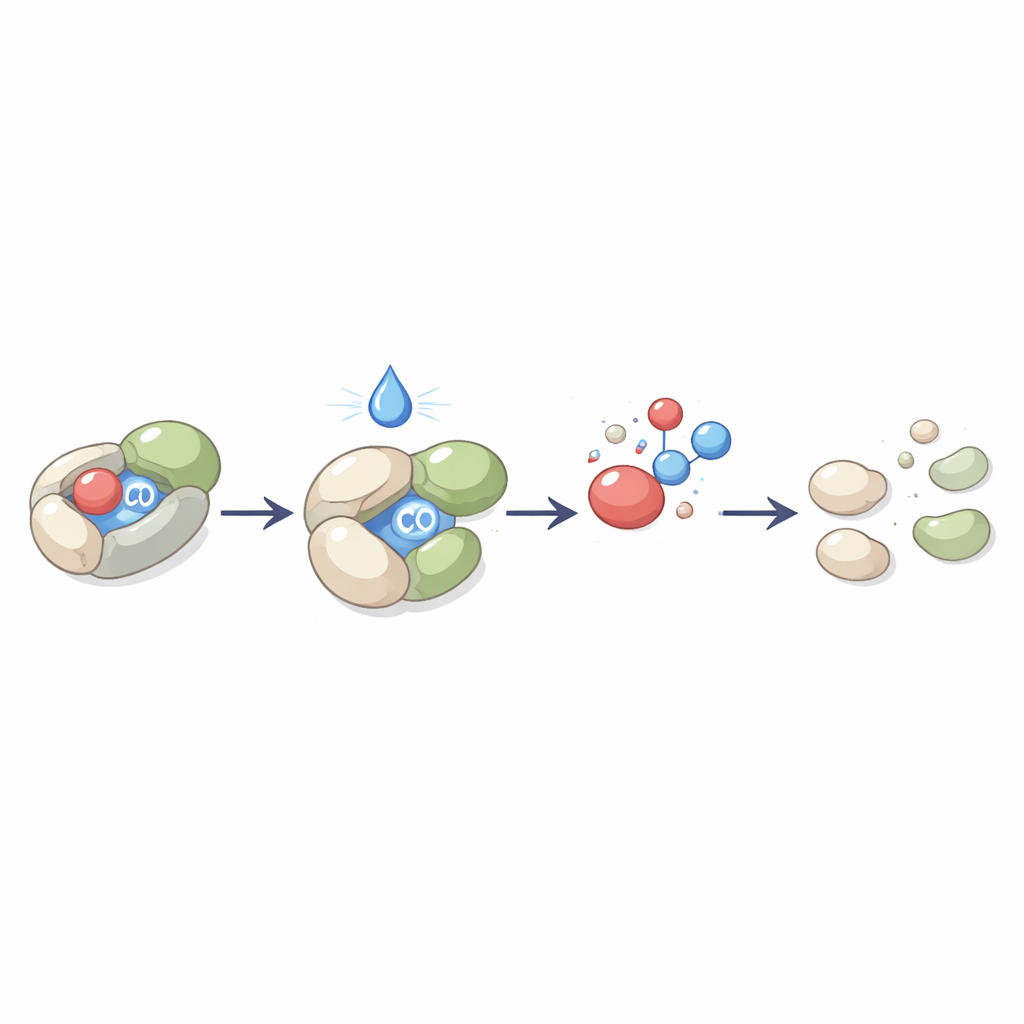
Intelligente Schalter und Logikgatter in der Medizin
Die fortschrittlichsten Systeme verhalten sich fast wie winzige Computer. Einige überbrückte Donoren nutzen „Click“-Reaktionen, um eine hochgespannte Struktur an bestimmten Orten zu erzeugen, etwa in speziellen Zellkompartimenten oder auf Materialoberflächen; diese Struktur zerstört sich dann selbst und setzt CO frei. Andere reagieren nur, wenn zwei Bedingungen erfüllt sind, etwa das Vorhandensein einer krankheitsbezogenen Chemikalie plus Licht, und bilden so ein „UND“-Gatter, das die Selektivität deutlich verbessert. Sichtbares oder nahes Infrarotlicht, Ultraschall oder eingebaute Empfindlichkeit gegenüber Oxidantien und Enzymen können allesamt als Ein-/Ausschalter dienen. Diese ausgefeilten Designs öffnen die Tür zu künftigen Therapien, bei denen eine Tablette, ein Pflaster oder ein injizierbares Material CO diskret durch den Körper transportiert und es nur im erkrankten Gewebe freigibt, während es gleichzeitig seine Aktivität durch eine Farb- oder Leuchtänderung meldet.
Wohin diese Forschung führen könnte
Vereinfacht gesagt kommt der Artikel zu dem Schluss, dass die Verwandlung von Kohlenmonoxid in ein sicheres Medikament von einer Chemie abhängt, die dieses Gas einkapseln, zielen und präzise freisetzen kann. Organische CO-Donoren bieten mittlerweile ein breites Menü an Optionen — schnelle oder langsame Freisetzung, Licht- oder chemische Auslöser und eingebaute Bildgebung — und rücken die Idee von „CO in einer Tablette“ wesentlich näher. Die verbleibenden Hürden bestehen darin, Stabilität und Reagibilität auszubalancieren, alle Nebenprodukte vollständig zu verstehen und beherrschbar zu machen sowie diese komplexen Moleküle praktikabel herzustellen und zu verabreichen. Können diese Herausforderungen gemeistert werden, könnte aus einem einst nur als Haushaltsrisiko gefürchteten Gas ein mächtiges, zielgerichtetes Werkzeug gegen Entzündungen, Organverletzungen und bestimmte Infektionen werden.
Zitation: Mu, W., Chen, X., Zhang, Z. et al. Chemical approaches to controlled carbon monoxide release: a focus on organic molecular donors. npj Soft Matter 2, 9 (2026). https://doi.org/10.1038/s44431-026-00021-0
Schlüsselwörter: Kohlenmonoxidtherapie, CO-freisetzende Moleküle, organische Prodrugs, stimuli-responsiver Wirkstofftransport, photoaktivierte Medizin