Clear Sky Science · de
Molekulare Prägung im Kanal eines organischen elektrochemischen Transistors auf Basis eines Doppelnetzwerk‑Hydrogels für die Glukoseerkennung
Intelligentere Sensoren für die tägliche Zuckerüberwachung
Glukose, der einfache Zucker, der unseren Körper antreibt, ist zugleich ein wichtiger Gesundheitsindikator. Menschen mit Diabetes oder Prädiabetes verlassen sich zunehmend auf kleine Sensoren, um ihre Glukosewerte ohne ständige Fingerstiche zu überwachen. Diese Studie untersucht eine neue Art weichen, elektrisch aktiven Materials, das direkt in winzige elektronische Schalter eingebaut werden kann, mit dem Ziel, künftige Glukosemonitore empfindlicher, selektiver gegenüber Glukose gegenüber anderen Zuckern und angenehmer zu tragen zu machen.
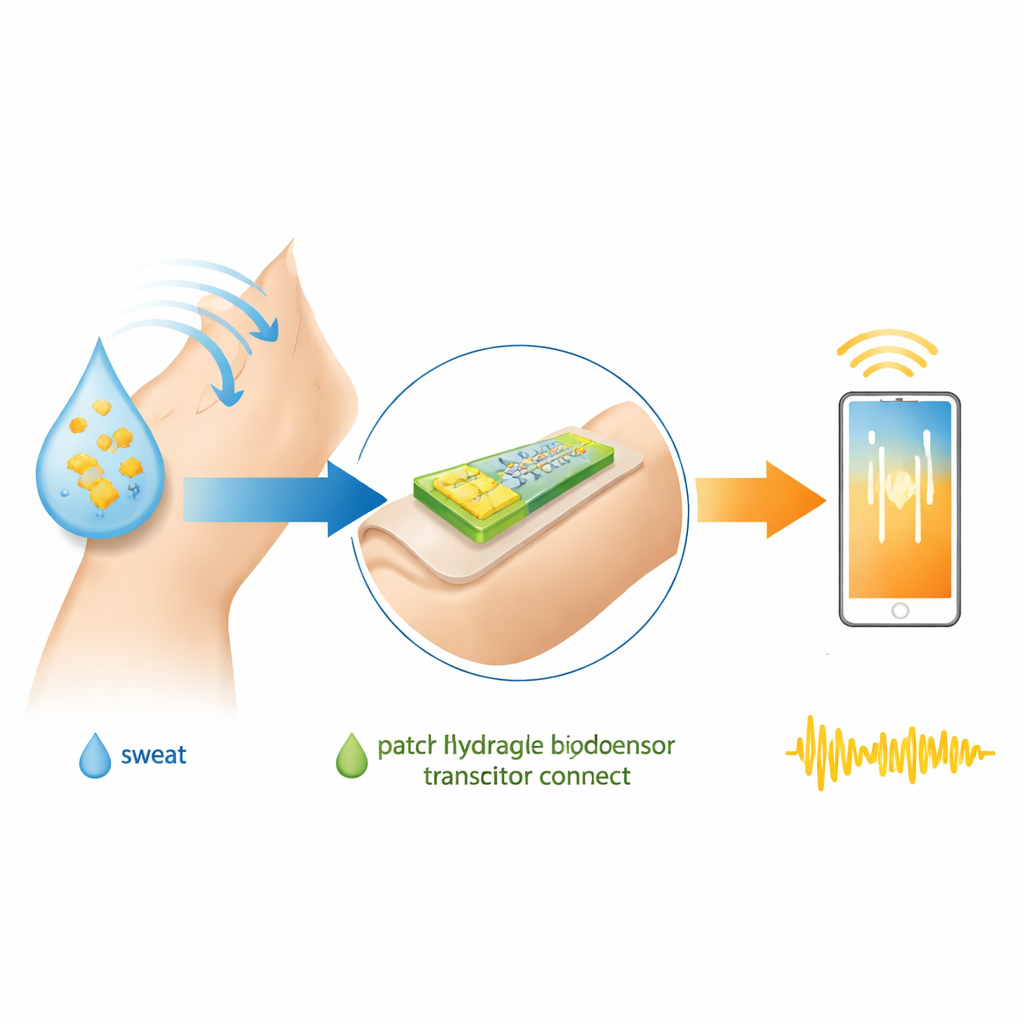
Ein weicher elektrischer Schalter, der Wasser mag
Die Forscher konzentrieren sich auf organische elektrochemische Transistoren, eine Klasse elektronischer Bauelemente, die in salzigen, wässrigen Umgebungen wie Blut, Schweiß oder Speichel gut funktionieren. Im Gegensatz zu herkömmlichen Siliziumchips, die von Flüssigkeiten isoliert werden, verwenden diese Transistoren einen weichen, leitfähigen Polymerkanal, der es Ionen aus einer umgebenden Lösung erlaubt, hinein- und herauszuwandern. Diese Bewegung verändert, wie leicht elektrischer Strom fließt, und wandelt biologische Aktivität an der Oberfläche in ein lesbares elektronisches Signal um. Ein gängiges Material für diesen Kanal ist PEDOT:PSS, ein flexibles, biokompatibles Polymer, das zu einem Hydrogel – einem wasserreichen, gelartigen Feststoff – geformt werden kann.
Dem Gel beibringen, Glukose zu erkennen
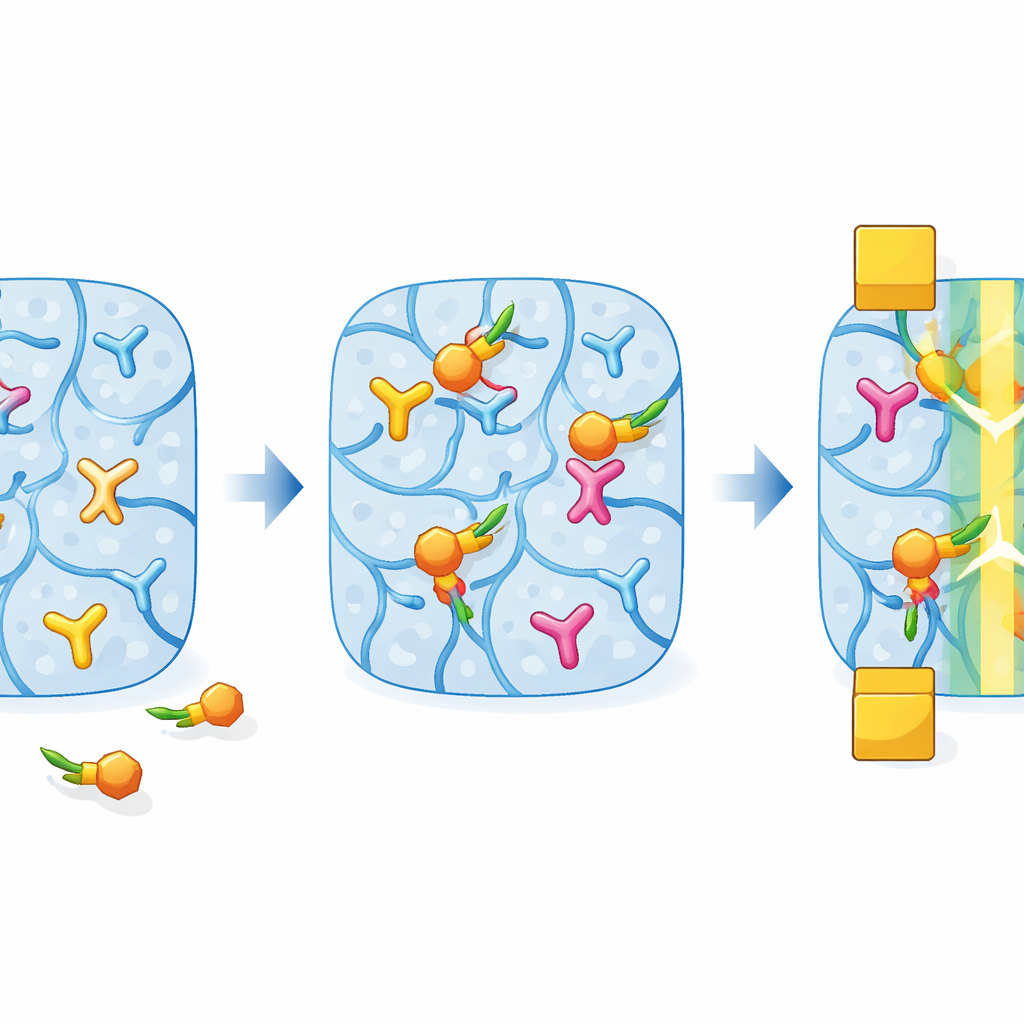
Um den weichen Kanal gezielt auf Glukose reagieren zu lassen, greift das Team ein Konzept namens molekulare Prägung auf. Während der Herstellung mischen sie in das Gel einen „Rezeptor“-Baustein ein, der gerne Moleküle mit paarweisen sauerstoffhaltigen Gruppen bindet, wie etwa Zucker. Gleichzeitig fügen sie echte Glukose als temporären Gast hinzu. Während sich das zweite Polymernetz im PEDOT:PSS‑Gel bildet und vernetzt, umschließt es diese Glukose‑Gäste und schafft winzige Hohlräume, die in Größe und Bindungsmuster zur Glukose passen. Anschließend wird die Glukose mit einer sauren Lösung ausgewaschen, sodass ein Schwamm mit glukoseförmigen Taschen zurückbleibt, der bereit ist, erneut Glukose aufzunehmen, wenn sie auftaucht.
Von Bindungsereignissen zu stärkeren elektrischen Signalen
Wenn eine glukosehaltige Flüssigkeit mit diesem Doppelnetzwerk‑Hydrogelkanal in Kontakt kommt, gleitet Glukose in die geprägten Taschen und reagiert mit den Rezeptorgruppen, wodurch sich deren elektrische Ladung ändert. Diese lokalen chemischen Änderungen beeinflussen, wie leicht das PEDOT:PSS‑Rückgrat Elektronen und Ionen austauschen kann, was wiederum den Strom durch den Transistor verändert. Die Autoren stellen zunächst sicher, dass das Gel gleichmäßig in engen Röhrchen gebildet wird, damit es gut an Goldelektroden haftet und sich konsistent verhält. Dann vergleichen sie Kanäle, die mit und ohne Glukose‑Template hergestellt wurden, und messen, wie die Stromantwort des Transistors mit steigender Glukosekonzentration über einen weiten Bereich wächst. Durch Anpassung der Daten an ein Modell, das beschreibt, wie Moleküle Bindungsstellen besetzen, schätzen sie eine effektive „Bindungsstärke“ zwischen Glukose und dem Gel ab.
Scharfer Blick für Glukose gegenüber anderen Zuckern
Die molekular geprägten Kanäle zeigen einen klaren Vorteil. Ihre scheinbare Bindungskonstante für Glukose ist etwa zehnmal höher als die von nicht geprägten Gelen, was bedeutet, dass Glukose stärker und effizienter eingefangen wird. Infolgedessen wird die Antwort des Transistors auf kleine Änderungen der Glukosekonzentration bei niedrigen Werten steiler, und die minimale Konzentration, die noch zuverlässig erkannt werden kann, fällt in den Sub‑Mikromolarbereich – deutlich unterhalb der typischen Glukosewerte im menschlichen Schweiß. Wichtig ist zudem, dass das Gel selektiver wird: Im geprägten Material wird Glukose gegenüber einem ähnlichen Zucker, Fruktose, um etwa zwei Größenordnungen bevorzugt im Vergleich zur gleichen Chemie in einfacher Lösung. Die Verstärkungseigenschaften des Transistors selbst helfen, diese chemischen Unterschiede in robuste elektrische Signale zu übersetzen, ohne separate Verstärkerschaltungen zu benötigen.
Warum das für künftige tragbare Gesundheitsgeräte wichtig ist
Für Leser ohne Fachkenntnisse ist die zentrale Botschaft, dass die Autoren ein weiches, wasserliebendes elektronisches Material so „trainiert“ haben, dass es sich an Glukose „erinnert“, und dieses Gedächtnis direkt in einen winzigen Schalter eingebaut haben. Diese Kombination aus molekularer Prägung innerhalb eines leitfähigen Hydrogels, verwendet als aktiver Kanal eines organischen elektrochemischen Transistors, führt zu stärkeren Bindungen an Glukose, besserer Unterscheidung gegenüber anderen Zuckern und einer niedrigeren Nachweisgrenze in einem Bereich, der für die Überwachung mittels Schweiß geeignet ist. Obwohl Herausforderungen bestehen – etwa der Umgang mit störenden Substanzen in echten Körperflüssigkeiten und die Sicherstellung langfristiger Stabilität – weist die Arbeit auf dünne, flexible Pflaster hin, die eines Tages kontinuierlich Zuckerwerte verfolgen könnten, indem sie subtile elektrische Veränderungen in einem intelligenten Gel messen, das sanft auf die Haut gedrückt wird.
Zitation: Kawamura, M., Tseng, A.C. & Sakata, T. Molecular imprinting in double-network-hydrogel-based organic electrochemical transistor channel for glucose sensing. npj Biosensing 3, 24 (2026). https://doi.org/10.1038/s44328-026-00093-y
Schlüsselwörter: Glukosesensor, tragbarer Biosensor, organischer elektrochemischer Transistor, molekulare Prägung, Hydrogel‑Elektronik