Clear Sky Science · de
Frühe cAMP-Signale orchestrieren die Einzellen-Synchronizität während der Entwicklung von Dictyostelium
Wie Zellen ihre gemeinsame Zeit halten
Viele Lebewesen wachsen auf bemerkenswert koordinierte Weise: Abschnitte einer Fischwirbelsäule entstehen nacheinander, die Einheiten eines Fliegenauges reihen sich wie Kacheln auf, und sogar einzellige Organismen können sich synchron bewegen und ihre Form ändern. Dieser Artikel untersucht, wie die bodenbewohnende Amöbe Dictyostelium discoideum Tausende ihrer Zellen während der Entwicklung im Gleichschritt hält. Das Verständnis dieser natürlichen „Zell-Choreografie“ hilft zu erklären, wie Gewebe korrekt entstehen – und was schiefgehen kann, wenn das Timing aus dem Takt gerät.
Eine soziale Amöbe mit Teamfähigkeit
Dictyostelium lebt die meiste Zeit als einzelne Amöben, die umherkriechen und Bakterien fressen. Wenn die Nahrung knapp wird, werden diese Einzelgänger plötzlich hochgradig sozial. Sie sammeln sich zu sichtbaren Klumpen, bilden fingerartige Strukturen, sogenannte Slugs, und schließlich schlanke Fruchtkörper, die Sporen in die Luft heben. Das alles vollzieht sich in etwa einem Tag, und verschiedene Zellgruppen auf einer Platte sehen in jedem Stadium oft fast identisch aus. Die Frage, die sich die Forschenden stellten, lautet: Wie schaffen es so viele einzelne Zellen, ihren inneren Zustand und ihre äußere Form so synchron zu verändern?
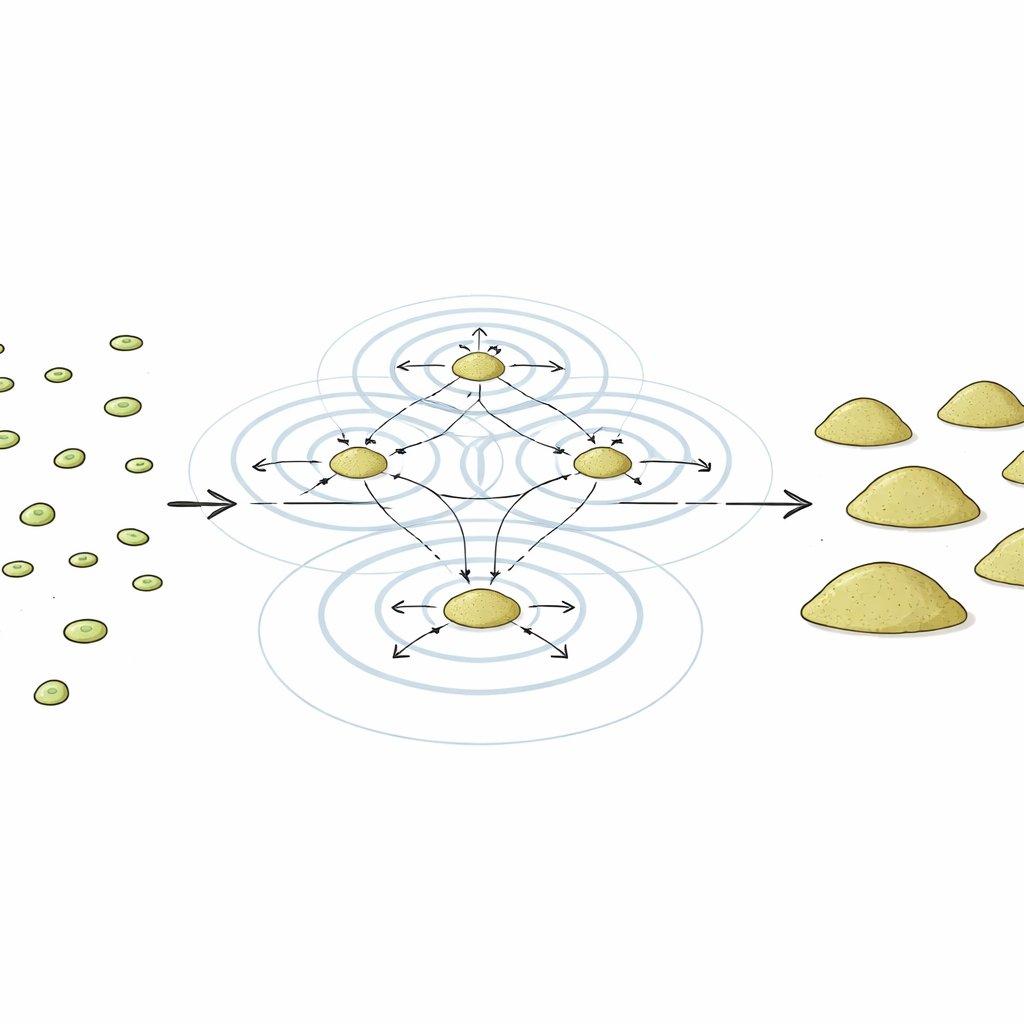
Ein chemischer Impuls, der das Tempo vorgibt
Frühere Arbeiten zeigten, dass hungernde Amöben sich rhythmische Stöße eines kleinen Signalmoleküls namens cAMP zusenden. Alle paar Minuten laufen Wellen von cAMP durch die Zellpopulation und leiten die Zellen an, sich zu bewegen und multizelluläre Klumpen zu bilden. Die Autor:innen schlugen vor, dass diese frühen cAMP-Impulse mehr bewirken als nur die Richtung vorzugeben — sie könnten auch wie ein Metronom wirken, das die inneren Programme von Tausenden Zellen im Takt hält, sodass Gene gleichzeitig aktiviert und abgeschaltet werden, während die Entwicklung fortschreitet.
Zellzustände einzeln auslesen
Um diese Idee zu prüfen, nutzte das Team die Einzelzell-RNA-Sequenzierung, eine Technik, die abliest, welche Gene in Tausenden einzelner Zellen gleichzeitig aktiv sind. Sie züchteten drei Versionen von Dictyostelium: einen normalen Stamm; ein Mutantenstamm, der keine cAMP-Impulse erzeugen kann; und einen Doppelmutanten, der nicht pulsen kann, aber durch die Aktivierung eines Schlüsselenzyms trotzdem zur Entwicklung gezwungen wird. Zu mehreren Zeitpunkten über 20 Stunden hinweg fingen sie Zellen ein und maßen deren RNA-Profile. Indem sie verglichen, wie ähnlich oder unterschiedlich diese Profile zwischen den Zellen waren, konnten sie eine numerische Kennzahl für „Synchronizität“ berechnen — also wie ähnlich die inneren Zustände der Zellen zu jedem Moment der Entwicklung waren.
Wenn das Metronom funktioniert — und wenn nicht
Bei normalen Zellen fiel die Synchronizität zunächst unmittelbar nach dem Hungern ab, was den Schock der veränderten Bedingungen widerspiegelt. Dann, zwischen vier und acht Stunden, als cAMP-Impulse auftauchten und die Zellen zu sammeln begannen, stieg die Synchronizität stark an und blieb auch in späteren Stadien hoch. Selbst als sich die Zellen in zwei Hauptschicksale aufspalteten — sporenbildende und stielbildende Typen — blieben die Zellen innerhalb jeder Gruppe eng koordiniert. Im auffälligen Gegensatz dazu bildeten Zellen, die keine cAMP-Impulse erzeugen konnten, nie richtige multizelluläre Strukturen und zeigten nur schwache, instabile Synchronizität über die Zeit. Der Doppelmutant, der sich ohne Pulse entwickeln kann, erreichte zwar fortgeschrittene Formen, aber seine Zellen gerieten außer Tritt: Zu jedem Zeitpunkt verteilten sie sich über viele Entwicklungszustände, und benachbarte Aggregate befanden sich oft sichtbar in unterschiedlichen Stadien.
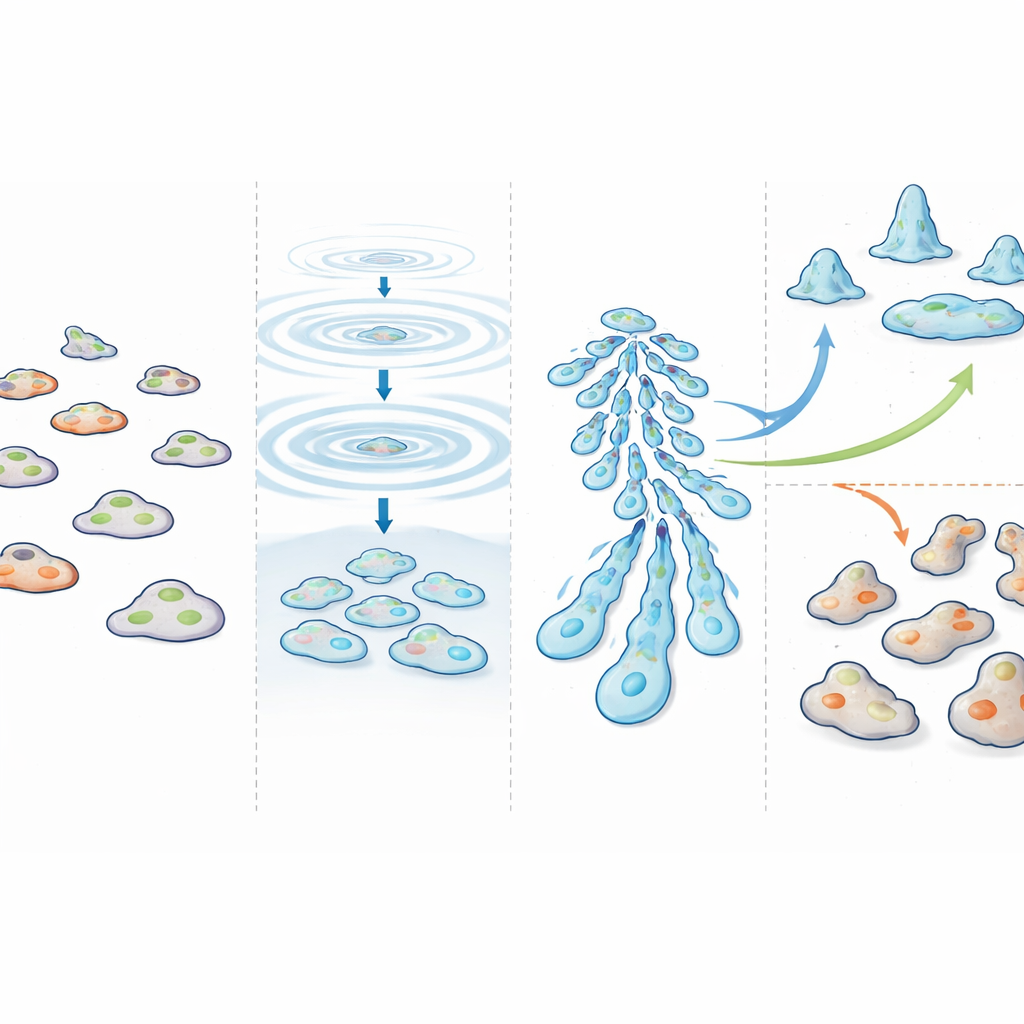
Ein genauer Blick auf Zelltypen und Entwicklungspfade
Mithilfe computergestützter Karten der Einzelzell-Daten verfolgten die Autor:innen, wie sich normale Zellen von frühen Einzelstadien zu späten multizellulären Formen bewegten. Sie konnten das Aufzweigen in zukünftige Sporen- und Stielzellen klar erkennen und bestätigten, dass Sporen-Vorläufer eine homogenere Gruppe bilden als die variableren Stiel-Vorläufer. Bemerkenswerterweise wählten die Zellen des Doppelmutanten ohne cAMP-Impulse dennoch dieselben zwei Hauptschicksale und folgten einem grob ähnlichen Pfad — nur nicht zur selben Zeit. Das zeigt, dass cAMP-Impulse nicht darüber entscheiden, was jede Zelle wird, wohl aber entscheidend dafür sind, dass viele Zellen diese Schicksale gleichzeitig erreichen.
Warum das für multizelluläres Leben wichtig ist
Die Studie schlussfolgert, dass frühe Wellen von cAMP als übergeordnetes Zeitsignal wirken, das sowohl die innere Genaktivität als auch die äußeren Formen der Dictyostelium-Zellen ausrichtet. Hat diese frühe Uhr einmal ihre Arbeit getan, kann sich die Entwicklung größtenteils synchron entfalten, unterstützt von weiteren, lokaleren Signalen zwischen Zellen. Obwohl dieser Mechanismus spezifisch für soziale Amöben ist, ähnelt das zugrundeliegende Prinzip — rhythmische chemische Signale zu nutzen, um Zellen auf denselben Zeitplan zu bringen — den Timing-Systemen in tierischen Embryonen. Indem gezeigt wird, dass Einzelzell-RNA-Sequenzierung Synchronizität über die Zeit quantifizieren kann, liefert diese Arbeit außerdem einen Bauplan, um zu untersuchen, wie Timing in komplexeren Organismen kontrolliert wird und was passiert, wenn dieses Timing zusammenbricht.
Zitation: Katoh-Kurasawa, M., Trnovec, L., Lehmann, P. et al. Early cAMP signaling orchestrates single-cell synchronicity throughout Dictyostelium development. Commun Biol 9, 543 (2026). https://doi.org/10.1038/s42003-026-09806-5
Schlüsselwörter: Zell-Synchronizität, Entwicklung von Dictyostelium, cAMP-Signalgebung, Einzelzell-RNA-Sequenzierung, multizellulare Koordination