Clear Sky Science · de
Personalisierte Analyse von Signalkaskaden bei gastrointestinalen Tumoren zur Patientenstratifizierung und Bewertung von Wirkstoffzielen mithilfe klinisch gewonnener Kernbiopsien
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Krebsspezialisten versuchen zunehmend, Therapien an die spezifische Biologie des Tumors jeder einzelnen Person anzupassen. Bei Krebserkrankungen des Verdauungssystems – etwa von Bauchspeicheldrüse, Darm, Leber oder Gallengängen – ist das besonders dringend, denn sie sind häufig, werden oft spät erkannt und sind schwer zu behandeln. Diese Studie untersucht eine neue Labormethode, die die Aktivität zahlreicher krebsrelevanter Proteine aus winzigen Biopsieproben ablesen kann, mit dem Ziel, Ärztinnen und Ärzte dabei zu unterstützen, präzisere Therapien für einzelne Patientinnen und Patienten auszuwählen.
Von DNA‑Listen zu lebendigen Signalen
Bislang beruht die meiste „personalisierte“ Krebsbehandlung auf der Analyse von DNA‑Veränderungen im Tumor. Zwar ist das mächtig, aber DNA allein zeigt nicht, welche Signale innerhalb der Zelle tatsächlich angeschaltet sind und das Wachstum antreiben. Diese Signale werden von Proteinen vermittelt, von denen viele direkt durch Medikamente angreifbar sind. Die Forschenden verwendeten eine hochdurchsatzfähige Technik namens DigiWest, eine moderne Variante des klassischen Westernblots, um gleichzeitig etwa 130–200 Proteine und deren aktivierte Formen zu messen. Wichtig ist, dass diese Methode nur etwa so viel Material benötigt wie eine einzelne Nadelbiopsie und sich damit für die klinische Praxis eignet.
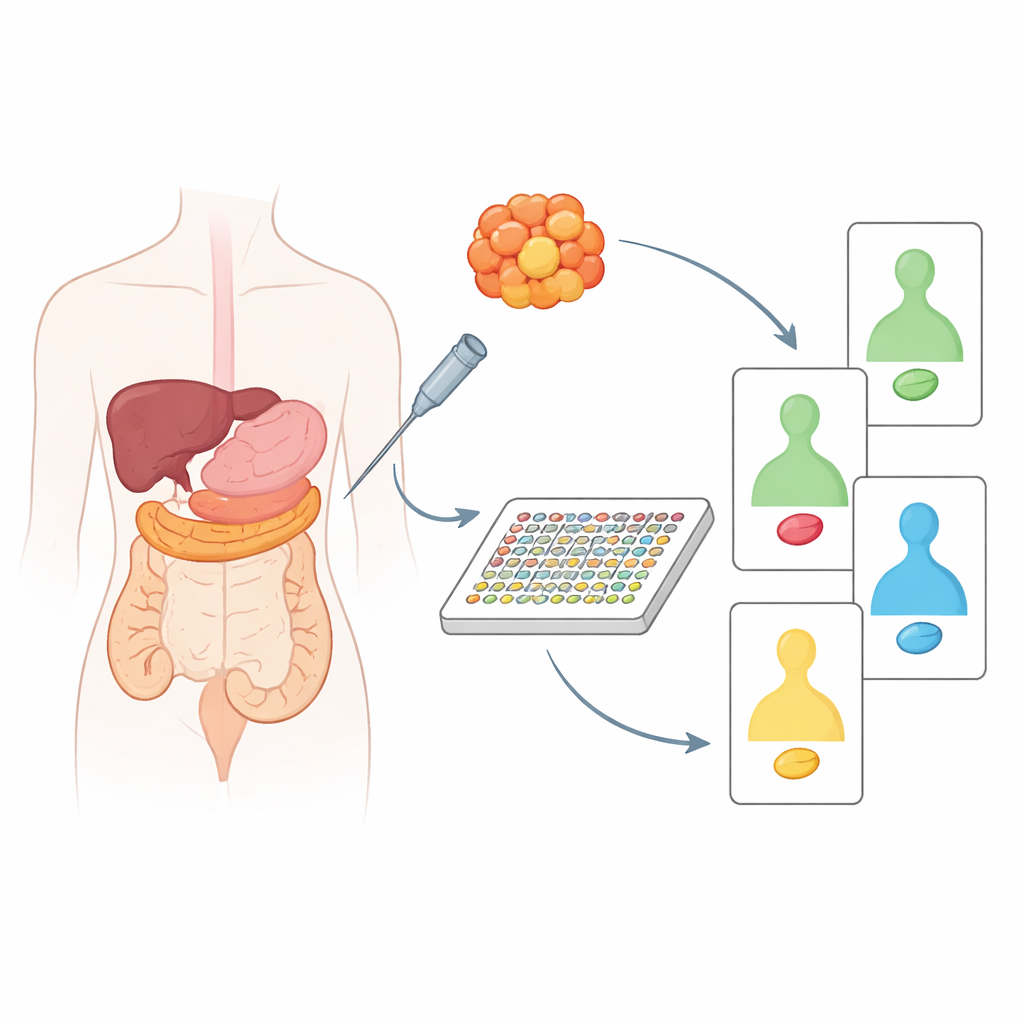
Vergleich von Tumorgewebe mit dem gesunden Nachbargewebe
Das Team analysierte zunächst archiviertes Gewebe von 20 Patientinnen und Patienten mit Bauchspeicheldrüsen‑ oder Darmkrebs, jeweils gepaart mit nahegelegenem nicht‑tumorösem Gewebe derselben Person. Durch den Vergleich der Tumoren mit ihren eigenen gesunden Gegenstücken konnten sie feststellen, welche Proteine wirklich durch den Krebs verändert waren und nicht nur normale Unterschiede zwischen Organen widerspiegelten. Dabei zeigten sich deutliche Unterschiede im Verhalten bekannter Tumorsuppressoren und Treiber wie p53, Ras, PTEN und anderen. Pankreastumoren wiesen beispielsweise tendenziell verstärkte wachstumsfördernde Signale und den Verlust schützender Proteine auf, während Darmtumoren ein eigenes, charakteristisches Muster gestörter Signalwege zeigten. Bei einer Clusteranalyse auf Basis dieser Proteinveränderungen ließen sich Pankreastumoren in zwei biologisch unterschiedliche Gruppen einteilen und aussagekräftige Unterschiede bei Darmtumoren erkennen, die mit dem Alter der Patienten und dem Tumorort im Darm zusammenhingen.
Individuelle Tumor‑„Barcodes“ der Signalaktivität
Über Gruppenmittelwerte hinaus erstellten die Forscher für jeden Tumor ein detailliertes Proteinprofil. Diese Profile machten deutlich, welche Signalwege – etwa mTOR, MAPK/Erk, Wnt oder immunbezogene Faktoren – besonders aktiv oder abgeschaltet waren. Viele der gemessenen Proteine sind direkte Ziele bereits verfügbarer Medikamente oder liegen unmittelbar stromabwärts solcher Ziele, sodass das Team ableiten konnte, welche Wirkstoffe wahrscheinlich die wichtigsten Wachstumstreiber eines Tumors stören würden. In drei Vierteln der retrospektiven Fälle konnten sie auf ein oder mehrere Wege hinweisen, die vermutlich das Tumorwachstum antrieben. Sie identifizierten außerdem Tumoren mit ausgeprägten Immunzellmarkern, was auf „heiße“ Tumoren hindeutet, die auf Immuntherapie ansprechen könnten, sowie ungewöhnliche Fälle mit auffällig einzigartigen Signaturen.
Anwendung der Methode bei realen Patientinnen und Patienten
Um die Nützlichkeit in der klinischen Praxis zu prüfen, wandten die Forschenden DigiWest anschließend auf frische Nadelbiopsien von 14 Patientinnen und Patienten mit verschiedenen gastrointestinalen Tumoren an, deren Fälle in einem Molecular Tumor Board diskutiert wurden. Diese Patientinnen und Patienten hatten komplexe Krankheitsverläufe und häufig vorherige Therapien. Da kein passendes gesundes Gewebe verfügbar war, wurden die Proteinlevel jedes Tumors mit dem Median der Gruppe verglichen, um abnorm hohe oder niedrige Werte zu definieren. Selbst unter dieser strengeren Bedingung zeigten 12 der 14 Tumoren klare, therapierelevante Muster der Signalwegaktivität. In zwei ausführlichen Fällen bestätigten die Proteindaten eine DNA‑Verstärkung des FGFR2‑Gens in einem Darmtumor und den Verlust einer mTOR‑Bremse in einem Lebertumor, was die Überlegung des Boards für FGFR‑blockierende bzw. mTOR‑blockierende Medikamente stark unterstützte. Insgesamt stimmten die DigiWest‑Befunde mit wichtigen genetischen Treibern überein und wiesen in den meisten auswertbaren Fällen auf mögliche Wirkstoffziele hin.
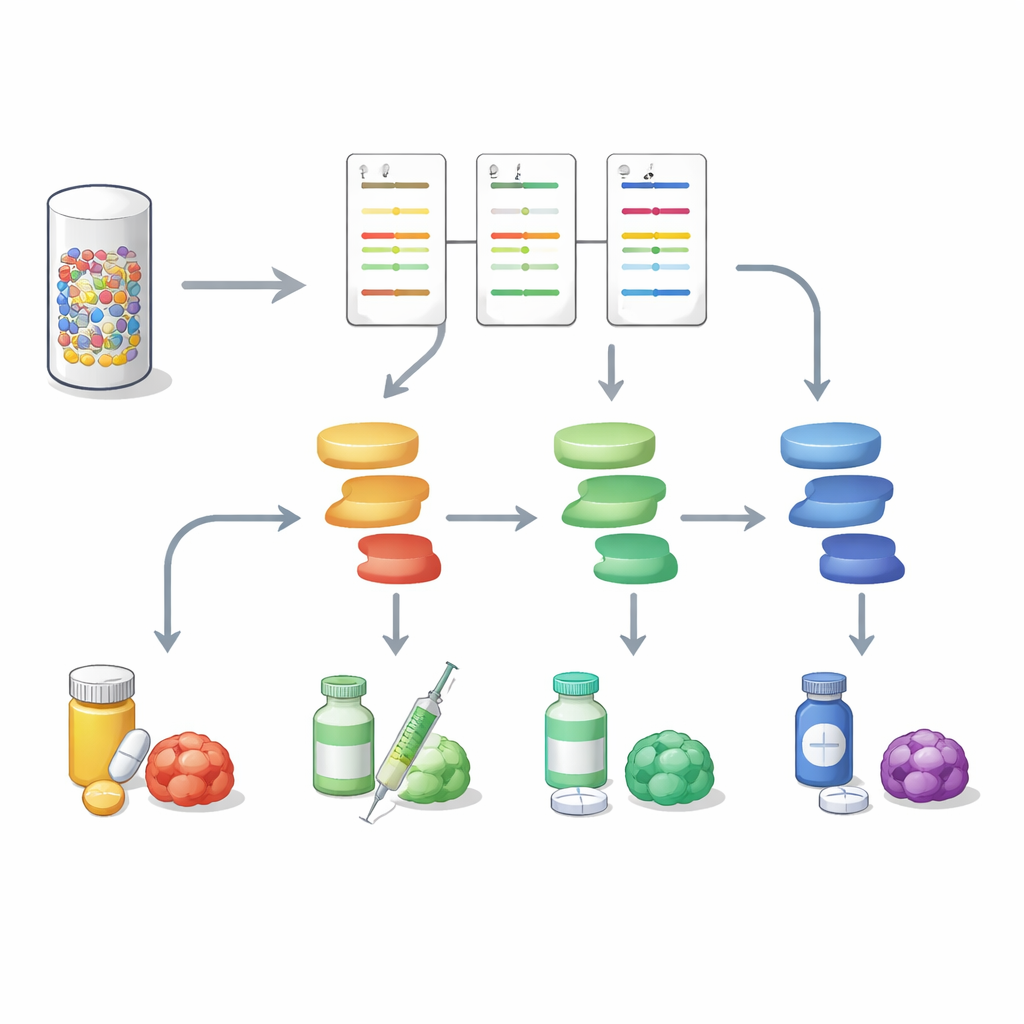
Auf dem Weg zu vollständigeren Tumorporträts
Die Arbeit zeigt, dass die Analyse von Proteinsignalen parallel zur DNA‑Sequenzierung ein reichhaltigeres und besser nutzbares Bild gastrointestinaler Tumoren liefern kann. Indem eine winzige Biopsie in eine Multi‑Pathway‑Aktivitätskarte verwandelt wird, hilft DigiWest zu unterscheiden, welche molekularen Schalter in einem bestimmten Tumor tatsächlich eingeschaltet sind und welche Medikamente sie am besten treffen könnten; außerdem kann die Methode aufkommende Resistenzwege anzeigen. Obwohl noch größere Studien nötig sind, bietet der Ansatz einen praktischen Weg, hochinformative Proteinprofile in die routinemäßige Präzisionsonkologie zu integrieren und Behandlungskonzepte zu ermöglichen, die sich am lebenden Tumor der Patientin bzw. des Patienten orientieren und nicht nur an dessen genetischer Blaupause.
Zitation: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Schlüsselwörter: präzisionsonkologie, gastrointestinale Tumore, Proteomik, Biopsieprofiling, targeted therapy