Clear Sky Science · de
Ein hybrides Dual‑Stream‑CNN‑Framework mit dynamischer Datenaugmentation und verbessertem Manta‑Ray‑Foraging‑Optimizer für robuste Glaukom‑Erkennung
Warum diese Forschung für Ihr Sehvermögen wichtig ist
Glaukom ist ein stiller Dieb des Sehens: Es schädigt den Sehnerv schrittweise ohne deutliche Symptome, sodass Sehverluste oft dauerhaft werden, bevor sie bemerkt werden. Regelmäßige Augenuntersuchungen können die Krankheit früh erkennen, doch das korrekte Auswerten von Netzhautbildern erfordert Zeit, teure Geräte und erfahrene Ärztinnen und Ärzte. Diese Arbeit stellt ein System der künstlichen Intelligenz (KI) vor, das als schneller, verlässlicher Assistent für Mediziner gedacht ist und Glaukome in üblichen Augenaufnahmen mit einer Genauigkeit erkennt, die mit aktuellen Methoden mithält und in manchen Tests sogar darüber hinausgeht.
Das Problem einer leisen Augenerkrankung
Glaukom betrifft weltweit zig Millionen Menschen und ist eine der Hauptursachen für irreversible Erblindung. Die Krankheit verändert allmählich das Erscheinungsbild des Sehnervenkopfs — der Stelle, an der Nervenfasern das Auge verlassen — und verändert dabei die relative Größe und Form der zentralen „Tasse“ innerhalb der Sehnervenpapille und des umliegenden Nervengewebes. Heute stützen sich Kliniker auf eine Kombination von Tests, darunter Netzhautfotos, Gesichtsfeldprüfungen und Druckmessungen im Auge. Diese Methoden funktionieren, sind aber arbeitsintensiv, stark von der Interpretation durch Spezialisten abhängig und können von Klinik zu Klinik oder Beobachter zu Beobachter variieren. Gleichzeitig werden in der Routineversorgung große Mengen an Augenbildern erfasst, was eine natürliche Chance für automatisierte Werkzeuge bietet, die risikobehaftete Fälle frühzeitig markieren könnten.
Einem Computer beibringen, Augenfotos zu lesen
Um ein solches Werkzeug zu entwickeln, verwenden die Autorinnen und Autoren Farbfundusaufnahmen — Standardbilder des Augenhintergrunds — aus vier öffentlichen Glaukom‑Datensätzen. Zunächst durchläuft jedes Bild eine sorgfältige Bereinigungspipeline: Rauschen wird geglättet, Helligkeit und Kontrast werden vereinheitlicht und störende schwarze Ränder entfernt. Eine Clustering‑Methode isoliert dann die Region um Papille und Tasse, die ausgeschnitten und skaliert wird, sodass jedes Bild den informativsten Bereich einheitlich darstellt. Dieser Schritt stellt sicher, dass die KI sich auf die Strukturen konzentriert, die Augenärztinnen und -ärzte tatsächlich zur Beurteilung des Glaukoms nutzen, statt auf irrelevante Hintergrunddetails.
Das Beste aus begrenzten und unordentlichen Daten machen
Eine große Herausforderung in der medizinischen Bildgebung ist, dass wirklich erkrankte Fälle im Vergleich zu normalen seltener sind und reale Bilder in Schärfe, Beleuchtung und Kameratyp variieren. Um dem zu begegnen, entwerfen die Autorinnen und Autoren eine "hybride Datenaugmentations"‑Strategie. Sie erzeugen realistische Varianten jedes Bildes durch Drehen, Verschieben, Zoomen und Spiegeln, ähnlich wie wenn dasselbe Augenfoto aus leicht unterschiedlichen Positionen aufgenommen würde. Darüber hinaus fügen sie eine abgestimmte Menge sanften visuellen Rauschens hinzu, berechnet aus der Helligkeit und dem Kontrast jedes Bildes, um die Unvollkommenheiten der klinischen Alltagsbildgebung zu simulieren. Diese kontrollierte Vielfalt hilft der KI, Glaukom über ein breites Spektrum von Bedingungen hinweg zu erkennen, statt sich auf einen engen, idealisierten Datensatz zu überanpassen. 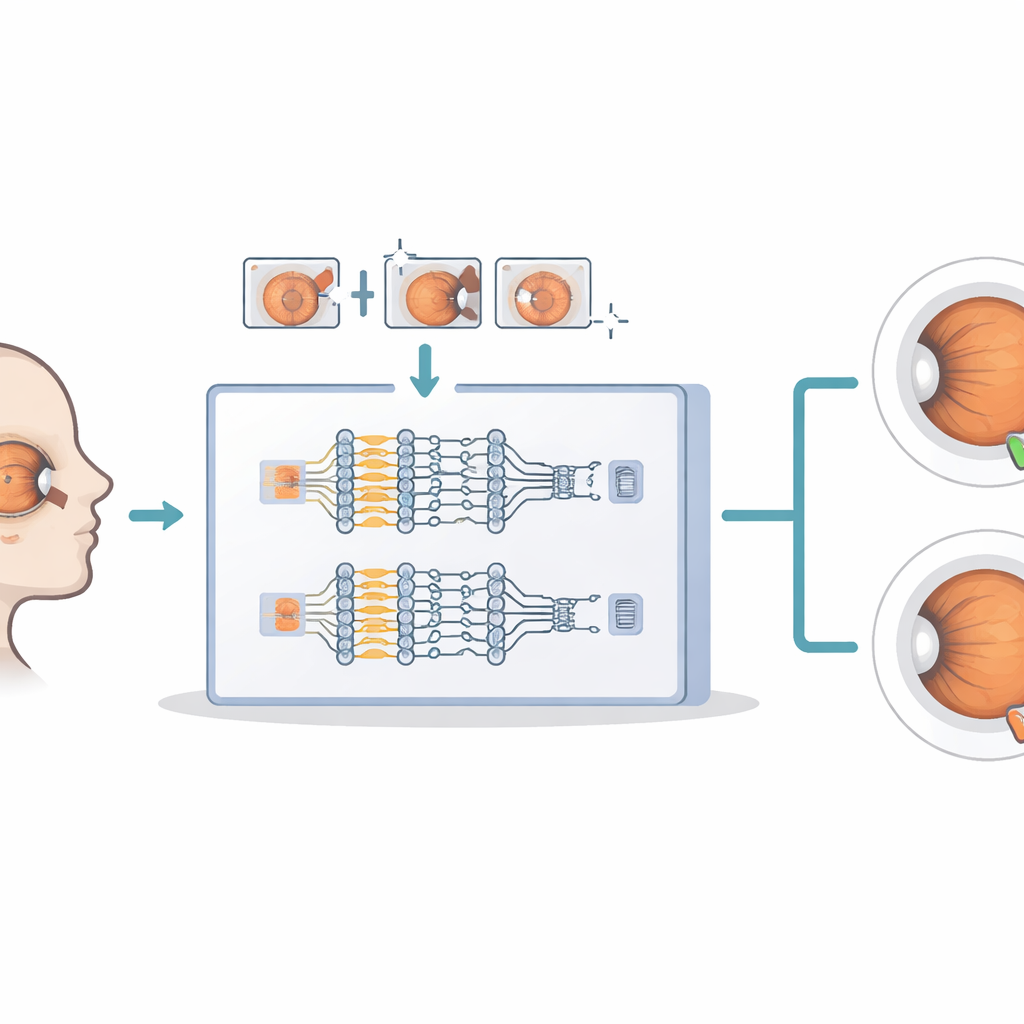
Zwei Expertenblicke und ein fokussierter Blick
Im Kern des Systems steht ein Dual‑Stream‑Deep‑Learning‑Design, das wie zwei komplementäre Spezialisten dieselbe Augenaufnahme untersucht. Ein Stream, basierend auf einem Netzwerk namens DenseNet121, konzentriert sich auf großskalige Strukturen: die Kontur der Papille, Form und Größe der Tasse und allgemeine Deformationen des Gewebes. Der andere Stream, basierend auf ResNet50, betrachtet feine Texturen: subtile Muster in der Nervenfaserschicht und kleine Unregelmäßigkeiten, die frühe Schäden signalisieren können. Ein leichtes "Attention"‑Mechanismus fungiert dann wie ein Scheinwerfer, der automatisch Bildmerkmale hervorhebt, die für das Glaukom am aussagekräftigsten sind, und solche dämpft, die repetitiv oder irrelevant sind. Die beiden angereicherten Blickwinkel werden schließlich verschmolzen und an einen einfachen Klassifikator übergeben, der ausgibt, ob das Bild glaukomatös oder gesund ist.
Die Feinabstimmung von der Natur leiten lassen
Die besten Einstellungen für ein solches System zu finden — wie stark Bilder zu drehen sind, welche Lernrate verwendet wird, wie viele Schichten nachtrainiert werden — ist normalerweise ein mühsames Trial‑and‑Error. Hier übergeben die Autorinnen und Autoren diese Aufgabe an eine Optimierungs‑Methode, die von der Nahrungssuche von Mantarochen im Ozean inspiriert ist. Dieser Algorithmus erkundet verschiedene Kombinationen von Trainingsparametern, springt gelegentlich zu "entgegengesetzten" Lösungen, um unproduktive Regionen zu verlassen, und konvergiert schrittweise auf Kombinationen, die die genauesten Glaukom‑Vorhersagen liefern. Indem diese Suche eng an die Validierungsleistung gekoppelt ist, findet das System einen Sweet Spot, der Genauigkeit, Robustheit und Rechenzeit ohne manuelle Feinabstimmung ausbalanciert. 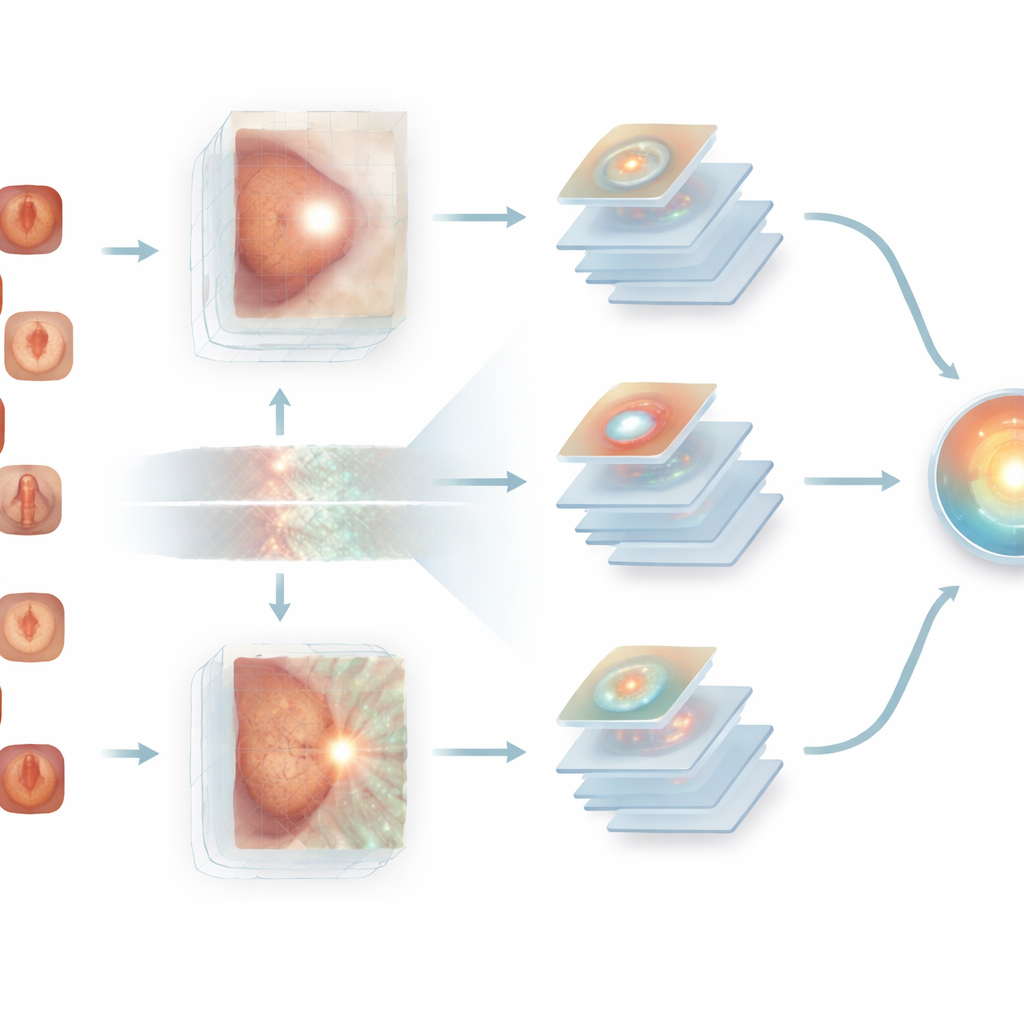
Wie gut funktioniert es wirklich?
Das Framework wurde auf vier häufig verwendeten Datensätzen getestet — ACRIMA, Drishti‑Gs, ORIGA und RIM‑ONE‑DL — und umfasst Hunderte von Netzhautbildern, die von Expertinnen und Experten annotiert wurden. Über diese Sammlungen hinweg erzielt das Modell auffallend hohe Werte: In einigen Fällen unterscheidet es glaukomatöse von normalen Augen in jedem einzelnen Testbild korrekt, mit nahezu keinen Fehlalarmen oder übersehenen Fällen und mit Fehlerwerten nahe null. Sorgfältige Ablationsstudien zeigen, dass jede Komponente beiträgt: Die hybride Augmentation verbessert die Generalisierung, Attention schärft den Fokus auf kritische Bereiche, und der manta‑ray‑basierte Optimierer bringt den letzten Schub hin zu nahezu perfekter Leistung.
Was das für die zukünftige Augenversorgung bedeutet
Für eine interessierte Leserschaft ist die zentrale Botschaft, dass diese Forschung uns näher an KI‑Werkzeuge bringt, die routinemäßige Augenfotos im Hintergrund still überwachen und Patienten hervorheben können, die vor ihrem eigenen Wahrnehmen eine dringende Untersuchung benötigen. Das vorgeschlagene System ersetzt nicht die Augenärztinnen und -ärzte, kann aber als unermüdlicher Assistent dienen, besonders in Kliniken mit begrenztem Zugang zu Spezialisten. Mit weiteren Tests an breiteren Patientengruppen und der Integration in schlanke Software oder tragbare Geräte könnten solche Dual‑Stream‑, Attention‑gestützten KI‑Systeme eine frühere, konsistentere Glaukom‑Screening‑Praxis unterstützen und dazu beitragen, das Sehvermögen von Millionen Menschen weltweit zu bewahren.
Zitation: Atia, A., Abdel-kader, H., Abo-Seida, O.M. et al. A hybrid dual-stream CNN framework with dynamic data augmentation and improved Manta Ray Foraging Optimization for robust glaucoma detection. Sci Rep 16, 12701 (2026). https://doi.org/10.1038/s41598-026-45384-6
Schlüsselwörter: Glaukom‑Screening, Retina‑Bildgebung, Deep Learning, medizinische KI, Sehnerv