Clear Sky Science · de
Multiparametrischer interferometrischer Reflektanz‑Bildsensor
Warum es wichtig ist, wenn Moleküle zusammenhaften
Viele medizinische Tests und neue Medikamente hängen davon ab, wie stark zwei Moleküle aneinander haften — etwa ein Wirkstoff an sein Ziel oder ein Virus an ein Antikörpermolekül. Heutige Instrumente können diese Bindung in Echtzeit ohne fluoreszierende Marker beobachten, verwechseln aber oft echte molekulare Bindung mit Hintergrundänderungen in der Lösung, etwa durch Temperatur‑ oder Salzgehaltsverschiebungen. Diese Arbeit stellt einen verbesserten optischen Sensor vor, der echte Bindung von solchen Störungen trennt und so Messungen genauer, einfacher und besser skalierbar macht.
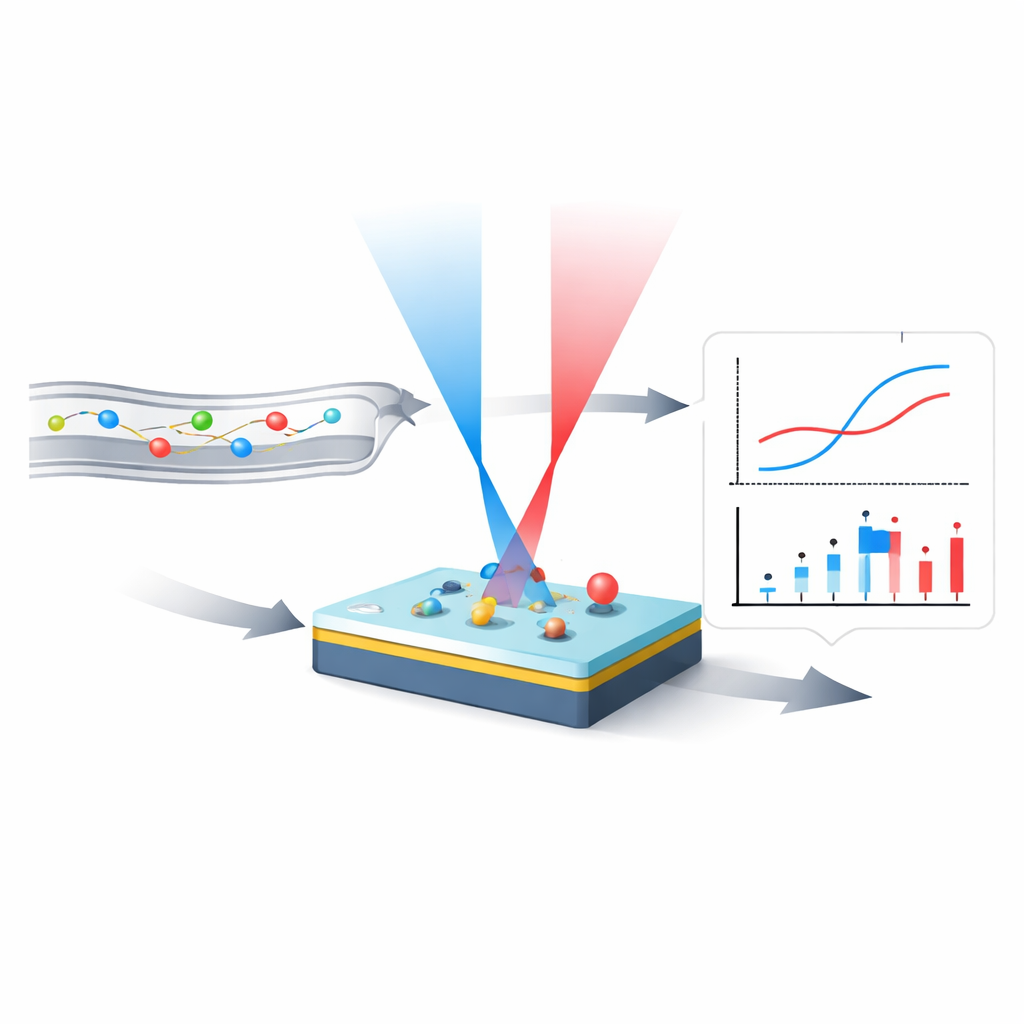
Kleine Änderungen mit reflektiertem Licht sichtbar machen
Die Arbeit baut auf einer bestehenden Technologie auf, dem interferometrischen Reflektanz‑Bildsensor, kurz IRIS. Bei IRIS ist ein Siliziumchip mit einer sehr dünnen transparenten Schicht überzogen, deren Dicke bekannt ist. Auf der Oberfläche sind in kleinen Flecken spezifische „Fang“-Moleküle befestigt. Wenn Zielmoleküle aus einer strömenden Lösung an diese Flecken binden, erhöhen sie die effektive Schichtdicke geringfügig. Durch Beleuchten dieser geschichteten Oberfläche und Aufzeichnen der reflektierten Intensität kann IRIS Änderungen des Rückstreusignals in Änderungen der scheinbaren Dicke übersetzen und daraus die Menge an gebundenem Material in jedem Fleck bestimmen — ganz ohne molekulare Marker.
Echte Signale von Hintergrundverschiebungen trennen
Viele andere optische Sensoren nutzen ein evaneszentes Feld, das nur die unmittelbare Umgebung über einer Metallfolie abtastet. In solchen Systemen sieht jede Änderung in der Nähe der Oberfläche — einschließlich Temperatur‑ oder Salzkonzentrationsänderungen oder Zusatzstoffe wie Dimethylsulfoxid (DMSO) — ähnlich aus wie echte Bindung, was als „Bulk‑Effekt“ bezeichnet wird. IRIS ist gegenüber solchen Lösungseffekten weniger empfindlich, aber nicht vollständig immun. Die Autoren stellen eine multiparametrische Version von IRIS (MP‑IRIS) vor, die nicht nur das Signal der Flecken liest, sondern auch gezielt ausgewählte Referenzflächen auswertet. Indem sie verfolgt, wie sich die Oberflächenantwort verändert, wenn sich die Zusammensetzung der Flüssigkeit ändert, kann das System den Bulk‑Effekt mathematisch in Echtzeit weitgehend entfernen. Experimente, bei denen die DMSO‑Konzentration absichtlich variiert wurde, zeigten, dass das korrigierte MP‑IRIS‑Signal den Bulk‑Fehler auf etwa 3 Pikogramm pro Quadratzentimeter reduzierte — in etwa die Größenordnung von wenigen Teilen pro Milliarde einer dünnen Molekülschicht und weit unter dem, was üblicherweise in kommerziellen Geräten beobachtet wird.

Mit zwei Lichtfarben für robuste Messungen
Während einfarbiges MP‑IRIS bereits Hintergrundeffekte unterdrückt, geht es dabei davon aus, dass die dünne Schicht auf dem Chip eine sehr genaue Anfangsdicke hat. In der Praxis treten durch Chipfertigung und chemische Oberflächenbehandlungen kleine Variationen auf, die absolute Messungen der gebundenen Menge verfälschen können. Um dem entgegenzuwirken, führen die Autoren eine zweite Lichtwellenlänge ein. Eine Farbe wird so gewählt, dass das reflektierte Signal stark auf Dickenänderungen reagiert, während die andere an einem Punkt liegt, an dem ihre Reflexion kaum mit der Dicke variiert, aber dennoch die optischen Eigenschaften der umgebenden Lösung erfasst. Durch die Kombination der Messungen beider Farben kann das System seine eigene Empfindlichkeit kontinuierlich abschätzen, Chip‑zu‑Chip‑Unterschiede korrigieren und gleichzeitig Bulk‑Effekte entfernen. Tests mit gezielten Variationen in der Proteinbeschichtung zeigten, dass das zwei‑farbige MP‑IRIS Messfehler in der Bindungsbestimmung unter etwa 10 % hielt, während ein einfacherer Ansatz dieselbe Bindung um bis zu 60 % falsch einschätzte.
Den Sensor mit DNA in Anwendung bringen
Um den biologischen Praxisnutzen zu demonstrieren, führte das Team DNA‑Hybridisierungsexperimente durch. Sie druckten winzige Arrays eines Proteins, das Biotin bindet, und befestigten kurze biotinmarkierte DNA‑Stränge an einigen dieser Flecken. Als komplementäre DNA‑Lösungen über den Chip gespült wurden, zeichnete MP‑IRIS für Dutzende von Flecken gleichzeitig auf, wie die scheinbare Dicke anstieg, während sich die Stränge fanden und banden, und wie sie sich veränderte, als wieder eine Lösung ohne DNA eingeführt wurde. Diese Tests bestätigten, dass der Sensor Bindung und Ablösung in Echtzeit an mehreren Stellen verfolgen kann, während er Änderungen der Pufferzusammensetzung und Unterschiede in der Aufbringungsdichte der Flecken korrigiert.
Was das für künftige Tests bedeutet
Alltäglich gesprochen gibt das neue MP‑IRIS‑Design Wissenschaftlern ein schärferes Augenpaar, um Molekülinteraktionen zu beobachten. Durch intelligente Vergleiche zwischen verschiedenen Regionen auf dem Chip und zwischen zwei Lichtfarben subtrahiert das System weitgehend das „Hintergrundrauschen“, das durch die Flüssigkeit selbst und durch kleine Unterschiede zwischen Chips entsteht. Das erleichtert den Vergleich von Ergebnissen über Experimente und Labore hinweg und ebnet den Weg für zuverlässige, kennzeichnungsfreie Tests für kleine Moleküle, DNA, Proteine und möglicherweise sogar Viren mit einfacherer und besser skalierbarer Hardware. Weitere Arbeiten werden untersuchen, wie die Methode in einem breiteren Spektrum realer diagnostischer und Wirkstoffscreening‑Anwendungen performt.
Zitation: Aslan, M., Snekvik, S., Seymour, E. et al. Multi-parametric interferometric reflectance imaging sensor. Sci Rep 16, 10780 (2026). https://doi.org/10.1038/s41598-026-45282-x
Schlüsselwörter: kennzeichnungsfreie Biosensorik, Bindungskinetik, optische Interferometrie, Korrektur von Bulk‑Effekten, DNA‑Hybridisierung