Clear Sky Science · de
PSD-LW-DCN: ein generalisierbares, leistungsspektrumsbasiertes, leichtgewichtiges tiefes Faltungsneuronales Netz zur Erkennung von Anfällen
Intelligenteres Anfallsmonitoring, das praktikabel wird
Für Menschen mit Epilepsie verschwindet die Angst vor einem unerwarteten Anfall selten vollständig. Ärztinnen und Ärzte nutzen Gehirnwellenmessungen, sogenannte EEGs, um Anfälle zu erkennen, doch das Durchsehen von Stunden voller Zickzacklinien per Auge ist langsam und ermüdend. Diese Studie stellt ein kompaktes Computermodell vor, das Anfälle in EEG-Aufzeichnungen nahezu in Echtzeit automatisch markieren kann — selbst bei Patientinnen und Patienten, die dem System unbekannt sind — und das zugleich leichtgewichtig genug ist, um auf Alltagsgeräten und künftigen Wearables zu laufen.
Warum das Lesen von Gehirnwellen so schwer ist
EEG misst winzige elektrische Signale von der Kopfhaut, wenn Gehirnzellen feuern. Während eines Anfalls verändern sich diese Signale auf komplexe Weise, die von Person zu Person, zwischen Anfallsarten und sogar über die Zeit bei derselben Patientin oder demselben Patienten variieren. Klassischerweise suchen Expertinnen und Experten manuell nach subtilen Mustern — ein Verfahren, das langsam, subjektiv und schwer reproduzierbar ist. Viele Computerprogramme wurden vorgeschlagen, um zu helfen, doch sie tun sich oft schwer, wenn sie an neuen Patientinnen und Patienten getestet werden, deren Gehirnaktivität anders ist als die der Trainingspersonen. Andere Modelle sind so groß und energiehungrig, dass sie für kontinuierliches Monitoring außerhalb des Krankenhauses unpraktisch sind.
Dem Gehirn in verschiedenen Tonhöhen zuhören
Anstatt rohe EEG-Signale direkt in ein riesiges neuronales Netz zu füttern, nutzen die Autorinnen und Autoren eine klassische Idee aus der Signalverarbeitung: sie betrachten, wie sich die Energie des Signals über verschiedene „Tonhöhen“ bzw. Frequenzbänder verteilt. Sie teilen jedes EEG-Segment in fünf bekannte Bereiche auf, von langsamen Wellen bis zu schnelleren Rhythmen. Für jedes Band berechnen sie, wie viel Energie die Aktivität bei jeder Frequenz hat, mithilfe einer sorgfältigen Mittelungsmethode, die zufälliges Rauschen reduziert. Anschließend mitteln sie diese Energiewerte über alle Aufzeichnungskanäle, wodurch viele einzelne Zickzacklinien in ein einziges, saubereres Profil verwandelt werden, das hervorhebt, wie sich die Gesamtaktivität des Gehirns zwischen Normal- und Anfallzuständen verschiebt.
Ein kleines, aber cleveres neuronales Netz
Diese kompakten Energieprofile werden in ein speziell entworfenes Deep-Learning-Modell eingespeist, das die Autorinnen und Autoren PSD-LW-DCN nennen. Anders als viele tiefe Netze mit Dutzenden von Schichten und Millionen frei verstellbarer Gewichte verwendet dieses Modell nur zwei schlanke Faltungsstufen gefolgt von einfachen Entscheidungsschichten und kommt so auf insgesamt etwa sechzigtausend Parameter. Die erste Stufe sucht nach detaillierten Mustern in den Energieprofilen; die zweite Stufe verdichtet diese zu niederdimensionalen Zusammenfassungen, die dennoch die wesentlichen Unterschiede zwischen Anfalls- und Nicht-Anfallsphasen bewahren. Indem das Netz auf bereits vereinfachten Eingaben arbeitet und komplexe räumliche Verknüpfungen über Elektroden vermeidet, bleibt es klein, schnell und leichter auf moderater Hardware einsetzbar.
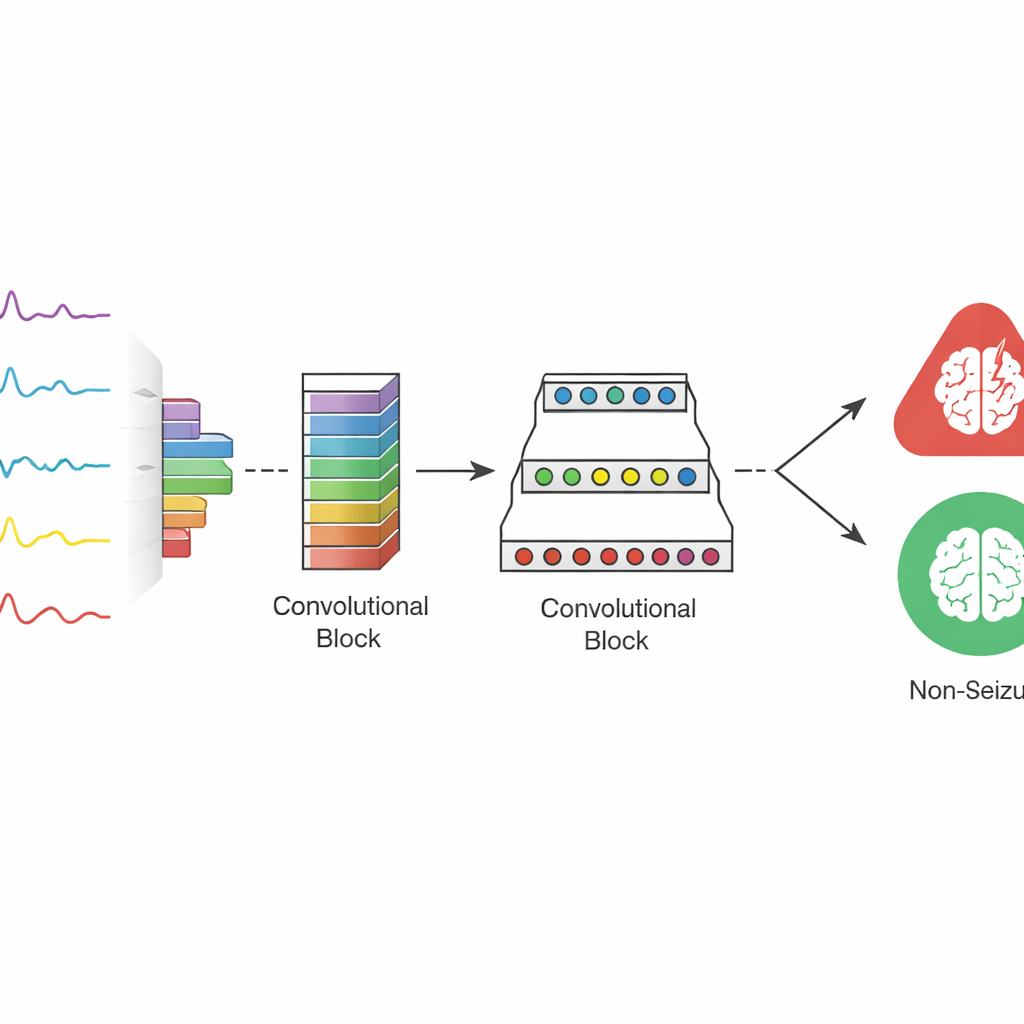
Wie gut funktioniert es bei realen Patientinnen und Patienten?
Das Team testete seinen Ansatz an zwei der größten öffentlichen EEG-Datensammlungen für Epilepsie, die jeweils Aufzeichnungen vieler verschiedener Patientinnen und Patienten und Tausende von Anfällen enthalten. Sie trainierten das Modell mit einer Leave-One-Person-Out-Strategie: in jeder Runde wurden alle bis auf eine Person zum Lernen verwendet, und die ausgesparte Person diente als Test, um zu prüfen, wie gut die Methode auf neue Personen generalisiert. In beiden Datensätzen klassifizierte das Modell etwa vier von fünf EEG-Segmenten korrekt und hielt die Rate falscher Alarme niedrig, oft unter einer Fehlalarmmeldung pro Stunde in langen Monitoring-Sitzungen. Im direkten Vergleich mit einer Reihe moderner Deep-Learning-Methoden, darunter auf Aufmerksamkeit beruhende Netze und Transformer-Modelle, erreichte dieses kompakte Design eine gleichwertige oder bessere Genauigkeit, lief dabei mehrere Male schneller und benötigte nur einen Bruchteil des Speichers.
Was die Energienmuster verraten
Um zu prüfen, ob das Modell sinnvolle Gehirnveränderungen erkennt und nicht nur die Daten auswendig lernt, untersuchten die Forscherinnen und Forscher, wie sich die Energie in verschiedenen Frequenzbändern bei Patientinnen und Patienten mit guter bzw. schlechter Erkennungsleistung verhielt. In vielen gut erkannten Fällen zeigten die Anfallsphasen deutliche Energieanstiege in bestimmten Bändern, besonders im sogenannten Theta-Bereich, verglichen mit ruhigen Interiktalphasen. In schwierigeren Fällen waren diese Energiedifferenzen schwächer oder sogar umgekehrt, was erklärt, warum einige Personen für automatisierte Systeme herausfordernd bleiben. Zusätzliche Tests zeigten, dass die Kombination mehrerer Frequenzbänder bessere Ergebnisse lieferte als die Nutzung eines einzelnen Bandes, was den Wert unterstreicht, das gesamte Spektrum der Gehirnrhythmen zu betrachten.
Kontinuierliches Monitoring näher an den Alltag bringen
Insgesamt zeigt diese Arbeit, dass ein sorgfältig gestaltetes, leichtgewichtiges Modell Anfälle in EEG-Aufzeichnungen vieler verschiedener Personen zuverlässig erkennen kann und dabei schnell genug läuft, um in Echtzeit auf energieeffizienten Geräten eingesetzt zu werden. Indem komplexe Gehirnsignale zuerst in kompakte Energie-Fingerabdrücke überführt und dann mit einem moderaten neuronalen Netz analysiert werden, findet der Ansatz ein Gleichgewicht zwischen Genauigkeit, Geschwindigkeit und Einfachheit. Für Patientinnen, Patienten und Klinikerinnen und Kliniker rückt damit die Aussicht auf verlässlichere, weniger aufdringliche Anfallsüberwachung — möglicherweise über stationäre Geräte am Bett oder tragbare Systeme — ein Stück näher an die Alltagsrealität.
Zitation: Gu, P., Zhang, M., Xu, M. et al. PSD-LW-DCN: a generalizable power spectral density based lightweight deep convolutional neural network for seizure detection. Sci Rep 16, 14073 (2026). https://doi.org/10.1038/s41598-026-44536-y
Schlüsselwörter: Epilepsie, EEG, Anfallerkennung, Deep Learning, tragbares Monitoring