Clear Sky Science · de
Multimerin1 und nicht Galectin-8 dämpft WNT-Signalgebung, um die Differenzierung von Magengrundzellen zu fördern
Warum der Zeitpunkt der Magenzellreifung wichtig ist
Die Magenschleimhaut wird ständig erneuert von spezialisierten Zellen, die zur richtigen Zeit ausreifen müssen. Wird dieser Prozess gestört, kann das den Nährboden für Erkrankungen bilden, einschließlich Krebs. Diese Studie untersucht, wie Zellen, die winzige Blutgefäße im Mausmagen auskleiden, unauffällig die Reifung benachbarter Verdauungszellen steuern, und wie ein versteckter genetischer Fehler in einer verbreiteten Versuchsmäuselinie die Forschenden zu einem unerwarteten Akteur in diesem Prozess führte.
Eine Überraschung in einer bekannten Mäuselinie
Das Team begann mit der Untersuchung eines Proteins namens Galectin 8, das bestimmte Zuckermuster binden kann, die in risikobehafteten präkanzerösen Geweben im Darm vermehrt vorkommen. Weil eine gut bekannte Mäuselinie das Gen für Galectin 8 nicht besitzt, erwarteten die Forschenden, dass diese Linie aufzeigt, wie Galectin 8 einen wichtigen Magentyp, die sogenannten Grundzellen (chief cells), beeinflusst — Zellen, die Verdauungsenzyme produzieren. Im Vergleich zu normalen Mäusen zeigten die jungen Knockout-Mäuse eine deutliche Verzögerung in der Reifung der Grundzellen, erkennbar am verzögerten Auftreten spezifischer Marker, die voll entwickelte Verdauungszellen signalisieren.
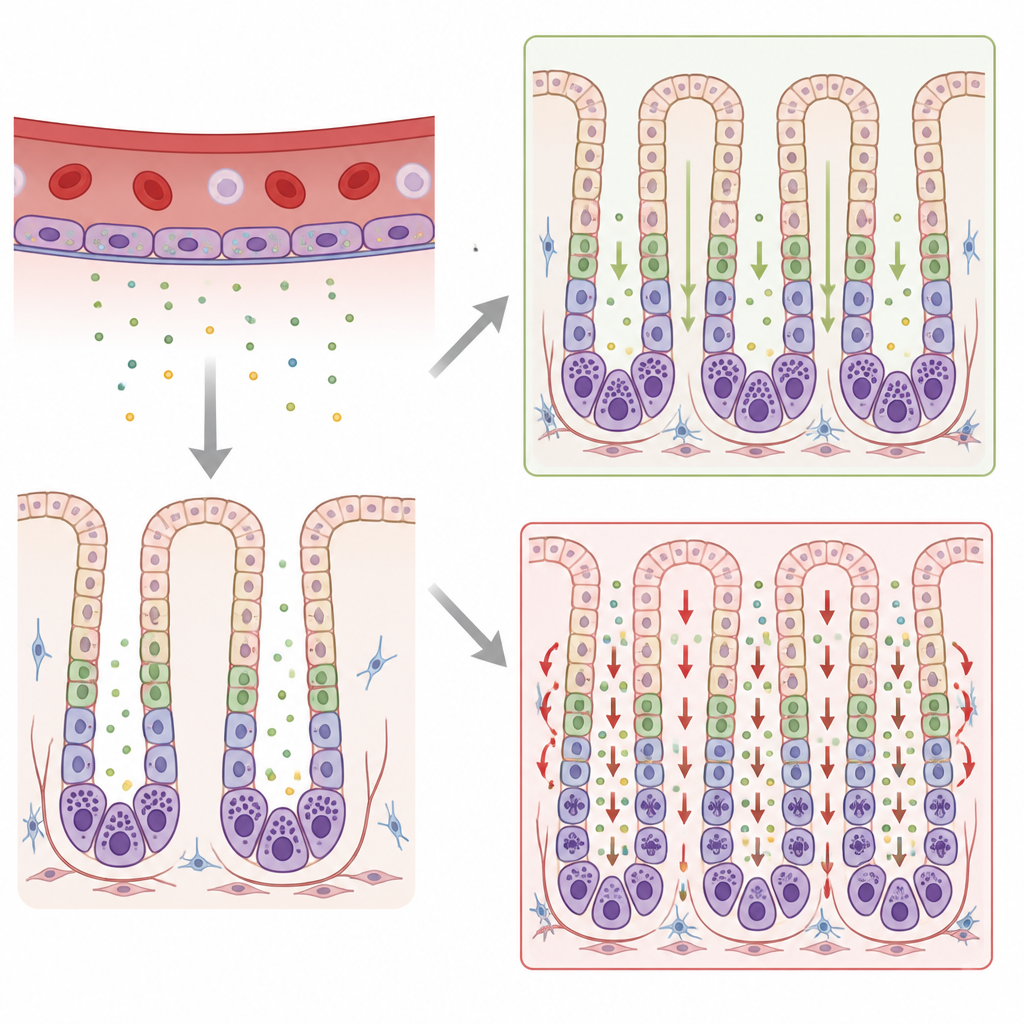
Den wahren Übeltäter eingrenzen
Auf den ersten Blick schien diese Verzögerung eine Rolle für Galectin 8 in der Magenentwicklung zu bestätigen. Weitere Analysen weckten jedoch Zweifel. Andere Magentypen, wie säureproduzierende Zellen und oberflächenbildende Zellen, wirkten normal. Einzelzell-RNA-Sequenzierung zeigte außerdem, dass das Galectin-8-Gen in den Grundzellen selbst gar nicht aktiv war, sondern in anderen Zelltypen. Bulk-RNA-Sequenzierung gefolgt von gezielten genetischen Tests förderte Überraschendes zutage: Die Galectin-8-Knockout-Linie trug außerdem eine bislang unerkannte Deletion von zwei benachbarten Genen auf einem anderen Chromosom, darunter eines namens Mmrn1, das für ein großes Gefäßprotein, Multimerin 1, kodiert.
Verknüpfte Gene trennen, um ihre Rollen zu testen
Um herauszufinden, welches fehlende Gen tatsächlich die Verzögerung der Grundzellreifung verursachte, kreuzten die Wissenschaftler die Mäuse so, dass die Galectin-8-Mutation vom Mmrn1-Deletion getrennt werden konnte. Bei Tieren, die nur Galectin 8 vermissten, aber normales Mmrn1 trugen, reiften die Grundzellen termingerecht, genau wie bei Standardmäusen. Im Gegensatz dazu zeigten Mäuse, denen Multimerin 1 (und ein zweites Gen, Alpha-Synuclein) fehlte, aber normales Galectin 8 hatten, weiterhin die verzögerte Reifung der Grundzellen. Alpha-Synuclein, vor allem für seine Rollen im Gehirn bekannt, war im Magen nicht nachweisbar, womit Multimerin 1 als wahrscheinlichster Auslöser des Effekts übrigbleibt.
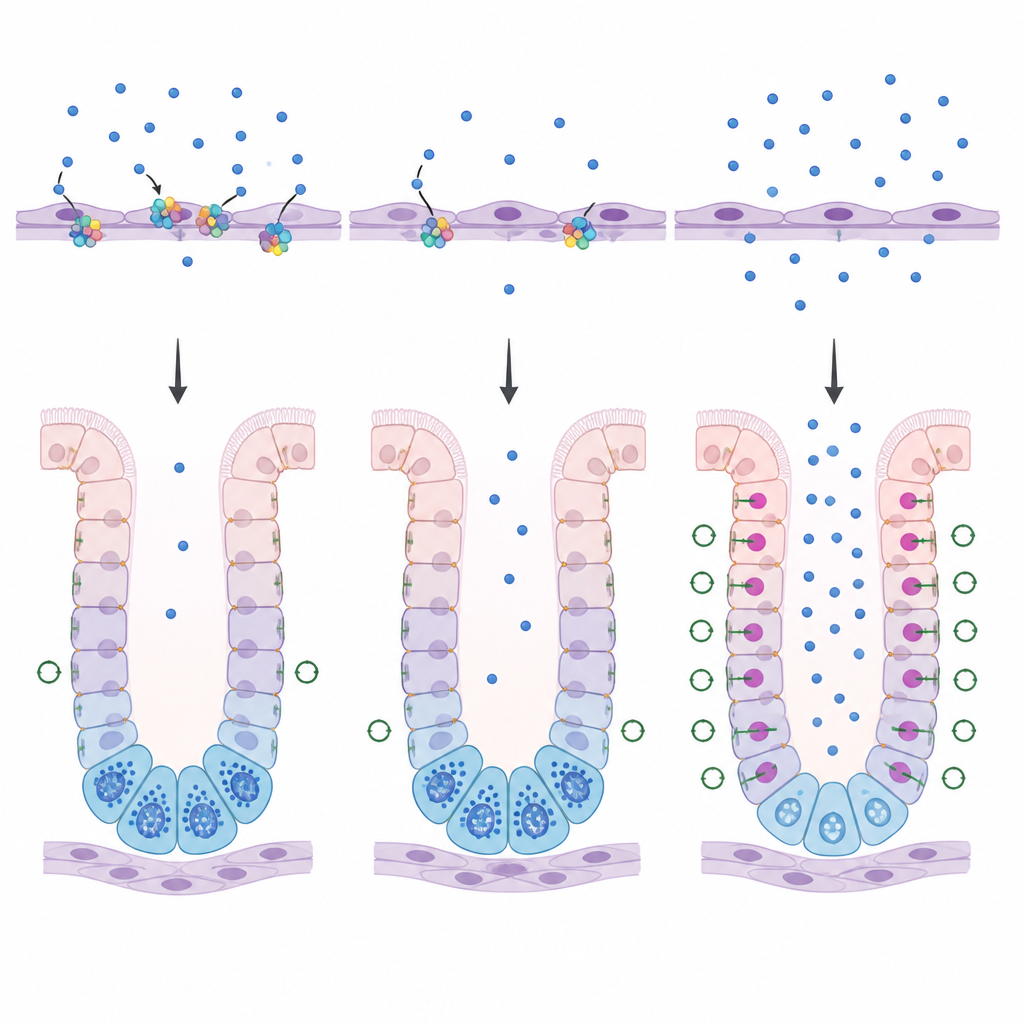
Wie Blutgefäßzellen das Magenwachstum steuern
Multimerin 1 wird von Zellen hergestellt, die Blutgefäße auskleiden, nicht von den Oberflächenzellen des Magens selbst. Frühere Arbeiten zu verwandten Proteinen legen nahe, dass sie die WNT-Signalgebung dämpfen können — ein starkes Wachstumssignal, das beeinflusst, wie Stammzellen ihr Schicksal bestimmen. Bei jungen Mäusen ohne Multimerin 1 beobachteten die Forschenden mehr Beta-Catenin in den Zellkernen der Magen-drüsenzellen und mehr Zellen in einem aktiven Teilungszustand, beides Hinweise auf erhöhte WNT-Aktivität. Mit zunehmendem Alter der Tiere ließ dieses Muster nach, was darauf hindeutet, dass andere Faktoren später die Aufgabe übernehmen, WNT zu begrenzen. Die Befunde deuten darauf hin, dass Multimerin 1 als eine Art Puffer wirkt, der WNT-Signale auf einem Level hält, das es den Grundzellen erlaubt, in einem kritischen frühen Zeitfenster richtig auszureifen.
Was das für Magengesundheit und Forschung bedeutet
Einfach ausgedrückt zeigt diese Studie, dass ein von Blutgefäßzellen freigesetztes Protein benachbarte Magenzellen dabei unterstützt, rechtzeitig „erwachsen“ zu werden, indem es ein starkes Wachstumssignal zügelt. Sie veranschaulicht auch, wie versteckte genetische Veränderungen in Versuchstieren Forschende in die Irre führen können, wenn es darum geht, welches Gen für einen bestimmten Befund verantwortlich ist. Die Autorinnen und Autoren schließen, dass Multimerin 1, nicht Galectin 8, die WNT-Signalgebung dämpft, um die normale Entwicklung der enzymproduzierenden Grundzellen im Mausenmagen zu fördern, und sie plädieren dafür, dass künftige Arbeiten mit saubereren genetischen Modellen nötig sind, um zu untersuchen, wie dieser Signalweg mit Metaplasie und Krebsrisiko verbunden sein könnte.
Zitation: Lin, X., Nicolazzi, G., Liu, X. et al. Multimerin1 and not Galectin-8 tempers WNT signaling to promote gastric chief cell differentiation. Sci Rep 16, 15011 (2026). https://doi.org/10.1038/s41598-026-43742-y
Schlüsselwörter: Magengrundzellen, WNT-Signalgebung, Multimerin 1, Magenreifung, Mausmagen