Clear Sky Science · de
Quantitative EEG-Signaturen von Leistungs- und funktionellen Konnektivitätsveränderungen bei Alzheimer-Krankheit und frontotemporaler Demenz
Warum Gehirnwellen für Gedächtnisverlust wichtig sind
Demenz betrifft Millionen von Familien, doch Ärztinnen und Ärzte haben weiterhin Schwierigkeiten, verschiedene Formen der Erkrankung frühzeitig voneinander zu unterscheiden. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Können wenige Minuten Gehirnwellenaufzeichnung, gemacht während einer ruhenden, augenverschlossenen Phase, verlässliche Hinweise liefern, die Alzheimer-Krankheit von frontotemporaler Demenz und von normaler Alterung unterscheiden? Durch genaue Messung der Stärke und der Koordination dieser Gehirnwellen wollen die Forschenden praktikable, kostengünstige Marker finden, die frühere und genauere Diagnosen unterstützen könnten.
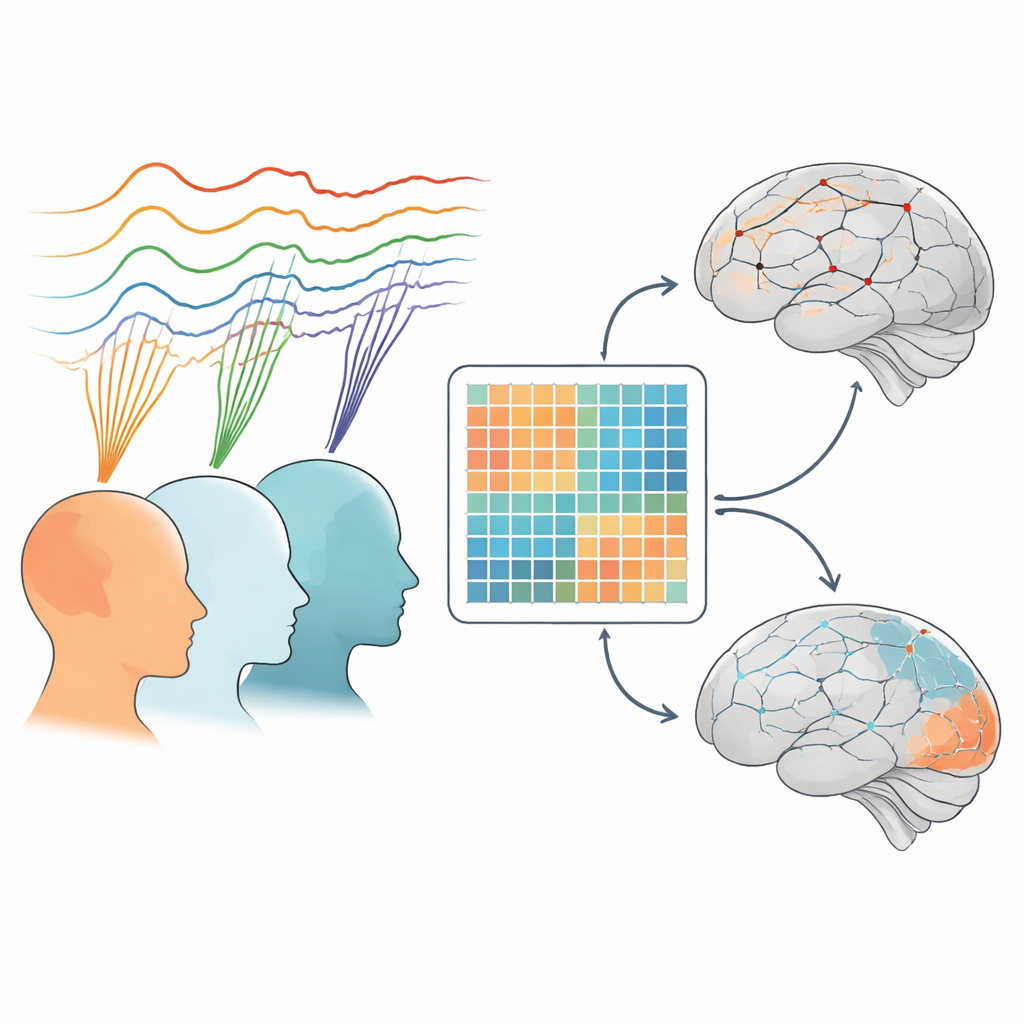
Zwei verbreitete, aber unterschiedliche Hirnerkrankungen
Alzheimer-Krankheit und frontotemporale Demenz führen beide zu einem allmählichen Verlust kognitiver Fähigkeiten, schädigen das Gehirn jedoch auf unterschiedliche Weise. Alzheimer trifft typischerweise gedächtnisrelevante Bereiche und äußert sich zuerst als Vergesslichkeit bei älteren Erwachsenen. Frontotemporale Demenz tritt häufiger im mittleren Lebensalter auf und verändert Persönlichkeit, Verhalten und Sprache, wenn frontale und temporale Hirnregionen degenerieren. Weil Symptome sich überschneiden können, fällt es Ärztinnen und Ärzten oft schwer, die zugrunde liegende Erkrankung zu bestimmen. Die Autorinnen und Autoren griffen zur Elektroenzephalographie (EEG) — einer nichtinvasiven Methode zur Aufzeichnung elektrischer Hirnaktivität — um zu prüfen, ob die „Rhythmen“ und Verbindungen der Gehirnwellen diese Zustände voneinander und von normaler Alterung trennen können.
Den verborgenen Rhythmen des Gehirns zuhören
Das Team analysierte einen offenen EEG-Datensatz von 88 Personen: 36 mit Alzheimer, 23 mit frontotemporaler Demenz und 29 kognitiv normalen älteren Erwachsenen. Alle lagen ruhig mit geschlossenen Augen, während 19 Sensoren auf der Kopfhaut die Hirnaktivität erfassten. Die Forschenden konzentrierten sich auf fünf bekannte Frequenzbänder — langsame Delta- und Theta-Wellen, mittleres Alpha sowie schnellere Beta- und Gamma-Wellen. Zuerst maßen sie, wie viel Leistung bzw. Stärke jede Wellenart in verschiedenen Hirnregionen wie Frontal-, Temporal-, Parietal- und Okzipitallappen hatte. Anschließend untersuchten sie, wie gut diese Bereiche „miteinander sprechen“, indem sie die Synchronisation der Wellen zwischen Sensormpaaren verfolgten. Mithilfe von Netzwerkanalysen fassten sie diese Verbindungen als Kantengewichte (einzelne Verbindungen) und Knotengewichte (gesamte Konnektivität einer Region) zusammen.
Muster der Hirnaktivität über dem Kopf
Ein deutliches Ergebnis war, dass gesunde ältere Erwachsene insgesamt stärkere Alpha-Wellen zeigten als sowohl die Alzheimer- als auch die frontotemporale-Demenz-Gruppen, besonders über temporalen und parietalen Regionen bei Alzheimer und über okzipitalen (Hinterkopf-)Regionen bei beiden Erkrankungen in Alpha- und Beta-Bändern. In gesunden Gehirnen verteilte sich die Leistung vielfältiger über Lappen und Frequenzen, was auf ein reichhaltiges, differenziertes Aktivitätsmuster hindeutet. Alzheimer-Gehirne zeigten eine ungleichmäßigere Mischung, mit relativ stärkeren langsamen Wellen und reduzierten schnellen Wellen in manchen Regionen, während frontotemporale Demenz ein gleichförmigeres, abgeflachtes Profil zeigte. Diese Unterschiede darin, wo und wie stark bestimmte Rhythmen auftreten — insbesondere in Delta-, Theta-, Alpha- und Gamma-Bändern — deuten darauf hin, dass die beiden Demenzen die Gehirnaktivität in unterschiedlichen räumlichen Mustern verändern, was bei der Klassifikation von Patientinnen und Patienten helfen könnte.
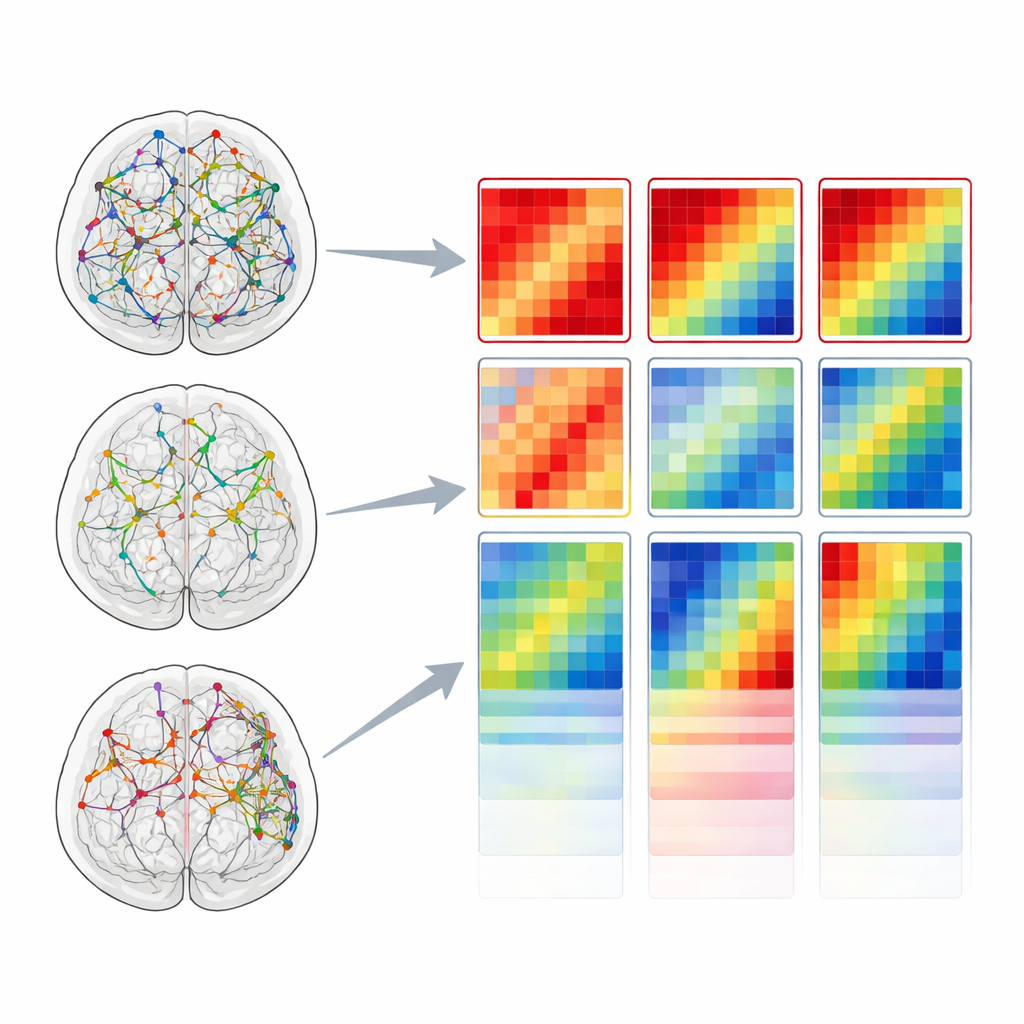
Wie Hirnregionen in Kontakt bleiben
Bei der Betrachtung der Konnektivität wurden die Kontraste noch deutlicher. Im Vergleich zu gesunden Erwachsenen zeigten Menschen mit Alzheimer schwächere Verbindungen zwischen vielen Hirnbereichspaaren über die meisten Frequenzbänder hinweg, was auf einen weitreichenden Zusammenbruch der Kommunikation hindeutet. Die frontotemporale Demenz zeigte ebenfalls reduzierte Konnektivität in den langsamen Delta- und Theta-Bändern, wies jedoch auffällig stärkere Verbindungen im Beta-Band auf als sowohl Alzheimer- als auch Kontrollgruppen. Betrachtet man spezifische Lappen, zeigte Alzheimer besonders reduzierte Konnektivität in frontalen und temporalen Regionen, während die frontotemporale Demenz ihre stärksten Störungen im Temporallappen aufwies, die frontalen Verbindungen jedoch relativ verschonte. Insgesamt lag die frontotemporale Demenz zwischen normaler Alterung und Alzheimer: deutlich beeinträchtigt, aber weniger global desynchronisiert als Alzheimer.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt legt die Studie nahe, dass kurze Ruhe-EEG-Aufnahmen eine doppelte Signatur der Demenz enthalten: Veränderungen in der Stärke zentraler Gehirnrhythmen und in der Koordination zwischen Hirnregionen. Alzheimer erscheint als Zustand mit abgeschwächter Alpha- und Beta-Leistung in bestimmten Regionen und weitreichendem Netzwerkkollaps, während die frontotemporale Demenz gleichmäßigere Leistungsänderungen und selektive, band-spezifische Verschiebungen in der Konnektivität zeigt, besonders im Temporallappen. Obwohl diese Ergebnisse in größeren und vielfältigeren Stichproben bestätigt werden müssen, deuten sie auf einfache, erschwingliche EEG-Maße hin, die Klinikerinnen und Klinikern helfen könnten, Demenztypen früher zu unterscheiden, weitere Untersuchungen zu steuern und letztlich eine gezieltere Versorgung zu unterstützen.
Zitation: Iqbal, S., Nisar, H. & Yeap, K.H. Quantitative EEG signatures of power and functional connectivity alterations in Alzheimer’s disease and frontotemporal dementia. Sci Rep 16, 12158 (2026). https://doi.org/10.1038/s41598-026-42452-9
Schlüsselwörter: Elektroenzephalographie, Alzheimer-Krankheit, frontotemporale Demenz, Gehirnkonnektivität, Biomarker