Clear Sky Science · de
IRX4204 macht multiples Myelom empfindlicher gegenüber Ferroptose und verbessert die Wirksamkeit von Lenalidomid über die HMOX1-GPX4-Achse
Warum diese Forschung wichtig ist
Multiples Myelom ist eine Krebserkrankung der im Knochenmark sitzenden, Antikörper produzierenden Zellen und bleibt für die meisten Patientinnen und Patienten unheilbar, vor allem weil Tumoren langfristig bestehenden Therapien ausweichen. Diese Studie untersucht eine neuerdings intensiv betrachtete Form des Zelltods, die Ferroptose—eine eisengetriebene Art des „Rostens“ innerhalb der Zelle—und zeigt, wie ein hochselektives experimentelles Präparat, IRX4204, Myelomzellen in diese Richtung drängen kann. Indem sie darlegen, wie IRX4204 die internen Abwehrmechanismen der Zelle umlenkt und Standardtherapien wie Lenalidomid wirksamer macht, eröffnet die Arbeit einen neuen Ansatz im Umgang mit medikamentenresistentem Myelom.
Ein neuer Weg, Krebszellen zu töten
Konventionelle Krebstherapien zielen häufig darauf ab, Apoptose auszulösen, eine geordnete, programmierte Form des Zelltods. Myelomzellen lernen jedoch oft, diesen Weg zu umgehen. Ferroptose bietet eine fundamental andere Route: Sie beruht auf Eisen und der Anreicherung zerstörerischer Lipide in Zellmembranen, was letztlich zum Zerfall der Zellen führt. Myelomzellen sind besonders auf Eisen angewiesen und produzieren große Mengen an Antikörpern, was sie unter ständigen oxidativen Stress stellt. Die Forschenden vermuteten, dass eine leichte Kippung dieses Gleichgewichts diese Zellen besonders anfällig für Ferroptose machen könnte, ohne normales Gewebe zu schädigen.
Das Medikament, das Zellen auf eisengetriebenen Tod vorbereitet
IRX4204 ist ein Aktivator der dritten Generation für Retinsäure-X-Rezeptoren (RXRs), Schaltstellen im Zellkern, die Gene steuern, die an Stoffwechsel und Stressantworten beteiligt sind. Die Forschenden behandelten mehrere Myelomzelllinien mit IRX4204 und stellten fest, dass es ihr Wachstum verlangsamte und die Empfindlichkeit gegenüber bekannten Ferroptose-induzierenden Verbindungen deutlich erhöhte. Ein schützendes Molekül namens Ferrostatin-1, das Ferroptose blockiert, rettete die Zellen größtenteils vor den toxischen Effekten von IRX4204. Das deutet darauf hin, dass das Medikament die Zellen nicht einfach vergiftete, sondern gezielt in die Ferroptose trieb. In Kombination mit Lenalidomid—einem weit verbreiteten Myelommedikament—wirkten beide Substanzen zusammen stärker, als jede für sich allein, und dieser Zusatznutzen hing ebenfalls von Ferroptose ab.
Wie die Stressmaschinerie der Zelle umprogrammiert wird
Bei der Aufschlüsselung des Mechanismus zeigten die Forschenden, dass IRX4204 die antioxidative Schutzschicht der Zelle angreift. Es senkt die Spiegel von GPX4 und SLC7A11, zwei Proteinen, die normalerweise verhindern, dass schädliche Lipide in Membranen akkumulieren. Gleichzeitig erhöht das Medikament das freie Eisen in den Zellen und fördert die Lipidperoxidation, eine Form oxidativer Schädigung, die eng mit Ferroptose verknüpft ist. Ein Schlüsselfaktor ist HMOX1, ein Enzym, das Häm abbaut und dabei Eisen freisetzt. Die Forschenden fanden, dass Myelomzellen, die Ferroptose-induzierenden Reizen ausgesetzt waren, das HMOX1-Gen hochfuhren, und dass höhere HMOX1-Spiegel in Patientenproben mit besserem Überleben assoziiert waren. Weiterhin zeigte sich, dass IRX4204 ein nukleares Rezeptorpaar, PPARα–RXRα, aktiviert, das direkt an die Kontrollregion des HMOX1-Gens bindet und dessen Aktivität erhöht.
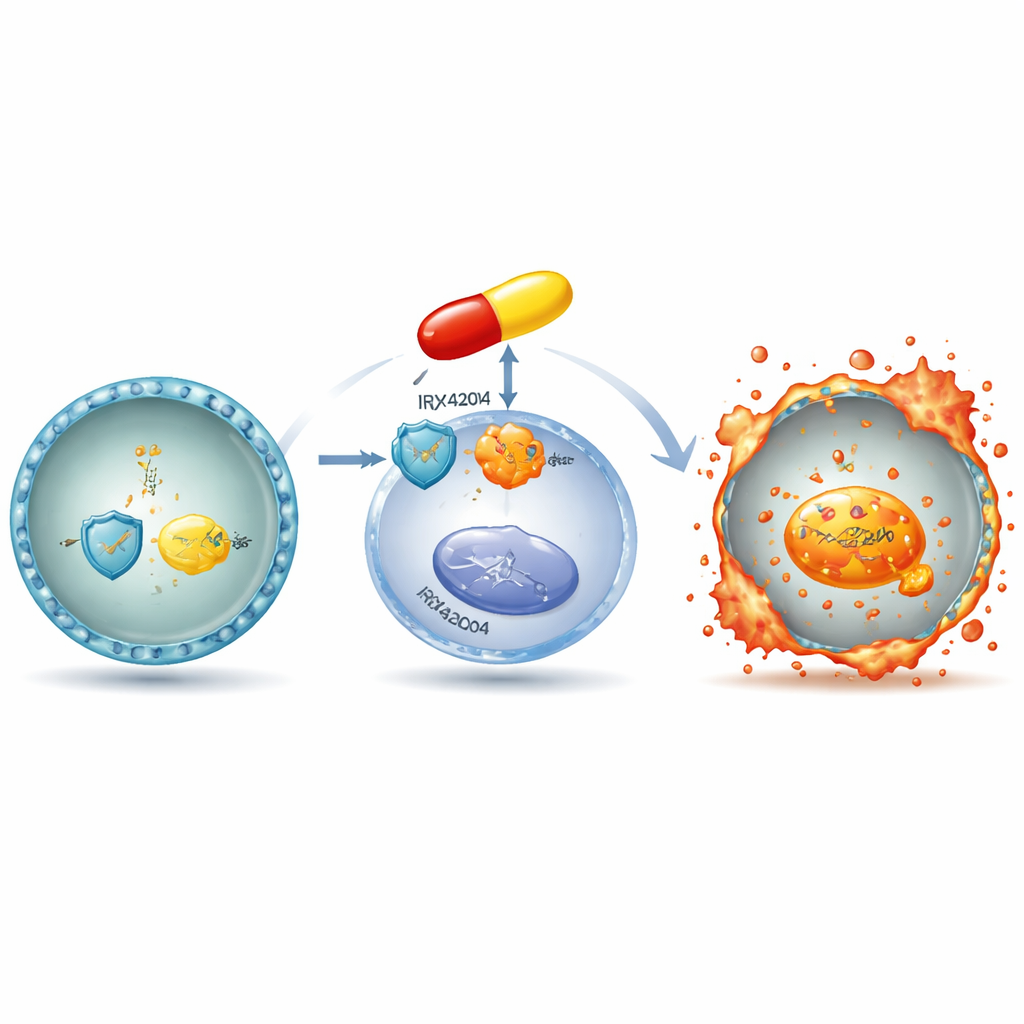
Der entscheidende Schalter zur Eisenauslösung
Um zu testen, ob HMOX1 nur ein Begleitfaktor oder wirklich essenziell ist, nutzte das Team CRISPR-Geneditierung, um es aus Myelomzellen zu entfernen. Ohne HMOX1 konnte IRX4204 die GPX4-Spiegel nicht mehr effizient senken, noch das Eisen ansammeln oder Lipidschäden treiben. Diese editieren Zellen waren deutlich weniger empfindlich gegenüber ferroptotischem Zelltod, was zeigt, dass HMOX1 upstream der gesamten Kaskade sitzt. In Mäusen mit humanen Myelomtumoren schrumpften Tumore bei Behandlung mit IRX4204 plus Lenalidomid stärker als bei Einzelbehandlungen, und das Überleben verlängerte sich; gleichzeitig zeigte sich dasselbe molekulare Muster wie in Zellkulturen: höheres HMOX1 und niedrigeres GPX4 im Tumorgewebe, ohne offensichtliche zusätzliche Toxizität.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt offenbaren die Ergebnisse einen bislang wenig beachteten Kontrollkreis—eine RXR–HMOX1–GPX4-Achse—die bestimmt, wie bereit Myelomzellen für Ferroptose sind. Durch das Verstellen dieses Reglers mit IRX4204 konnten die Forschenden Standardtherapien wirksamer machen und eine Schwachstelle in ansonsten widerstandsfähigen Krebszellen aufdecken. Obwohl weitere Arbeiten in immunkompetenten Modellen und klinischen Studien nötig sind, legt die Studie nahe, dass die gezielte Nutzung eisengetriebenen Zelltods bestehende Behandlungen ergänzen und helfen könnte, medikamentenresistentem multiplem Myelom zuvorzukommen.
Zitation: Wu, J., Yan, Z., Burcher, K. et al. IRX4204 sensitizes multiple myeloma to ferroptosis and improves lenalidomide efficacy through the HMOX1-GPX4 axis. Sci Rep 16, 13832 (2026). https://doi.org/10.1038/s41598-026-42123-9
Schlüsselwörter: multiples Myelom, Ferroptose, RXR-Agonist, HMOX1, Lenalidomid