Clear Sky Science · de
Bewertung der Auswirkungen von Gewebetyp, Konservierungsmethode und Zersetzung auf DNA‑Qualität zur Unterstützung genetischer Probenahme bei gestrandeten kleinen Cetaceen
Warum Delphinstrandungen trotzdem wichtige Erkenntnisse liefern können
Wenn ein Delphin tot an Land gespült wird, ist das eine Tragödie — aber auch eine seltene wissenschaftliche Gelegenheit. Diese gestrandeten Tiere ermöglichen es Forschern, Gewebe zu entnehmen, das Aufschluss darüber geben kann, wie es um Delphinpopulationen steht, wie sie sich bewegen und wie sie mit Verschmutzung und Klimawandel zurechtkommen. All das hängt jedoch von einer fragilen Zutat ab: intakter DNA. Diese Studie stellt eine praktische, aber entscheidende Frage: Welche Gewebe sollten wir von einem sich zersetzenden Delphin am Strand entnehmen, und wie sollten wir sie lagern, um DNA zu erhalten, die für moderne genetische Analysen ausreicht?
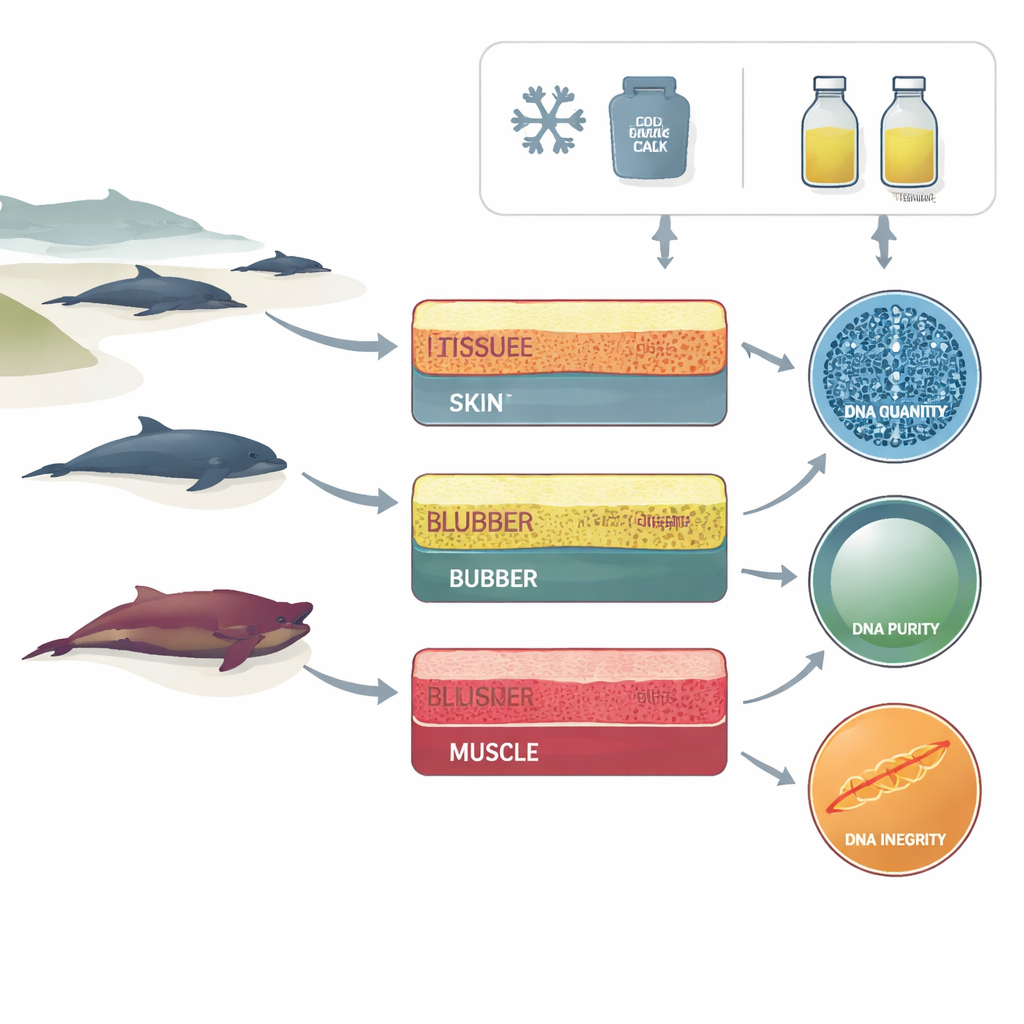
Vom Strand ins Reagenzglas
Die Forscher arbeiteten mit einem Strandungsnetzwerk entlang der portugiesischen Küste und nutzten Kadaver kleiner Delphine, die unter unterschiedlichen Bedingungen tot angespült worden waren — von frisch verstorbenen bis zu mumifizierten Überresten. Von jedem Tier entnahmen sie drei Gewebetypen, die bei Obduktionen üblicherweise verfügbar sind: die äußere Haut, das darunterliegende Fettgewebe (Blubber) und den darunterliegenden Muskel. Jede Gewebeprobe wurde danach mit einer von zwei einfachen Methoden konserviert, die die meisten Feldteams realistisch einsetzen können: eingetaucht in starkem (96 %) Ethanol bei Raumtemperatur oder eingefroren bei etwa minus 20 Grad Celsius.
Messgrößen für „gute“ DNA
Im Labor isolierte das Team DNA aus allen Kombinationen von Gewebe, Konservierungsmethode und Zersetzungsgrad. Anschließend betrachteten sie drei Aspekte der DNA‑Qualität. Zuerst: wie viel DNA sich aus einem bestimmten Gewebestück gewinnen ließ. Zweitens: die „Reinheit“, also inwieweit die Probe durch Proteine, Salze oder andere Chemikalien kontaminiert ist, die Analysen stören können. Drittens: die „Integrität“ — ob die DNA‑Stränge lang und relativ intakt sind oder in kurze Fragmente zerbrochen. Mit standardisierten Geräten maßen sie Konzentration und Reinheit und vergaben für jede Probe eine DNA‑Integritätszahl, einen Wert, der zusammenfasst, wie fragmentiert die DNA ist.
Haut für Menge, Muskel für Stabilität
Die Ergebnisse zeigten einen klaren Kompromiss zwischen erzielbarer DNA‑Menge und deren Erhaltungszustand. Die Haut war klarer Spitzenreiter bezüglich Ausbeute: über nahezu alle Zersetzungsstadien und beide Konservierungsarten hinweg erzeugte Haut deutlich höhere DNA‑Konzentrationen als Muskel oder Blubber. Hautproben wiesen zudem im Allgemeinen eine gute Reinheit auf, also wenige störende Substanzen. Mit fortschreitender Zersetzung zerfiel die DNA in der Haut jedoch schnell. Im Gegensatz dazu lieferte Muskel insgesamt weniger DNA, hielt diese aber in fortgeschrittenen Zersetzungsstadien besser intakt, insbesondere wenn das Gewebe eingefroren worden war. Blubber schnitt meist am schlechtesten ab, mit geringen DNA‑Mengen und mehr Kontamination; dennoch lieferte es brauchbare DNA, wenn Haut oder Muskel nicht verfügbar waren.
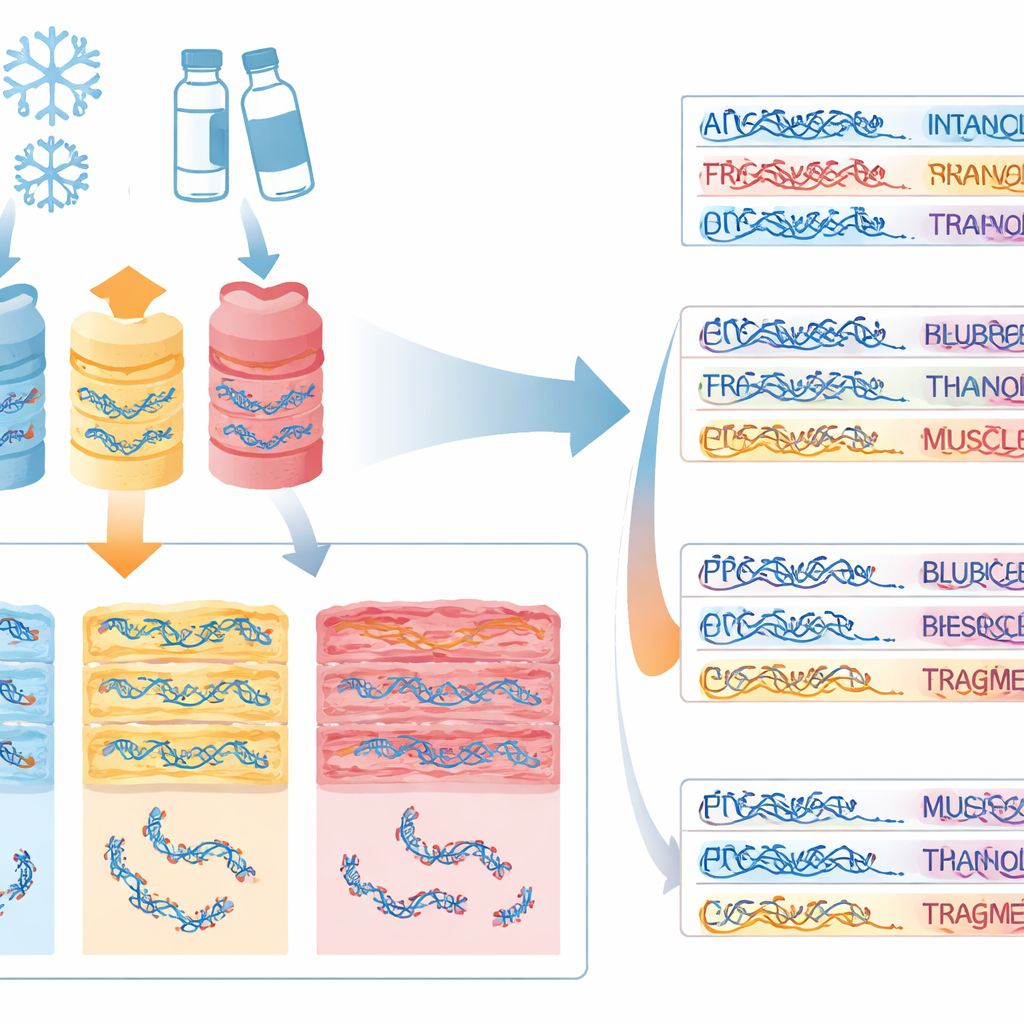
Was passiert, wenn der Körper zerfällt
Wie zu erwarten nahm die DNA‑Qualität mit zunehmender Zersetzung ab: frischere Kadaver (frühe Stadien) wiesen höhere DNA‑Konzentrationen und bessere Integrität auf, während stark zersetzte (späte Stadien und mumifizierte Überreste) mehr Fragmentierung zeigten. Es gab jedoch Überraschungen. Muskelgewebe mancher mumifizierter Kadaver, die eingefroren worden waren, zeigte tatsächlich relativ hohe DNA‑Integrität — wahrscheinlich, weil innere Gewebeschichten vor Sonne, Hitze und Aasfressern geschützt sind und anschließendes Austrocknen weiteren Abbau verlangsamen kann. Die Studie fand außerdem, dass die Menge an vorhandener DNA nicht zuverlässig vorhersagt, wie intakt sie ist: Eine Probe kann reich an DNA sein, aber dennoch zu fragmentiert für anspruchsvolle Methoden wie die Gesamtgenomsequenzierung.
Einfache Regeln für Einsatzteams vor Ort
Auf Grundlage dieser Muster schlagen die Autoren zwei praxisorientierte Rahmen vor: eine detaillierte Tabelle für Forscher, die bestimmte genetische Methoden planen, und einen vereinfachten Entscheidungsleitfaden für Strandungsteams im Feld. Bei frisch bis mäßig zersetzten Tieren empfehlen sie, die Haut zu priorisieren, konserviert entweder in Ethanol oder durch Einfrieren, da sie hohe Ausbeute, gute Reinheit und akzeptable Integrität bietet. Bei stark zersetzten oder mumifizierten Kadavern raten sie dazu, sich auf tieferliegende Muskulatur zu konzentrieren, idealerweise eingefroren, um die Chance zu maximieren, DNA zu erhalten, die noch lang und intakt genug für anspruchsvollere Analysen ist.
Was das für den Delphinschutz bedeutet
Indem die Studie systematisch untersucht, wie Gewebetyp, Konservierungsmethode und Zersetzungsstadium zusammenwirken, verwandelt sie eine unordentliche Realität — tote Delphine in unterschiedlichen Zuständen an entlegenen Stränden — in klare, evidenzbasierte Leitlinien. Für Naturschützer und Genetiker bedeutet das weniger verschwendete Proben, zuverlässigeren Daten und bessere Vergleiche zwischen Regionen und Jahren. Für die Delphine heißt das: Selbst nach dem Tod können ihre Körper effektiver dazu beitragen, Populationsgesundheit, Wanderwege und Reaktionen auf menschliche Einflüsse zu verstehen — und so die wissenschaftliche Grundlage verbessern, um diese Tiere in einem sich wandelnden Ozean zu schützen.
Zitation: Grilo, M.L., Leal e Rigor, M., Moura, A.E. et al. Evaluating effects of tissue type, preservation method, and decomposition on DNA quality to support genetic sampling in stranded small cetaceans. Sci Rep 16, 13555 (2026). https://doi.org/10.1038/s41598-026-41686-x
Schlüsselwörter: Cetacean-Genetik, Delphinstrandungen, DNA-Konservierung, Meeresnaturschutz, Wildtierprobenahme