Clear Sky Science · de
Elektrochemische Bestimmung von Dihydroxybenzol-Isomeren mittels Poly-L-Cystin-AgTiCrO2-Nanohybriden
Warum das Nachverfolgen winziger Gifte im Wasser wichtig ist
Viele industrielle Produkte, auf die wir angewiesen sind – etwa Farbstoffe, Pestizide, Gummi, Kosmetika und einige Arzneimittel – geben kleine chemische Verbindungen in Luft und Wasser ab. Drei eng verwandte Substanzen, Katechol, Hydrochinon und Resorcinol, gehören zur Familie der Dihydroxybenzole. Schon in sehr geringen Konzentrationen können sie Herz, Leber, Nieren und DNA schädigen; einige stehen im Zusammenhang mit Krebs. Da sie häufig gemeinsam auftreten und für Standardinstrumente fast identisch aussehen, benötigen Forscher schlauere, selektivere Sensoren, um sie in realen Proben wie Flusswasser oder Kosmetika schnell und kostengünstig zu erkennen.
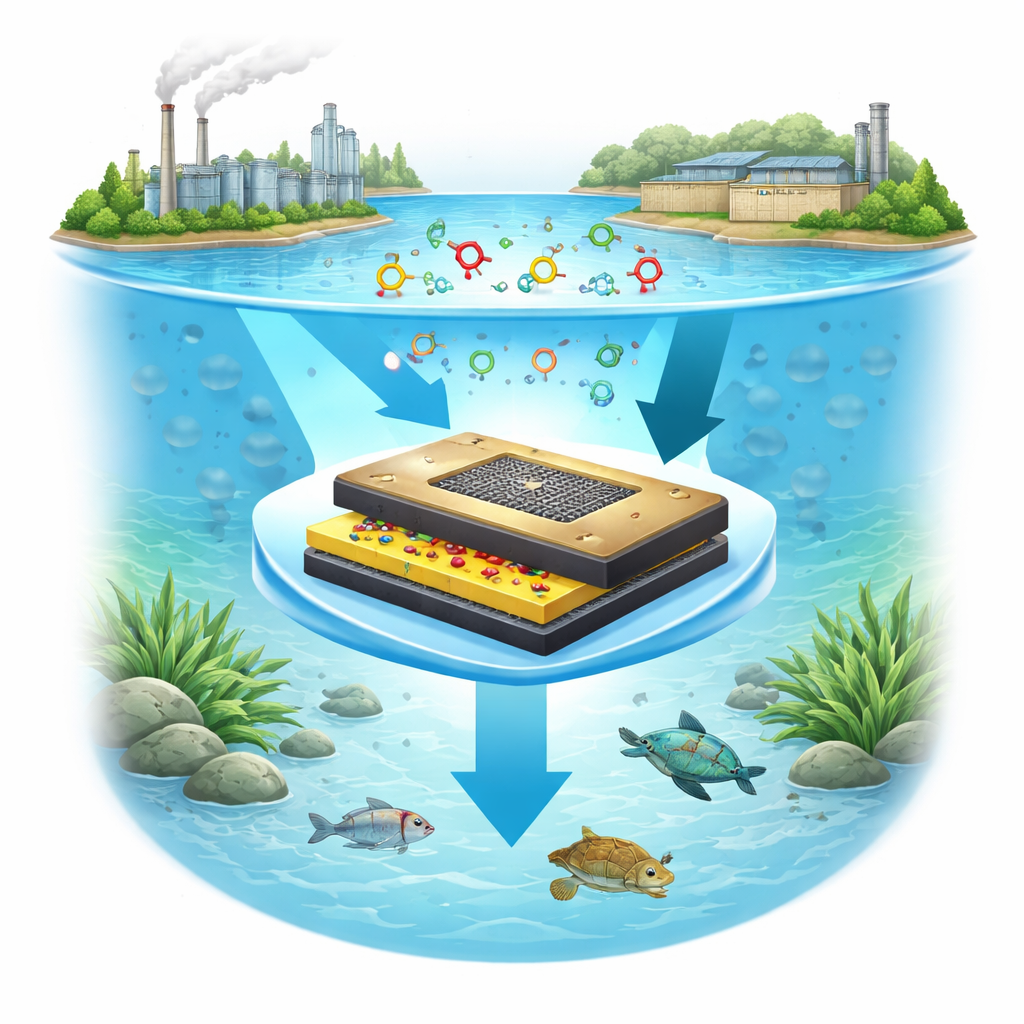
Aufbau eines neuen kleinen Detektors
Die Autoren entwickelten einen neuen elektrochemischen Sensor – im Wesentlichen eine kleine, drahtverbundene Oberfläche, deren elektrisches Verhalten sich ändert, wenn bestimmte Moleküle an ihr anhaften. Um die Oberfläche hochsensitiv zu machen, bauten sie sie aus einer geschichteten „Nanohybrid“-Struktur: Silber-, Titan- und Chromoxide, kombiniert auf Nanometerskala, getragen auf Schichten leitfähigen Kohlenstoffs, bekannt als reduziertes Graphenoxid, und beschichtet mit einem dünnen Polymer, das aus der Aminosäure L-Cystin gewachsen ist. Dieser Aufbau wird auf einer gängigen Glaskohlenstoffelektrode gebildet, unter Verwendung eines relativ einfachen „Verbrennungs“-Verfahrens zur Herstellung des Oxid-Nanohybrids, gefolgt von Lösungsschichten und elektrochemischer Filmbildung.
Wie die intelligente Oberfläche funktioniert
Der Sensor misst, wie leicht Elektronen fließen, wenn die drei Zielchemikalien in einer wässrigen Lösung vorhanden sind. Katechol, Hydrochinon und Resorcinol können jeweils Oxidations- und Reduktionsreaktionen durchlaufen – reversibler Elektronen- und Protonenaustausch – und bilden dabei verwandte Strukturen, die Benzochinone genannt werden. Die speziellen Oberflächenschichten erleichtern diesen Elektronenaustausch, sodass er schnell und sauber abläuft. Die Metalloxide liefern zahlreiche aktive Stellen und gute elektrische Leitfähigkeit; Graphen bietet eine große, leitfähige Fläche; und das auf L-Cystin basierende Polymer stellt chemische Gruppen bereit, die die Schadstoffe anziehen und den Elektronentransfer beschleunigen. Zusammengenommen macht das den Sensor reaktionsfähiger als eine nackte Kohlenstoffelektrode, die dazu neigt, zu verschmutzen, überlappende Signale zu liefern und sehr niedrige Konzentrationen zu übersehen.
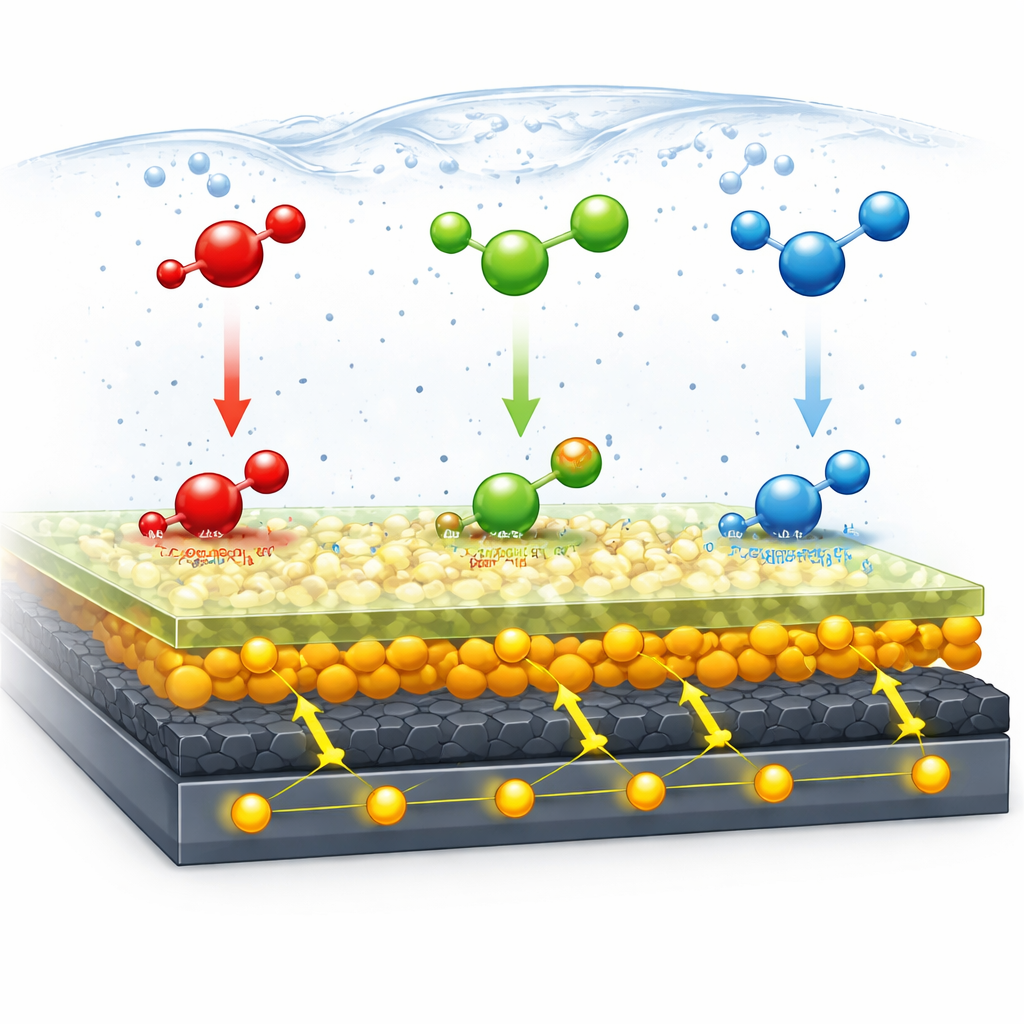
Feinabstimmung des Sensors für reale Leistung
Um die beste Leistung zu erzielen, justierte das Team mehrere Parameter sorgfältig. Sie optimierten die auf die Elektrode aufgetragene Menge an Nanohybrid-Material, sodass der Film dick genug war, um aktiv zu sein, aber nicht so dick, dass er den Elektronenfluss blockierte. Sie passten auch die Bildung des L-Cystin-Films an und ermittelten die Anzahl elektrochemischer Wachstumzyklen, die das Signal maximierten, ohne die Schicht zu überbauen. Anschließend untersuchten sie, wie der Säuregrad (pH) der Lösung und die Geschwindigkeit des Spannungsscans die Stromsignale beeinflussten. Diese Tests zeigten, dass die Reaktionen einen eng gekoppelten Austausch von zwei Elektronen und zwei Protonen umfassen und dass der Prozess hauptsächlich durch die Diffusionsgeschwindigkeit der Moleküle zur Oberfläche gesteuert wird. Durch die Wahl leicht saurer bis nahezu neutraler Bedingungen erzielten sie klare, gut getrennte Peaks für jede Verbindung.
Drei ähnlich aussehende Schadstoffe gleichzeitig erkennen
Praktisch gesehen konnte die verbesserte Elektrode Katechol, Hydrochinon und Resorcinol in extrem niedrigen Konzentrationen nachweisen – bis in den Bereich von einigen zehn bis einigen hundert Teilen pro Milliarde in Lösung – mit einer linearen, leicht kalibrierbaren Antwort über nützliche Konzentrationsbereiche. Wichtig ist, dass sie die Signale unterscheiden konnte, wenn alle drei gleichzeitig vorhanden waren, was eine zentrale Herausforderung löst, da diese Moleküle strukturell sehr ähnlich sind. Tests zeigten, dass übliche Substanzen wie Salze, Farbstoffe und Harnstoff nur geringe Störungen verursachten, und wiederholte Messungen über die Zeit hinweg lieferten gute Stabilität und Reproduzierbarkeit. Die Forscher setzten den Sensor außerdem an kommerziellen Produkten mit verwandten Inhaltsstoffen ein, etwa einer Kosmetikcreme und pharmazeutischen Formulierungen, und bestimmten realistische Konzentrationen der Zielstoffe.
Vom Labortisch zu saubereren Umgebungen
Für Nicht-Spezialisten ist die Hauptbotschaft, dass die Autoren eine hochreaktive, geschichtete Sensoroberfläche entwickelt haben, die drei giftige, ähnlich aussehende Schadstoffe in winzigen Konzentrationen in komplexen Gemischen erkennen kann. Durch die Kombination eines durchdacht entworfenen Metalloxid-Nanohybrids mit leitfähigem Kohlenstoff und einem biologisch inspirierten Polymer verbesserten sie Empfindlichkeit und Selektivität gegenüber vielen bestehenden Geräten. Diese Art tragbarer, kostengünstiger elektrochemischer Sensoren könnte letztlich Regulierungsbehörden und Herstellern helfen, Wasser, Kosmetika und industrielle Ströme effektiver zu überwachen, die Exposition gegenüber schädlichen Chemikalien zu reduzieren und zu sichereren Produkten sowie saubereren Umgebungen beizutragen.
Zitation: Achar, S., Bhat, R.S., Sajankila, S.P. et al. Electrochemical determination of dihydroxybenzene isomers utilising poly-L-cystine-AgTiCrO2 nanohybrids. Sci Rep 16, 14340 (2026). https://doi.org/10.1038/s41598-026-41391-9
Schlüsselwörter: elektrochemischer Sensor, Wasserverunreinigungen, Nanomaterialien, Umweltüberwachung, phenolische Verbindungen