Clear Sky Science · de
Der Mausstamm 129S1/SvImJ bildet schweren hypertensiven Zielorganschaden bei moderater Angiotensin-II-induzierter Hypertonie nach
Warum einige Körper unter hohem Blutdruck zusammenbrechen
Hoher Blutdruck wird oft als „stiller Killer“ bezeichnet, weil er Gehirn, Herz, Nieren und Augen über viele Jahre hinweg unauffällig schädigt. Doch nicht alle Menschen mit demselben Blutdruckniveau entwickeln die gleichen Schäden. Diese Studie nutzt Mäuse, um eine einfache, aber wichtige Frage zu stellen: Wenn zwei Individuen derselben Druckerhöhung ausgesetzt sind, warum erleidet der eine Schlaganfälle, Gedächtnisverlust und Nierenversagen, während der andere relativ verschont bleibt?
Zwei Mäusestämme, eine gemeinsame Belastung
Die Forschenden verglichen zwei gängige Labormausstämme, die sich genetisch unterscheiden. Beide Gruppen erhielten über kleine unter der Haut platzierte Pumpen eine konstante, moderate Dosis Angiotensin II, ein Hormon, das zuverlässig den Blutdruck erhöht. Sorgfältige Telemetrie zeigte, dass beide Stämme über vier Wochen sehr ähnliche Blutdruckwerte und Herzfrequenzen erreichten. Körpergewicht und Überleben waren ebenfalls vergleichbar, sodass Unterschiede in der Schädigung nicht einfach damit erklärt werden konnten, dass eine Gruppe stärker hypertensiv war als die andere.
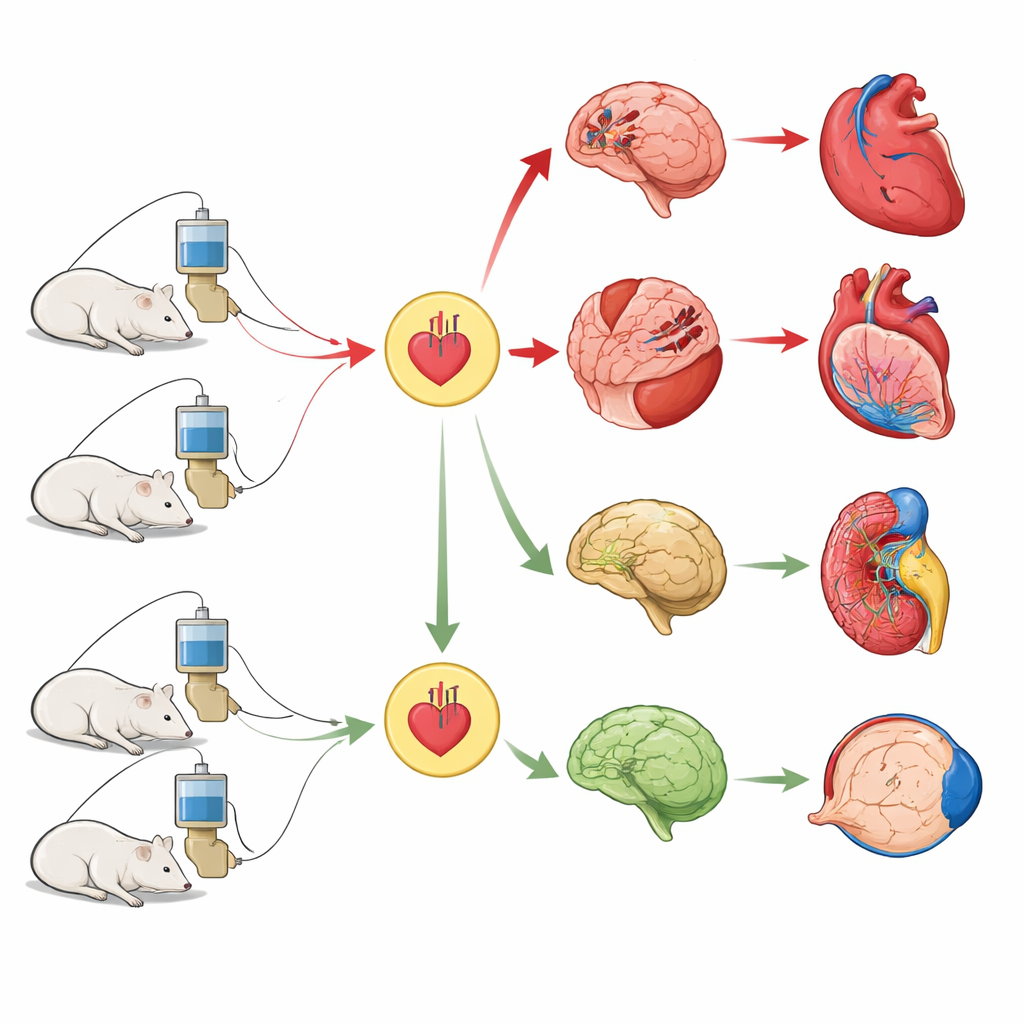
Ein Stamm zeigt Gehirn- und Augenschäden
Trotz derselben Druckerhöhung entwickelten nur die 129S1/SvImJ-Mäuse eindeutige Anzeichen für Gehirnprobleme. In Gedächtnistests mit dem Morris-Wasserlabyrinth taten sich diese Mäuse schwer, den Standort der Plattform zu erlernen und sich zu merken, während die weit verbreiteten C57BL/6J-Mäuse normal abschnitten. Beim Blick auf die schützende Blut-Hirn-Schranke fanden die Forschenden, dass kleine Farbmoleküle leichter ins Gehirngewebe der 129-Stämme eindrangen, was auf eine „leckende“ Barriere hinweist. Diese Mäuse zeigten zudem mehr kleine Hirnblutungen und stärkere Aktivierung von sternförmigen Stützzellen, den Astrozyten — ein Muster, das der menschlichen Kleingefäßerkrankung ähnelt, einer wichtigen Ursache vaskulärer Demenz.
Nieren, Herzen und Netzhaut unter Belastung
Niere, Herz und Augen erzählten eine ähnliche Geschichte. Nur der 129-Stamm entwickelte einen starken Albuminverlust im Urin, ein Warnsignal dafür, dass die Filterbarriere der Niere versagt. Elektronenmikroskopisch zeigten ihre Podozyten — die spezialisierten Zellen, die die Nierenfilter umhüllen — abgeflachte, beschädigte Fußfortsätze. Gentests bestätigten, dass Schlüsselmoleküle für die Gesundheit von Podozyten und Gefäßen herunterreguliert waren. Im Herzen wies derselbe Stamm verdickte Herzwände, vergrößerte Herzmuskelzellen und Veränderungen in der elektrischen Leitung auf, konsistent mit hypertensiver Kardiomyopathie, während die Herzen der C57BL/6J-Mäuse nahezu normal blieben. In der Netzhaut zeigten die 129-Mäuse Leckagen von fluoreszierenden Tracern und eine Störung der Blut-Retina-Barriere, wiederum ein Spiegelbild von Komplikationen, wie sie bei langjähriger Hypertonie beim Menschen beobachtet werden.
Immunologische Signale bereiten den Boden
Um zu untersuchen, warum ein Stamm unterlag, während der andere resistent blieb, analysierte das Team die Genaktivität in kleinen Hirngefäßen zu frühen und späten Zeitpunkten. Schon nach einer Woche Angiotensin II zeigten Gefäße der 129-Mäuse eine starke Aktivierung immunologischer und entzündlicher Programme, einschließlich vieler interferonbezogener Gene. Nach vier Wochen verschob sich ihr Genprofil hin zu Markern struktureller Umgestaltung und Vernarbung, passend zu den sichtbaren Schäden. Im Gegensatz dazu reagierten die Gefäße der C57BL/6J-Mäuse deutlich zurückhaltender. Interessanterweise zeigten diese „geschützten“ Mäuse eine verstärkte Rekrutierung von Mikroglia und perivaskulären Immunzellen, was auf eine kontrollierte, möglicherweise schützende Entzündungsreaktion hindeutet, die die Barrierefunktion bewahrte, statt sie zu zerstören.
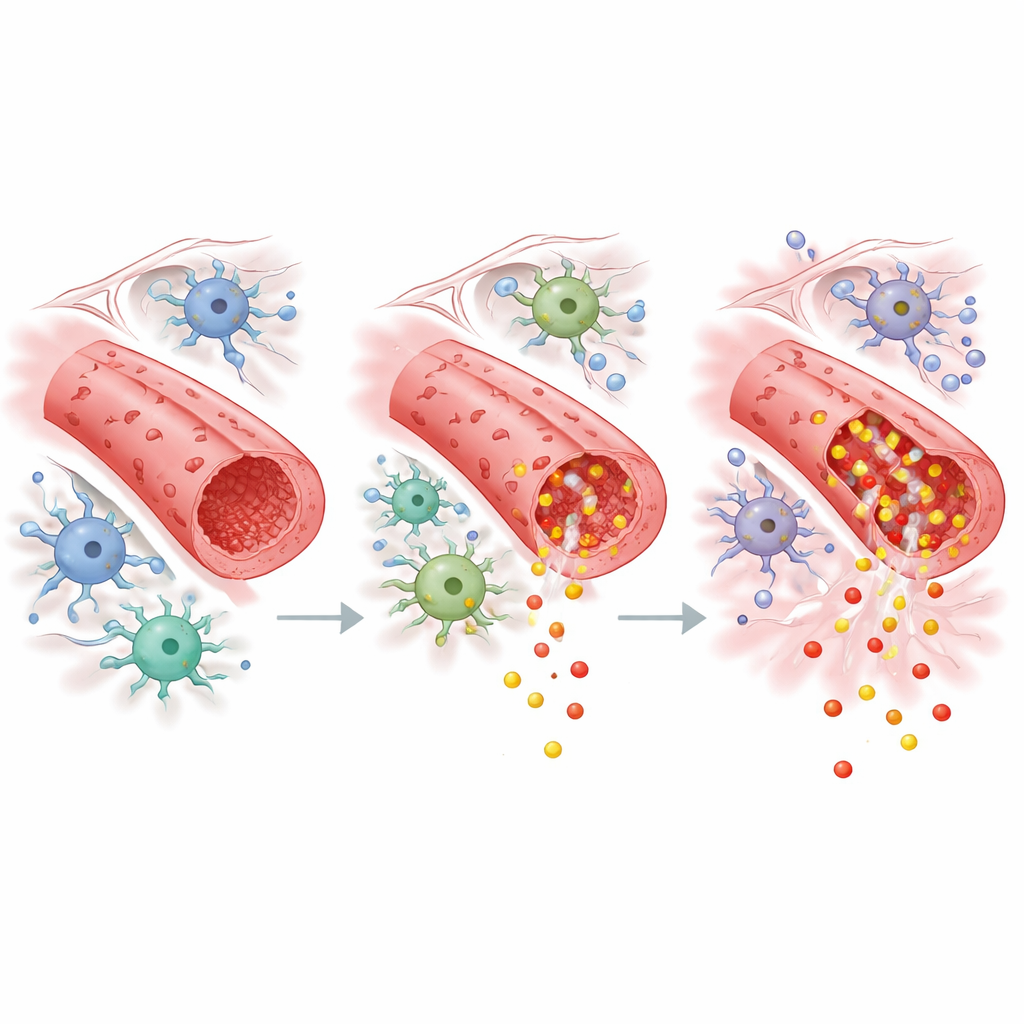
Was das für das Verständnis von Risiko bedeutet
Die Ergebnisse zusammen zeigen, dass der genetische Hintergrund maßgeblich bestimmt, wie Organe auf denselben Blutdruck reagieren. Der Stamm 129S1/SvImJ erweist sich als sensibles Modell, das viele der Gehirn-, Nieren-, Herz- und Augenkomplikationen nachbildet, die bei schwerer menschlicher Hypertonie auftreten, während C57BL/6J-Mäuse oft überraschend verschont bleiben. Für Laien lautet die zentrale Botschaft: „Wie Ihr Körper gebaut ist“ ist mindestens ebenso wichtig wie die bloße Blutdruckzahl. Dieses Mausmodell bietet Forschenden nun ein wertvolles Werkzeug, um herauszufinden, welche Gene und Immunwege das Gleichgewicht von stiller Hypertonie zu verheerendem Organschaden kippen — und letztlich um Therapien zu entwickeln, die diejenigen schützen, die am stärksten gefährdet sind.
Zitation: Orieux, A., Boulestreau, R., Bats, ML. et al. The 129S1/SvlmJ mouse strain recapitulates severe hypertensive target organ damage under moderate angiotensin II–induced hypertension. Sci Rep 16, 12155 (2026). https://doi.org/10.1038/s41598-026-41288-7
Schlüsselwörter: Hypertonie, genetische Anfälligkeit, Zielorganschaden, Mausmodelle, Kleingefäßerkrankung