Clear Sky Science · de
Hybride fuzzy Machine‑Learning‑Modelle, optimiert mit Metaheuristiken, für präzise EEG‑basierte neurologische Beurteilung
Den Hirnwellen lauschen
Wenn jemand Epilepsie hat oder in ein tiefes Koma fällt, greifen Ärzte häufig auf Elektroenzephalogramme (EEGs) zurück — Aufzeichnungen der elektrischen Aktivität des Gehirns — um zu verstehen, was vor sich geht. Doch diese feinen Zuckungen rein visuell zu lesen ist langsam, subjektiv und stark von der Expertise der Beurteilenden abhängig. Dieser Beitrag stellt ein automatisiertes, hochpräzises System vor, das lernt, EEG‑Muster sowohl zur Erkennung von Anfällen als auch zur Koma‑Beurteilung zu interpretieren, und damit schnellere und konsistentere Hilfe für Patienten verspricht, wenn jede Sekunde zählt.
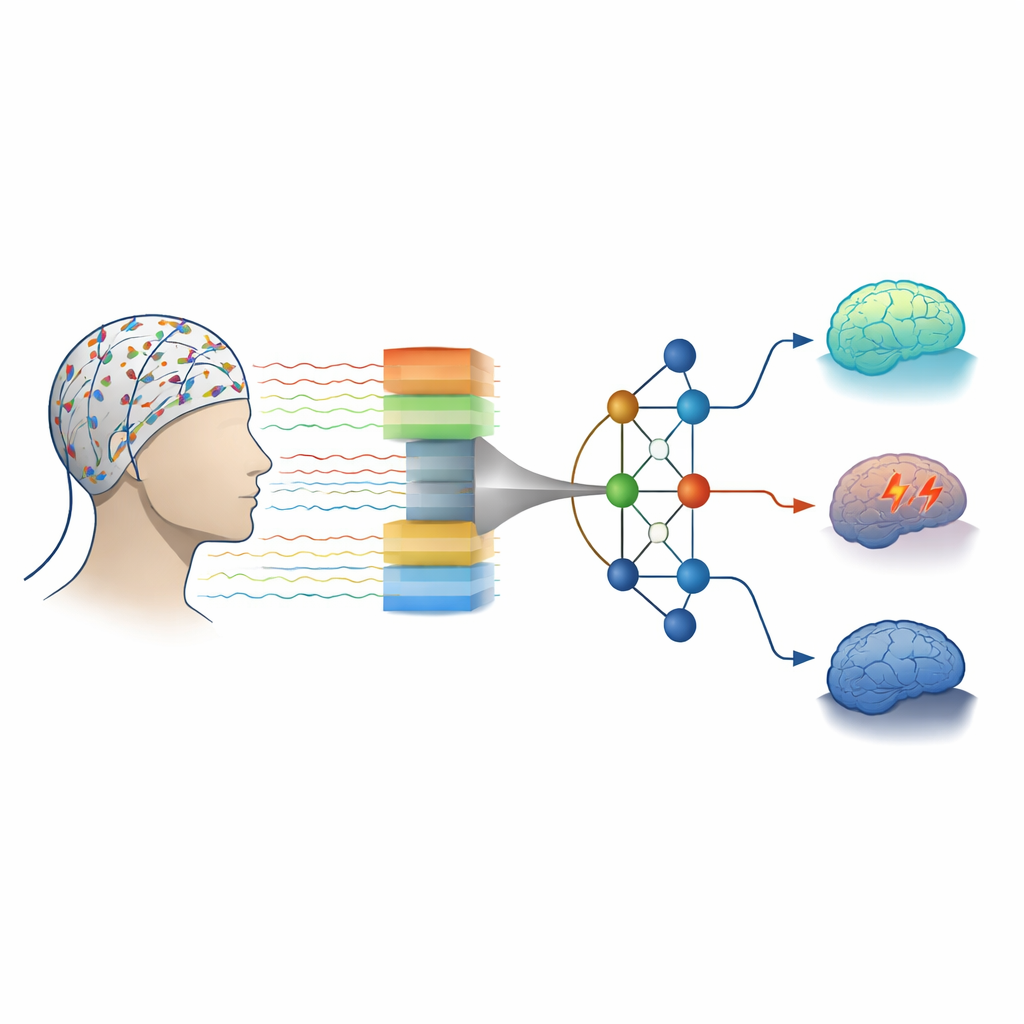
Warum Hirnsignale schwer zu lesen sind
EEG wird seit einem Jahrhundert eingesetzt, um die Gehirnaktivität ohne Operation zu überwachen. Es ist entscheidend, um epileptische Anfälle zu erkennen und um abzuschätzen, wie bewusst ein komatöser Patient tatsächlich ist. Trotzdem sind Roh‑EEG‑Signale unordentlich: Sie enthalten Störgeräusche durch Muskelbewegungen, elektrische Interferenzen und natürliche Unterschiede zwischen Individuen. Subtile Unterschiede zwischen normaler Hirnaktivität, tumorbetroffenen Regionen und Anfallsereignissen können in diesem Durcheinander verborgen liegen. Ärzte verbringen derzeit lange Stunden mit dem Absuchen dieser Kurven, und in vielen Regionen gibt es zu wenige Spezialisten, sodass Anfälle übersehen und das Koma‑Ausmaß falsch eingeschätzt werden können. Die Autoren zielen darauf ab, einen Großteil dieser Belastung an intelligente Software abzugeben, die verlässliche Muster im Chaos erkennt.
Komplexe Hirnwellen auf das Wesentliche reduzieren
Das System beginnt damit, die EEG‑Signale zu säubern und zu zerlegen. Es filtert Rauschen heraus und misst anschließend eine breite Palette von Eigenschaften in jedem Aufnahmefenster: einfache Statistiken wie Mittelwert und Varianz, wie die Signalenergie über verschiedene Frequenzbänder verteilt ist (etwa die bekannten Delta‑, Theta‑, Alpha‑ und Beta‑Wellen) sowie fortgeschrittenere "Unregelmäßigkeits"‑Maße, sogenannte Entropien, die erfassen, wie unvorhersehbar das Signal ist. Diese vielen Messgrößen bilden eine sehr hochdimensionale Beschreibung jedes Zeitpunkts der Gehirnaktivität. Um das handhabbar zu machen, führen die Autoren eine Merkmalsreduktions‑Stufe ein, die dutzende Zahlen mathematisch auf eine kompakte Menge komprimiert und dabei bewahrt, was Zustände des Gehirns am besten voneinander trennt.
Von der Natur inspirierte Abstimmung des Klassifikators
Zur Gestaltung dieser Kompressionsstufe und des anschließenden Klassifikators entlehnen die Forschenden Ideen aus der Natur. Ein "Wasserzyklus"‑Algorithmus ahmt nach, wie Bäche zu Flüssen und Meeren zusammenfließen, erkundet viele alternative Möglichkeiten, Merkmale zu kombinieren, und behält diejenigen bei, die ähnliche EEG‑Muster eng zusammenclustern, während unterschiedliche Muster weiter auseinandergehalten werden. Parallel dazu imitiert ein "Seestern"‑Optimierungsalgorithmus, wie Seesterne sich bewegen und anpassen, und nutzt virtuelle Schwärme, um die internen Parameter eines Entscheidungssystems feinzujustieren. Dieses Entscheidungssystem, DT‑FIS genannt, verbindet einen Entscheidungsbaum (der Daten in Verzweigungen aufteilt) mit Fuzzy‑Logik (die weiche, graduelle Grenzen statt starre Schwellenwerte zulässt). Zusammengenommen ermöglichen diese Elemente dem Modell, mit Unsicherheit und Feinheiten in den Hirnsignalen umzugehen, statt zu früh grobe Ja/Nein‑Entscheidungen zu erzwingen.
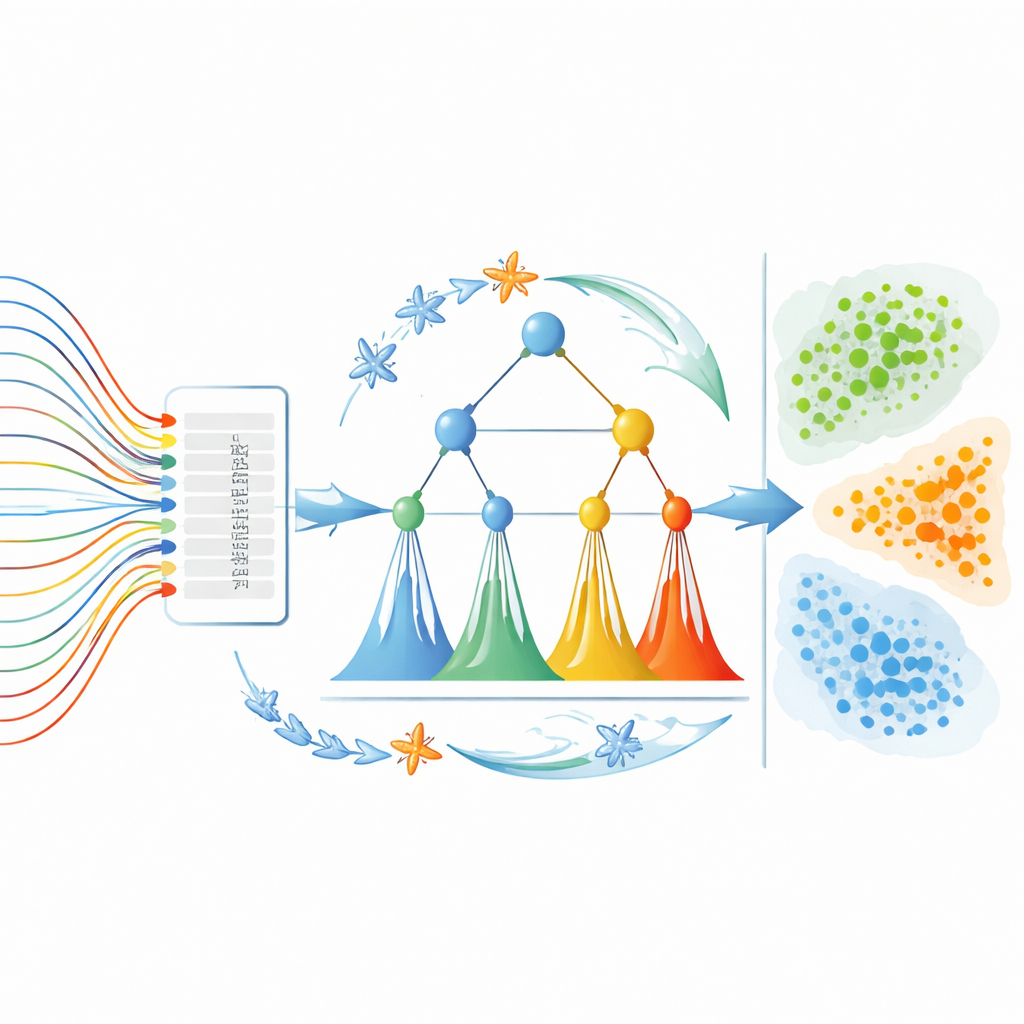
Anfälle und Bewusstseinsgrade einordnen
Die Autoren testen ihr Framework an zwei anspruchsvollen Aufgaben. Erstens, mit EEG‑Aufnahmen des American University of Beirut Medical Center, muss das System verschiedene Arten von Anfallsaktivität von ruhigen, nicht‑anfallsbezogenen Perioden unterscheiden. Zweitens, mit einem separaten Datensatz aus Intensivstationen, soll es anhand der weit verbreiteten Glasgow Coma Scale abschätzen, wie bewusst Koma‑Patienten sind, während diese sich in Ruhe‑ und Stimulationsphasen mit Pflegenden und Angehörigen bewegen. Nach dem Training erreichen die hybriden Modelle beeindruckende Leistungen: etwa 99 % Genauigkeit bei der Identifizierung tiefer Komapegel und ähnliche Werte bei der Abgrenzung von Anfall‑ und Nicht‑Anfall‑Zuständen, und übertreffen damit viele aktuelle Deep‑Learning‑Ansätze, während sie weniger Merkmale verwenden und besser interpretierbar bleiben.
Was das für Patienten bedeutet
Einfach gesagt zeigt die Studie, dass die Kombination aus sorgfältig ausgewählten EEG‑Messgrößen, intelligenter Dimensionsreduktion und fuzzy, naturnah abgestimmten Entscheidungsregeln einen nahezu "immer richtigen" automatischen Leser von Hirnwellen ergeben kann. Solche Systeme könnten am Patientenmonitor oder auf tragbarer Hardware laufen, Anfälle innerhalb von Sekunden melden und dem Personal eine objektive Zweitmeinung darüber liefern, wie wach oder bewusstlos ein Patient wirklich ist. Zwar müssen die Modelle noch an größeren und vielfältigeren Populationen validiert werden, doch weist die Arbeit in Richtung einer Zukunft, in der kontinuierliche, verlässliche Hirnüberwachung auch in ressourcenarmen Krankenhäusern verfügbar ist und so hilft, gefährliche Ereignisse früh zu erfassen und Therapieentscheidungen auf solide, datenbasierte Einsichten zu stützen.
Zitation: Lak, M., Jamali, J., Adlband, N. et al. Hybrid fuzzy machine learning models optimized with meta-heuristics for accurate EEG-based neurological assessment. Sci Rep 16, 11888 (2026). https://doi.org/10.1038/s41598-026-35669-1
Schlüsselwörter: EEG, epileptische Anfälle, Koma‑Beurteilung, fuzzy Machine Learning, neurologische Überwachung