Clear Sky Science · de
Eine offene B‑Mode‑Ultraschalldatenbank für Deep‑Learning‑basierte Atherosklerose‑Plaque‑Segmentierung
Warum es wichtig ist, versteckte Gefäßprobleme zu erkennen
Herzinfarkte und Schlaganfälle treten oft ohne Vorwarnung auf, doch die Gefahr entsteht schleichend, wenn fettige Ablagerungen, sogenannte Plaques, die Arterien verengen, die Gehirn und Herz versorgen. Ärztinnen und Ärzte können diese Plaques mit Ultraschallaufnahmen des Halses sichtbar machen, doch jede Aufnahme per Hand sorgfältig nachzuzeichnen ist zeitaufwendig und fehleranfällig. Dieser Artikel stellt eine offene, fachkundig annotierte Bildsammlung vor, mit der Computer lernen können, Plaques automatisch zu finden — mit dem langfristigen Ziel, die Einschätzung des Schlaganfall‑ und Herzinfarktrisikos schneller, konsistenter und breiter zugänglich zu machen.
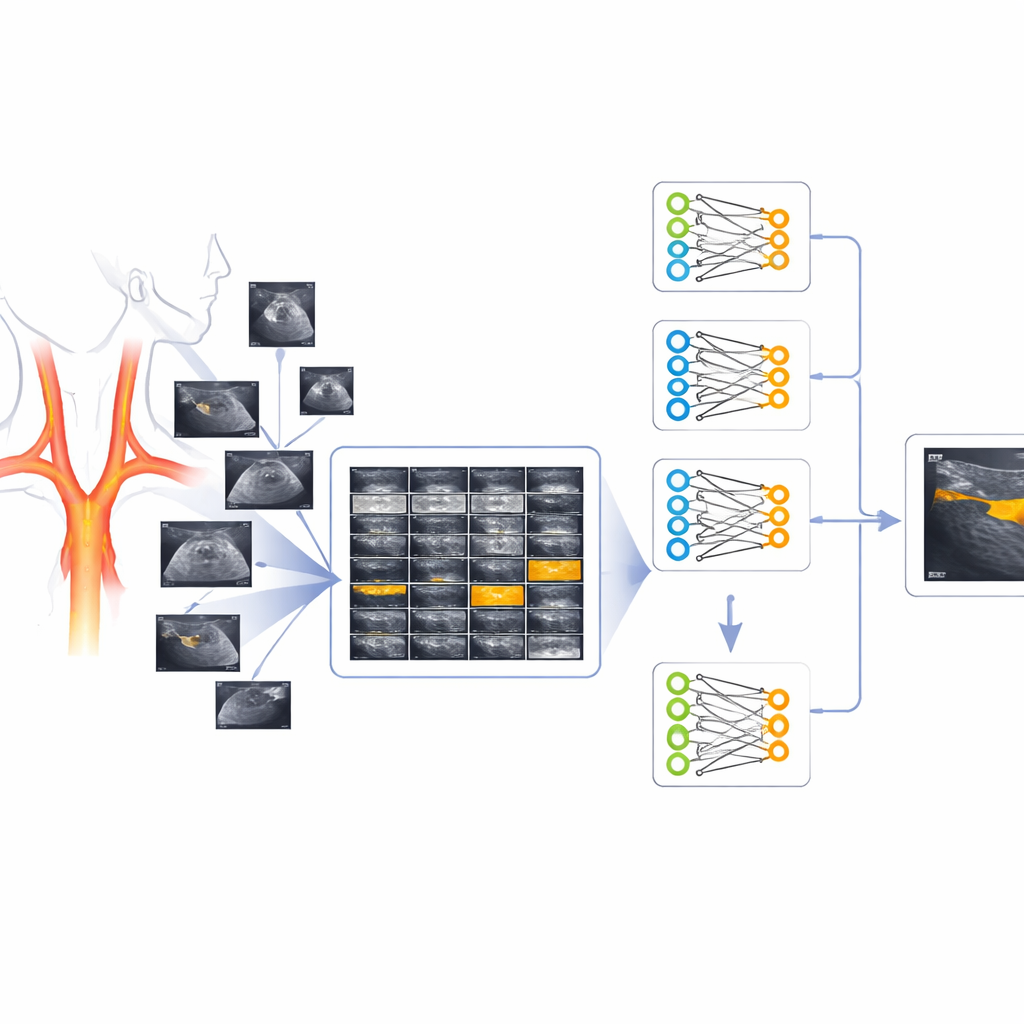
Ein genauerer Blick auf Gefäßablagerungen
Atherosklerose ist die langsame Verhärtung und Verdickung mittelgroßer und großer Arterien, wenn Fette und Entzündungszellen in der Gefäßwand akkumulieren. Betroffen die Karotisarterien im Hals, kann dies den Blutfluss zum Gehirn verringern und das Schlaganfallrisiko erhöhen. Eine aussagekräftige Risikoschätzung ergibt sich aus der Messung der gesamten Fläche, die diese Plaques entlang der Karotis einnehmen. Das Problem ist, dass bevor Ärztinnen, Ärzte oder Computer die Plaque‑Fläche messen können, jemand auf jeder Ultraschallaufnahme die Plaque markieren muss — eine Aufgabe, die Ausbildung, Zeit und eine Konstanz erfordert, die in belebten Kliniken schwer durchzuhalten ist.
Warum Computer bessere Beispiele brauchen
Moderne künstliche Intelligenz, insbesondere Deep Learning, kann lernen, Plaques automatisch nachzuzeichnen, wenn ihr genügend Beispiele gezeigt werden, in denen Expertinnen und Experten bereits die korrekten Grenzen gezogen haben. Viele frühere Forschungsprojekte nutzten solche Methoden erfolgreich, jedoch häufig unter idealisierten Bedingungen: Bilder werden sorgsam auf eine einzelne, deutliche Plaque zugeschnitten, es fehlen Beispiele von Bildern ohne Plaque oder mit mehreren Plaques. Solche privaten Datensätze werden meist nicht geteilt, sodass es schwierig ist, Ergebnisse zu reproduzieren oder einzuschätzen, ob ein Algorithmus in der alltäglichen, unordentlichen klinischen Realität funktioniert.
Aufbau einer realistischen Bildsammlung
Um diese Lücke zu schließen, stellten die Autorinnen und Autoren eine gereinigte Datenbank mit 541 Ultraschallaufnahmen der Karotisarterien aus einer Hochrisikogruppe in Argentinien zusammen. Für jedes Bild lieferten Spezialistinnen und Spezialisten eine passende „Maske“, in der Plaque‑Regionen markiert waren, sodass jeweils ein Paar entstand: die originale Schwarz‑Weiß‑Aufnahme und eine einfache Schwarz‑Weiß‑Kontur der Plaque. Das Team entfernte sorgfältig visuelle Störungen wie Kreuze, Zahlen und Gerätekennzeichnungen, standardisierte alle Bilder auf ein quadratisches Format und sorgte dafür, dass beide Bilder eines Paares perfekt ausgerichtet waren. Die finale Sammlung enthält absichtlich Aufnahmen ohne Plaques, mit einzelnen oder mehreren Plaques sowie Plaques, die abseits der Bildmitte liegen — eine bessere Abbildung dessen, was Ärztinnen und Ärzte tatsächlich sehen.
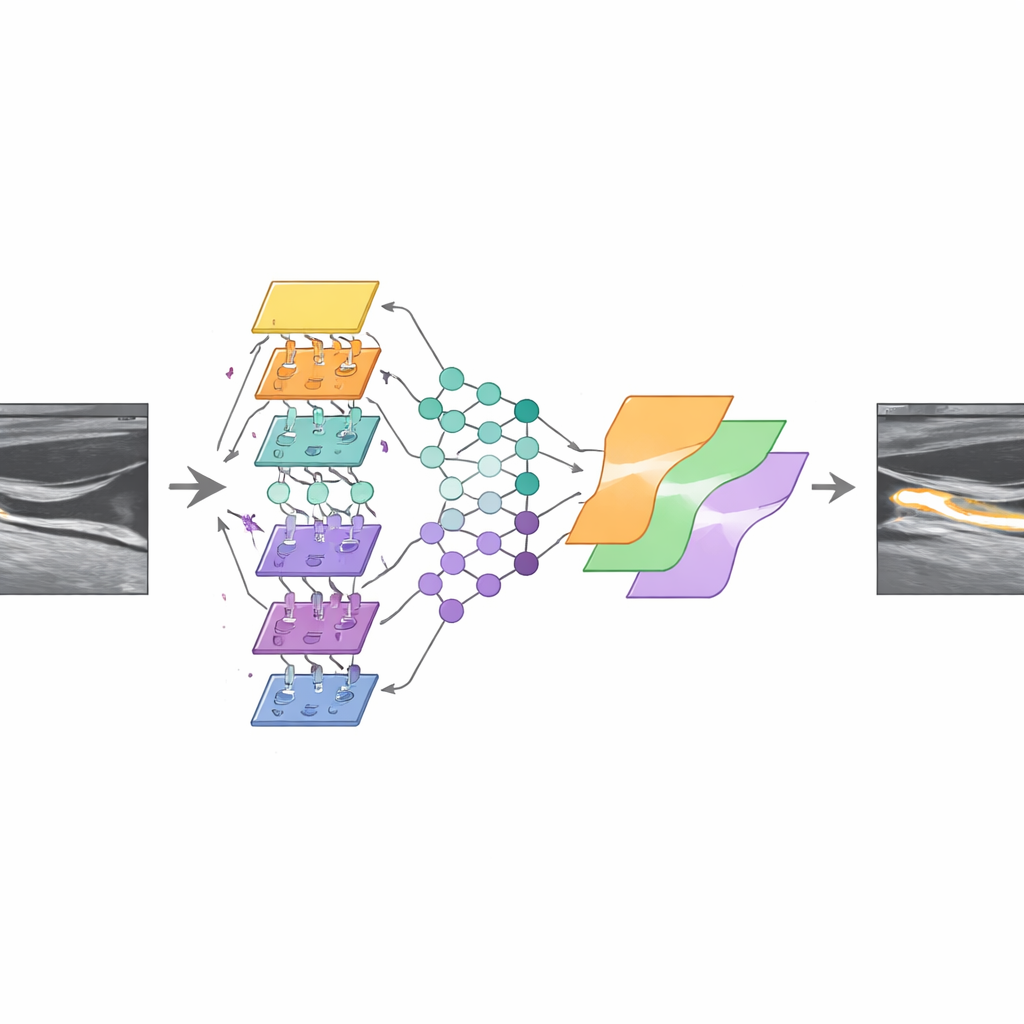
Neurale Netze die Konturen ziehen lassen
Um zu prüfen, ob die Datenbank tatsächlich nützlich für die Algorithmusentwicklung ist, trainierten die Forschenden drei Varianten eines verbreiteten Bildsegmentierungsnetzes, bekannt als U‑Net, jeweils mit anderem Backbone zur Mustererkennung. Sie erweiterten die Trainingsdaten durch Spiegeln und leichtes Verschieben der Bilder und kombinierten die drei Modelle zu einem „Ensemble“, das pixelweise darüber abstimmt, ob eine Stelle zur Plaque gehört oder nicht. Auf Bildern mit Plaques erreichte dieses Ensemble eine moderate Überlappung mit den Expertenzeichnungen, vergleichbar mit dem, was verschiedene menschliche Spezialistinnen und Spezialisten untereinander erzielen. Bei plaque‑freien Bildern erzeugte das kombinierte System relativ wenige Fehlalarme, was darauf hindeutet, dass es nicht nur gelernt hat, wie Plaque aussieht, sondern auch wann keine vorhanden ist.
Was das für die zukünftige Versorgung bedeutet
Für Nicht‑Spezialisten ist die zentrale Botschaft, dass diese offene Datenbank verstreute, schwer zugängliche klinische Bilder in eine gemeinsame Ressource verwandelt, die jede und jeder nutzen kann, um Plaque‑Erkennungsalgorithmen zu trainieren und zu testen. Obwohl die Leistung noch nicht perfekt ist und vom speziellen Patientenkollektiv sowie der Bildgebungshardware beeinflusst wird, zeigt die Arbeit, dass Computer selbst unter realistischeren und vielfältigeren Bedingungen an Expertenniveau heranreichen können. Indem die Studie sowohl die Bilder als auch den Evaluationscode frei zugänglich macht, schafft sie die Grundlage für robustere Werkzeuge, die Ärztinnen und Ärzten helfen können, die Plaque‑Last schnell und konsistent zu messen und damit Präventionsstrategien gegen Herzinfarkte und Schlaganfälle zu verbessern.
Zitation: Rulloni, V.S., Perez, H.A., Dori, T. et al. An open B-mode ultrasound database for deep learning-based atherosclerotic plaque segmentation. Sci Data 13, 702 (2026). https://doi.org/10.1038/s41597-026-06952-7
Schlüsselwörter: Atherosklerose, Karotisultraschall, medizinische Bild‑KI, Plaque‑Segmentierung, kardiovaskuläres Risiko