Clear Sky Science · de
Elektronische Herkunft der Rekorganisationsenergie bei interfacialem Elektronentransfer
Warum es darauf ankommt, wie Oberflächen Elektronen bewegen
Von den Batterien in Handys bis zu den Proteinen, die unsere Zellen antreiben: Viele Technologien und Lebensprozesse beruhen darauf, dass Elektronen die Grenze zwischen einer festen Oberfläche und einer Flüssigkeit überqueren. Jahrzehntelang gingen Forschende davon aus, dass die flüssige Seite dieser Grenze den Löwenanteil der Kontrolle über die Geschwindigkeit dieses Elektronensprungs übernimmt, während die feste Seite lediglich bei Bedarf Elektronen bereitstellt. Diese Arbeit stellt diese Annahme auf den Kopf, indem sie zeigt, dass die elektronische Beschaffenheit der festen Oberfläche selbst stark die Kosten für das Bewegen eines Elektrons — und damit die Geschwindigkeit von Energie- und Chemieflüssen — steuern kann.
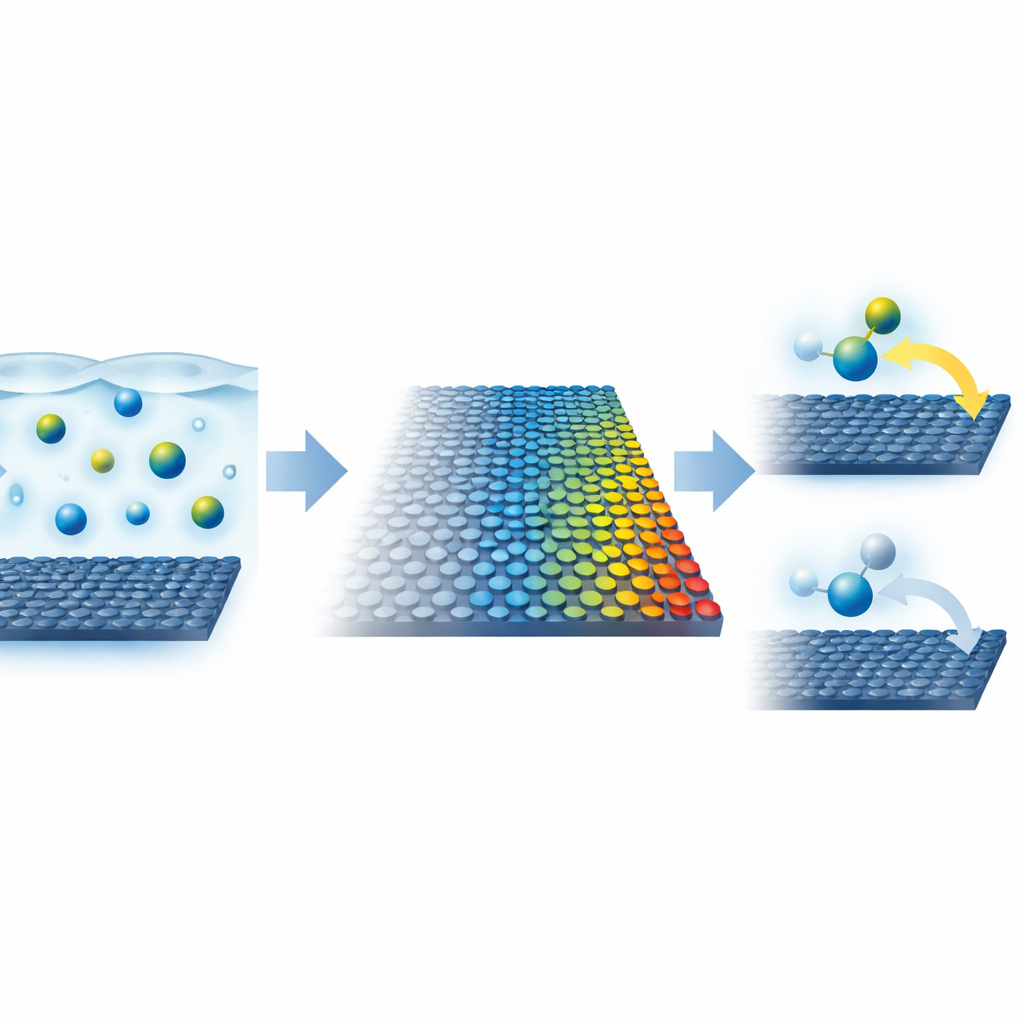
Ein klassisches Bild des Elektronenflusses neu betrachtet
Traditionelle Theorien des Elektronentransfers beschreiben den Prozess wie das Überwinden eines Hügels mit einem Ball. Die Höhe dieses Hügels, die Aktivierungsbarriere, hängt weitgehend davon ab, wie stark sich die Atome und die umgebende Flüssigkeit verschieben müssen, um die neue Ladung aufzunehmen — ein Energieaufwand, der als Rekorganisationsenergie bekannt ist. In der Standardvorstellung stammt dieser Aufwand nahezu vollständig aus der Flüssigkeit und dem gelösten Molekül, während die feste Elektrode hauptsächlich als Elektronenreservoir fungiert, dessen verfügbare Zustände die möglichen Pfade für das Elektron bestimmen. Die Autorinnen und Autoren stellen eine einfache, aber weitreichende Frage: Was, wenn die Elektronen der Elektrode selbst und ihre Neigung zur Umverteilung ebenfalls die Höhe dieses Hügels verändern?
Designer-Stapel aus atomdünnen Materialien aufbauen
Um diese Idee zu untersuchen, bauten die Forschenden sorgfältig geschichtete Strukturen aus einatomigen Kristallen. Eine Graphenschicht diente als Elektrode, deren elektronische Fülle sich gezielt einstellen ließ. Auf der anderen Seite einer ultradünnen Isolatorschicht aus hexagonalem Bornitrid platzierten sie Kristalle, die entweder Elektronen aus dem Graphen ziehen oder ihm Elektronen zuführen. Durch Variation der Dicke dieses Abstandsgebers konnten sie fein steuern, wie viele zusätzliche Ladungsträger sich im Graphen ansammelten und wie metallisch es sich verhielt. Anschließend verwendeten sie eine mit einem gut untersuchten Redoxmolekül gefüllte Nanopipette, um winzige, gut definierte Flüssigkeitszellen auf der Graphenoberfläche zu erzeugen, und maßen, wie schnell Elektronen zwischen dem Molekül in Lösung und der festen Schicht wechselten.
Beobachtung, wie sich Elektronengeschwindigkeiten mit elektronischer Fülle ändern
Mit steigender elektronischer Fülle beziehungsweise Zustandsdichte im Graphen erhöhte sich die Elektronentransferrate dramatisch — weit mehr, als die klassische Theorie allein anhand einer größeren Anzahl verfügbarer elektronischer Pfade vorhersagen würde. Selbst wenn der Dotierkristall durch mehrere zehn Nanometer Bornitrid vom Graphen getrennt war, zeigte die Oberfläche schnelleren Elektronaustausch als undotiertes Graphen. Unabhängige Messungen mittels Raman-Spektroskopie und Hall-Transport bestätigten, wie sich die Ladungsträgerkonzentration im Graphen mit der Schichtdicke änderte, und Fluoreszenzstudien deuteten darauf hin, dass Defekte im Bornitrid bei sehr kleinen Abständen zusätzlichen Ladungstransfer vermittelten. Zusammengenommen stellten diese Experimente eine klare, quantitative Verbindung zwischen dem elektronischen Charakter der Elektrode und der Geschwindigkeit des interfacialen Elektronentransfers her.
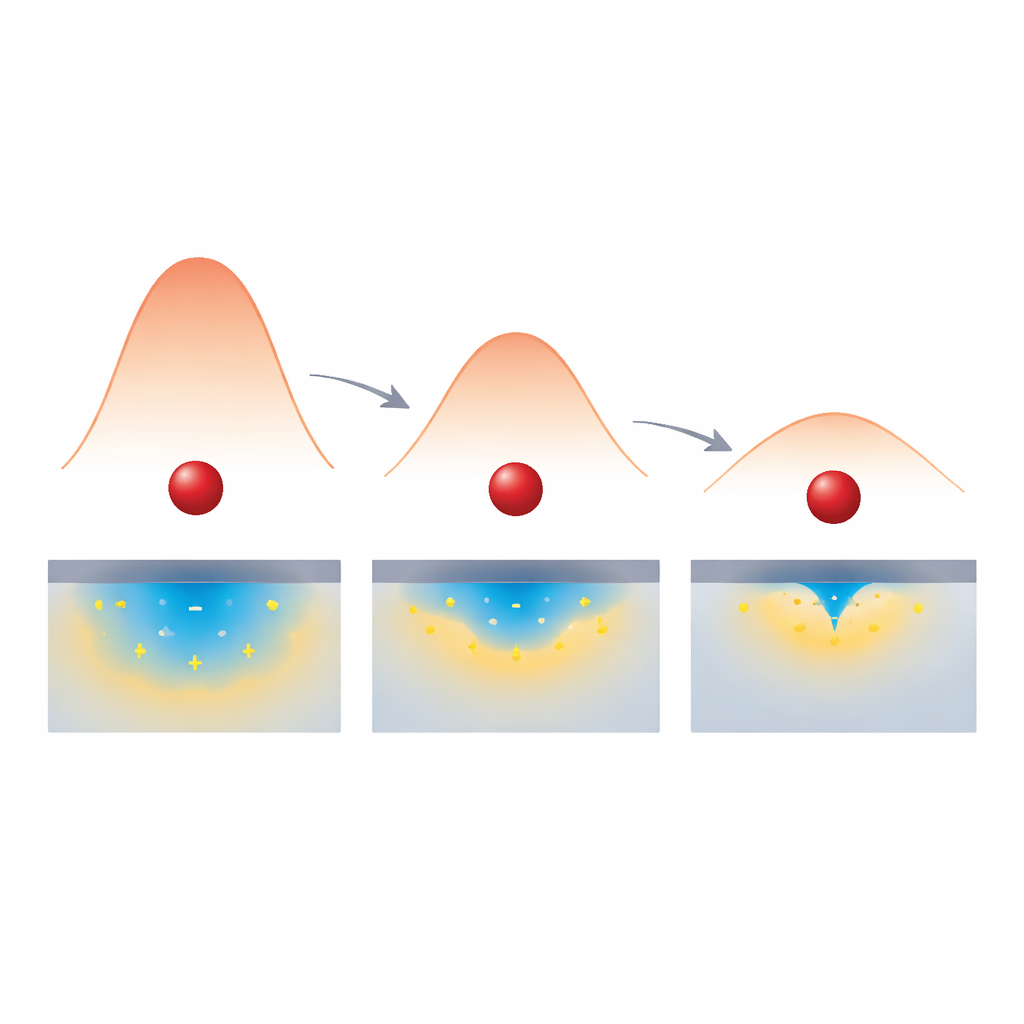
Wie Ladungsabschirmung die Energiekosten senkt
Um zu verstehen, warum der Effekt so stark war, wandten sich die Autorinnen und Autoren der Theorie und Computersimulationen zu. Sie modellierten, wie sich die Elektronen der Elektrode als Reaktion auf ein geladenes Molekül, das sich knapp über der Oberfläche befindet, umverteilen. In einer schlecht metallischen Elektrode mit wenigen Ladungsträgern verteilt sich die induzierte Ladung über einen breiten Bereich und bietet nur eine schwache Stabilisierung des Übergangszustands für den Elektronentransfer. Mit wachsender Ladungsträgerdichte und zunehmender Metallizität wird die induzierte Ladung schärfer und sammelt sich direkt unter dem Molekül, wie eine fokussierte Spiegel-Ladung. Diese stärkere, lokalisiertere Abschirmung senkt die Rekorganisationsenergie: Die Umgebung muss sich weniger verschieben, um ein Elektron zu bewegen, sodass der Energiehügel niedriger wird. Wenn sie diese dichteabhängige Rekorganisationsenergie in ein erweitertes Marcus-ähnliches Modell einbauten, stimmten die Berechnungen mit den experimentellen Ratenänderungen über den gesamten Dotierungsbereich überein, während Modelle mit fester Rekorganisationsenergie stark versagten.
Was das für zukünftige Energie- und Quantenbauteile bedeutet
Die Studie zeigt, dass die elektronische Struktur der festen Elektrode weit mehr tut als nur Elektronen bereitzustellen — sie formt die energetische Landschaft, die Elektronen überqueren müssen. In Systemen mit geringer elektronischer Fülle, wie vielen Halbleitern und atomar dünnen Materialien, kann der zusätzliche Rekorganisationsaufwand durch die Elektrode selbst ebenso groß sein wie der bekannte Beitrag des Lösungsmittels. Wenn die elektronische Beschaffenheit der Elektrode explizit in das Design von Grenzflächen einbezogen wird, können Forschende Elektronentransfer in Batterien, Solarzellen, Katalysatoren und Quantenbauteilen besser vorhersagen und steuern. Kurz: Die Abstimmung darauf, wie gut eine Elektrode Ladung abschirmt, bietet ein wirksames neues Steuerungsinstrument, um Schlüsselreaktionen an Oberflächen zu beschleunigen oder zu verlangsamen.
Zitation: Maroo, S., Coello Escalante, L., Wang, Y. et al. Electronic origin of reorganization energy in interfacial electron transfer. Nature 653, 98–103 (2026). https://doi.org/10.1038/s41586-026-10311-2
Schlüsselwörter: Elektronentransfer, Graphen-Elektroden, Reorganisationsenergie, elektrochemische Grenzflächen, Zustandsdichte