Clear Sky Science · de
Vagale Blutvolumenrezeptoren kompensieren Blutverlust und Lagewechsel
Warum Aufrechtstehen Sie nicht ohnmächtig werden lässt
Jedes Mal, wenn Sie aufstehen, zieht die Schwerkraft plötzlich Blut in Richtung Beine. Den Großteil der Zeit werden Sie dennoch nicht bewusstlos. Diese Studie enthüllt ein verborgenes Sicherheitssystem von Nervenzellen, das konstant registriert, wie voll das Herz mit Blut ist, und dem Gehirn auf der Stelle sagt, den Blutdruck anzupassen. Das Verständnis dieses Systems erklärt, warum manche Menschen beim Aufstehen schwindelig werden und warum starker Blutverlust rasch lebensbedrohlich werden kann.
Verborgene Sensoren, die das Blutvolumen spüren
Das Herz ist von sensorischen Nerven durchzogen, die dem Gehirn laufend berichten, was sich im Brustkorb abspielt. Wissenschaftler kennen seit Jahrzehnten eine große Gruppe, die Barorezeptoren, welche den Blutdruck in großen Arterien messen. Eine andere Gruppe von Sensoren, die auf die tatsächliche Füllung des Herzens reagieren, blieb jedoch rätselhaft. Die Autoren konzentrierten sich auf Nervenzellen im Vagusnerv, die ein mechanisches Sensorprotein namens PIEZO2 tragen. Da PIEZO2 sich beim Dehnen öffnet, waren diese Neurone vielversprechende Kandidaten, um als Volumenmesser des schlagenden Herzens zu fungieren.
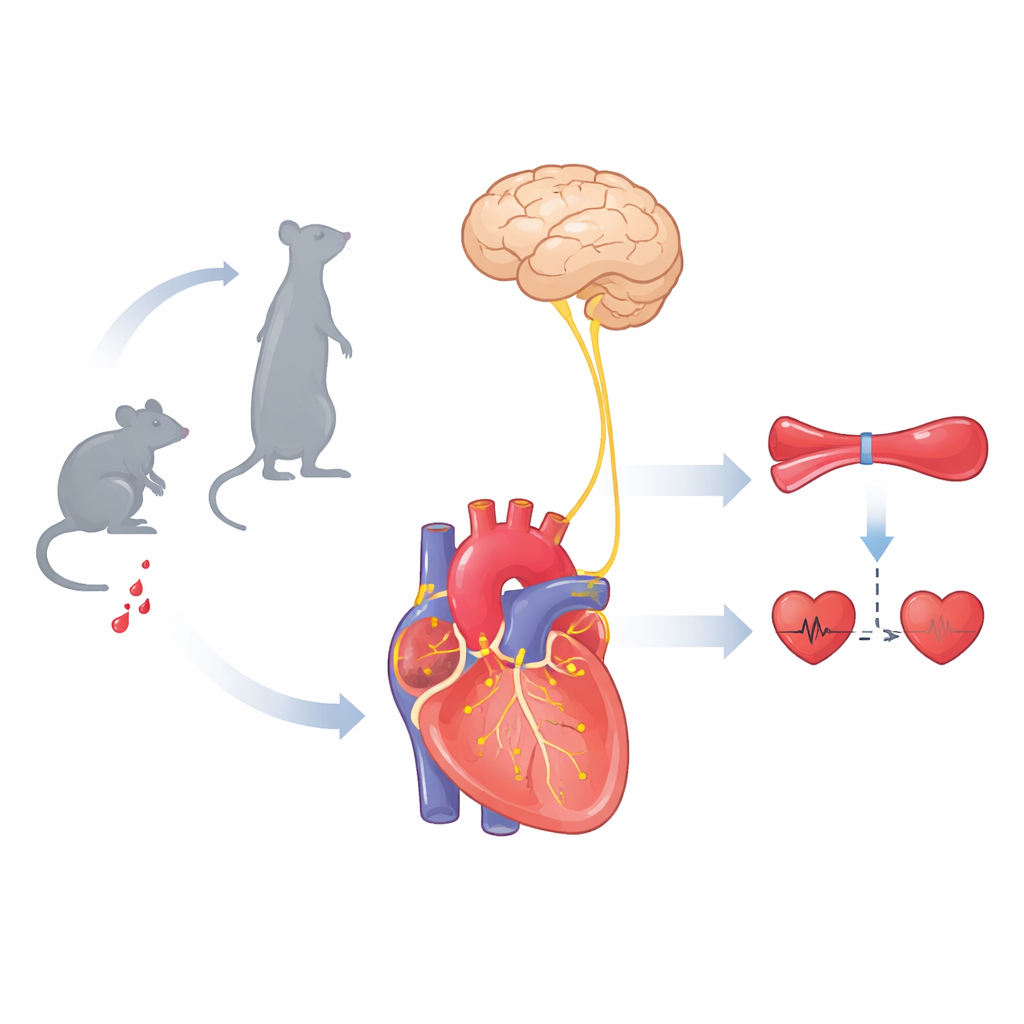
Eine Mausversion des Kippbett‑Tests
Um zu untersuchen, wie verschiedene Sensoren dem Körper beim Lagewechsel helfen, passte das Team den klinischen Kippbett‑Test für Mäuse an. Unter Narkose wurden die Tiere vom Liegen in die aufrechte Position gedreht, während Blutdruck und Herzfrequenz überwacht wurden. Normale Mäuse zeigten beim Aufrichten einen starken Blutdruckabfall, gefolgt binnen Sekunden von einer Erholung und einem anhaltenden Anstieg der Herzfrequenz, wodurch die Durchblutung des Gehirns erhalten blieb. Das Durchtrennen wichtiger Halsnerven, einschließlich des Vagus, beseitigte diese Kompensation und führte zu anhaltend niedrigem Druck. Auffällig war, dass Mäuse, denen genetisch PIEZO2 nur in bestimmten vagalen Sensorneuronen fehlte, ebenfalls nicht richtig wiederherstellten, obwohl ihr klassischer Barorezeptorreflex intakt war. Das zeigte, dass ein zweiter, PIEZO2‑abhängiger Weg entscheidend ist, um den Blutdruck zu stabilisieren, wenn die Schwerkraft das Blut plötzlich nach unten verschiebt.
Kartierung der speziellen Nervenendigungen im Herzen
Die Forscher verfolgten anschließend, wohin die PIEZO2‑tragenden vagalen Neuronen ziehen. Mit Viren, die diese Zellen fluoreszent markieren, erstellten sie dreidimensionale Bilder der Nervenendigungen im Mäuseherz. Sie fanden, dass PIEZO2‑Neuronen charakteristische netzartige "End‑Net"‑Endigungen an Vorhöfen und Ventrikeln bildeten, besonders gehäuft dort, wo Blut aus den großen Venen ins Herz eintritt. Eine andere große vagale Gruppe, markiert durch den Rezeptor NPY2R, bildete sowohl End‑Nets als auch buschigere "Flower‑Spray"‑Endigungen. Als das Team selektiv PIEZO2‑Neuronen im Vagus abtötete, verloren die Mäuse erneut ihre Fähigkeit, den Blutdruckabfall beim Kippen zu korrigieren, während die Eliminierung der NPY2R‑Gruppe dies nicht bewirkte. Damit wurden die PIEZO2‑End‑Nets als die entscheidenden Sensoren für lagebedingte Kontrolle identifiziert und von anderen herzempfindenden Nerven unterschieden.
Dem Nervenverkehr bei jedem Herzschlag zuhören
Als Nächstes zeichneten die Autoren direkt die elektrische Aktivität des Vagusnervs direkt oberhalb des Herzens auf, während sie gleichzeitig das Elektrodiagramm und die Drücke in den Herz‑Kammern verfolgten. Bei gesunden Mäusen sahen sie Impulsbursts, die an zwei präzise Zeitpunkte jedes Herzschlags gekoppelt waren: während der Kontraktion der Vorhöfe und während der Kontraktion der Ventrikel. Bei langsamem Blutentzug schwächten sich diese herzschlaggekoppelten Signale ab; wenn salzhaltige Flüssigkeit zur Volumenausweitung infundiert wurde, wurden die Signale stärker. Kleine Blutverluste beeinflussten die vorhofzeitlich gebundenen Signale am stärksten, was darauf hindeutet, dass diese Sensoren auf frühe Anzeichen zentralen Volumenverlusts abgestimmt sind. Bei Mäusen ohne PIEZO2 oder nach Ablation ihrer PIEZO2‑Neuronen verschwand die herzschlaggekoppelte Aktivität nahezu und änderte sich nicht mehr mit dem Volumen, was beweist, dass PIEZO2 der zentrale Dehnungssensor für diese Rezeptoren ist.
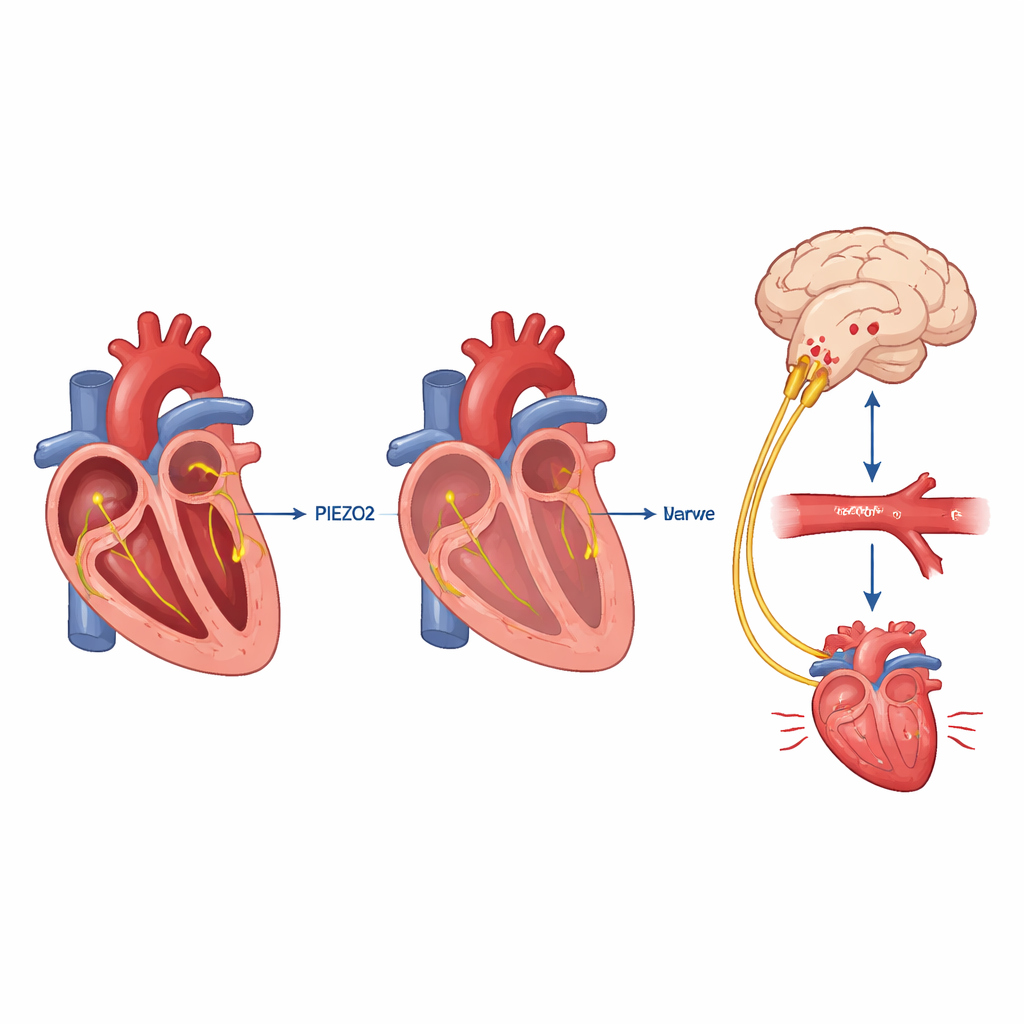
Ein Sicherheitsnetz bei starkem Blutverlust
Die Herzvolumensensoren wirken nicht nur bei Lagewechseln. In einem kontrollierten Schwanzblutungsmodell, das traumatischen Blutverlust nachahmt, hielten normale Mäuse anfangs ihren Blutdruck und erhöhten ihre Herzfrequenz, obwohl sie innerhalb einer halben Stunde etwa ein Viertel ihres Blutes verloren. Mäuse ohne PIEZO2 in vagalen Sensorneuronen bluteten zwar im gleichen Tempo, konnten diese kompensatorische Reaktion jedoch nicht aufbauen: Ihr Blutdruck sackte ab, die Herzfrequenz stieg nicht ausreichend, und sie überlebten deutlich kürzer. Die künstliche Aktivierung von PIEZO2‑vagalen Fasern in Herznähe mittels Licht verursachte bei normalem Volumen einen Blutdruckabfall, was anzeigt, dass das Gehirn den Kreislauf je nach Beladung dieser Rezeptoren hoch- oder herunterregeln kann.
Was das für Gesundheit und Krankheit bedeutet
Zusammen zeigen die Ergebnisse eine dedizierte Gruppe herzbasierter Volumenrezeptoren, die bei jedem Schlag feuern, registrieren, wie viel Blut ins Herz zurückkehrt, und dem Gehirn helfen, die Durchblutung beim Aufstehen und bei Blutverlust stabil zu halten. Anders als Barorezeptoren, die hauptsächlich den Druck in den Arterien melden, berichten diese PIEZO2‑positiven vagalen Neuronen darüber, wie voll das zentrale Blutreservoir ist. Wenn sie funktionieren, können wir aufstehen, etwas Blut verlieren oder andere Herausforderungen bewältigen, ohne sofort ohnmächtig zu werden. Versagen sie, führt das zu orthostatischer Hypotonie und schlechterem Überleben nach großem Blutverlust. Das Verständnis dieses Volumensinneswegs könnte letztlich zu besseren Diagnosen und Therapien für Menschen mit Lage‑schwindel oder zur Stabilisierung von Patienten nach Trauma und Operation führen.
Zitation: Liu, Z., Lu, S., Haskell, I.A. et al. Vagal blood volume receptors compensate for haemorrhage and posture change. Nature 651, 1068–1076 (2026). https://doi.org/10.1038/s41586-025-10010-4
Schlüsselwörter: Vagusnerv, Blutvolumen, orthostatische Hypotonie, PIEZO2, kardiovaskuläre Reflexe