Clear Sky Science · de
Auswirkungen von Fütterungsstrategien auf Kulturleistung und Produktqualität in NISTCHO
Warum die Fütterung von Zellen für moderne Arzneimittel wichtig ist
Monoklonale Antikörper sind zentrale Wirkstoffe in der Behandlung von Krebs und Immunerkrankungen und werden meist in großen Gefäßen mit Hamsterzellen hergestellt. Diese Studie stellt eine einfache, aber wichtige Frage: Wie verändert die zeitliche Versorgung dieser Zellen mit Zucker und Nährstoffen sowohl ihr Wachstum als auch die feinen Eigenschaften der von ihnen produzierten Antikörper? Anhand einer gemeinsamen Referenzzelllinie namens NISTCHO zeigen die Forschenden, wie das Anpassen von Zeitpunkt und Zusammensetzung der Fütterung Leistung und subtile Zuckerprofile beeinflussen kann.
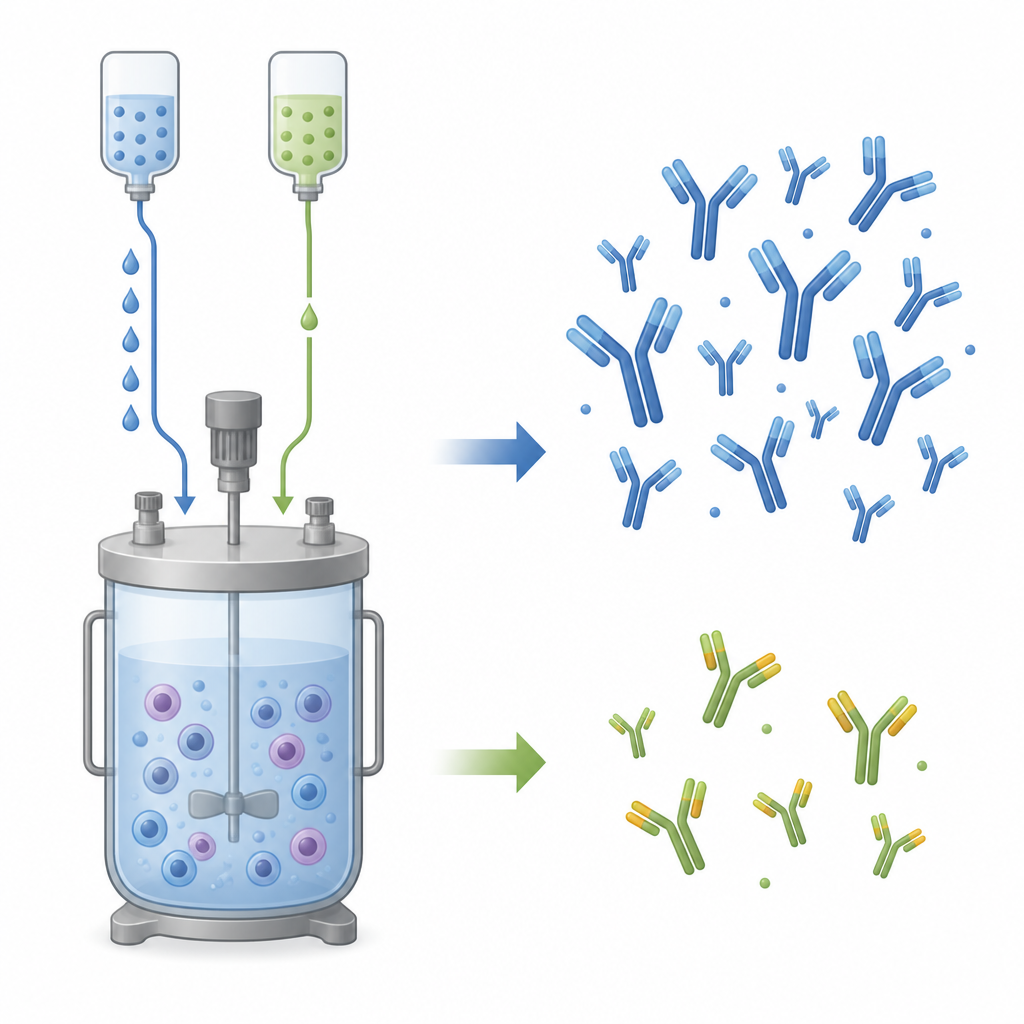
Medizinische Fabriken im Glas wachsen lassen
Das Team arbeitete mit NISTCHO, einer standardisierten Hamsterzelllinie, die ein Modellantikörper namens cNISTmAb produziert. Weil viele Labore dieselben Zellen verwenden können, wird NISTCHO zunehmend zu einem Referenzsystem für den Vergleich von Produktionsverfahren. Die Autoren führten kleine fed‑batch Kulturen durch, bei denen die Zellen etwa elf Tage wachsen, während frische Nährstoffe nach einem festen Plan zugegeben werden. Sie testeten sieben unterschiedliche Fütterungspläne, die sich darin unterschieden, wie viel Glukose zugeführt wurde, wie häufig Nachschub gegeben wurde und ob eine zusätzliche Mischung aus Galactose und Mangan, genannt Gal+, beigemischt wurde.
Wie die Zuckerversorgung Wachstum und Ertrag formt
Glukose, die Hauptenergiequelle, erwies sich als stärkster Treiber für Zellwachstum und Antikörperertrag. Wenn alle zwei Tage ausreichend Glukose zugegeben wurde, blieben die Zellen gesund, erreichten hohe Zelldichten und erzielten die höchsten Antikörpertiter. Wurde die Glukosezufuhr halbiert, ging der Treibstoff früher aus, die Zellzahlen fielen schnell und die Antikörperproduktion stagnierte. Ein alternativer Plan mit kleineren, dafür häufigeren Glukosegaben reduzierte die Anreicherung von Abbauprodukten, verringerte aber ebenfalls die Produktivität — wahrscheinlich weil der Zucker über längere Zeit nahe der unteren Grenze lag, die die Zellen effizient nutzen können.
Feinabstimmung der Zucker auf Antikörpern
Antikörper tragen kurze Zuckerketten, die beeinflussen, wie lange sie im Körper verbleiben und wie stark sie das Immunsystem ansprechen. Die Forschenden maßen diese Zucker sorgfältig und verwendeten statistische Werkzeuge, die sonst in großen Datensätzen eingesetzt werden. Sie fanden heraus, dass sowohl die Verweildauer in Kultur als auch die Fütterungsstrategie die Zuckerprofile prägten. In allen Bedingungen zeigten spätere Proben vermehrt bestimmte Zucker, darunter Fucose, und weniger Varianten ohne dieses Zuckerstück — Veränderungen, die einige Immunfunktionen verringern könnten. Die Zugabe der Gal+‑Mischung erhöhte durchgängig den Galactoseanteil an den Antikörperzuckern, eine Änderung, die bekanntlich eine Form der Immunaktivität stärkt, ohne das Zellwachstum zu beeinträchtigen.
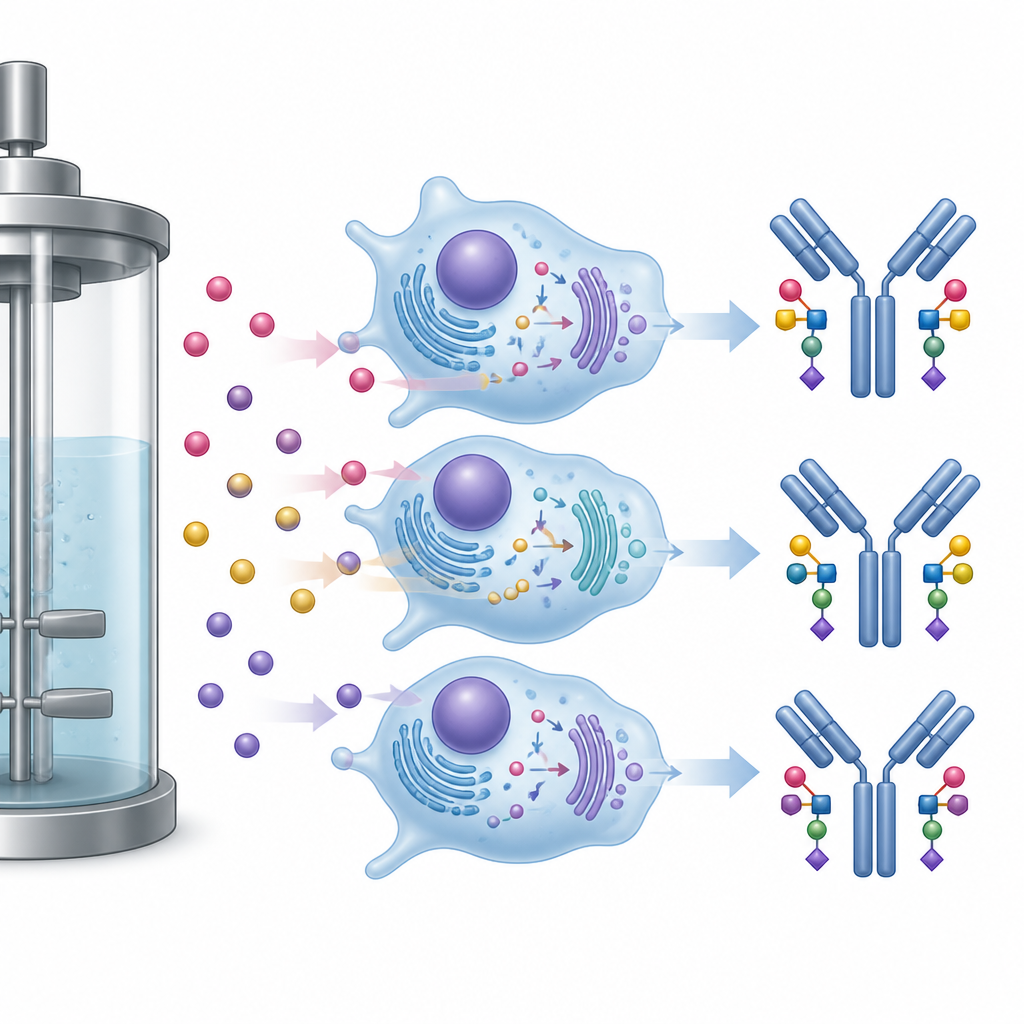
Verborgene Effekte von Zucker‑Spitzen auf Nebenreaktionen
Glukose im Medium kann sich außerdem nicht‑enzymatisch an Antikörper anlagern — eine Reaktion, die als Glykation bezeichnet wird und die Eigenschaften leicht verändern sowie die Analyse erschweren kann. Die Studie zeigte, dass Fütterungshäufigkeit und verbleibende Glukosespiegel beeinflussten, wie viel Glykation während der schnellen Wachstumsphase auftrat. Strategien mit täglicher Glukosezugabe führten frühzeitig eher zu mehr glykatierten Antikörpern, vermutlich weil mehr freier Zucker im Medium vorhanden war, verteilt auf weniger Zellen. Gegen Ende der Kultur glichen sich diese Unterschiede jedoch an, und die Gesamtglykation blieb niedrig, etwa bei fünf Prozent, über alle Strategien hinweg.
Was das für die Herstellung besserer Biopharmazeutika bedeutet
Insgesamt zeigen die Ergebnisse, dass allein die Änderung von Art und Zeitpunkt der Nährstoffzugabe sowohl Menge als auch Qualität der von NISTCHO‑Zellen hergestellten Antikörper lenken kann. Eine hohe, aber kontrollierte Glukosezufuhr unterstützt starke Produktivität, während das Gal+‑Supplement verlässlich den Galactosegehalt an den Antikörperzuckern erhöht und den Zellen unter kargeren Bedingungen hilft zu überleben. Da NISTCHO ein öffentliches Referenzsystem ist, liefern diese Befunde Herstellern und Forschenden eine gemeinsame Orientierung, um Fütterungsstrategien so anzupassen, dass Antikörper‑Zuckerprofile feinjustiert werden können, ohne unerwünschte Veränderungen wie übermäßige Fucosylierung und Glykation zu fördern.
Zitation: Schäpertöns, V., Hofer, L., Berger, T. et al. Effects of feeding strategies on culture performance and product quality in NISTCHO. npj Syst Biol Appl 12, 67 (2026). https://doi.org/10.1038/s41540-026-00686-3
Schlüsselwörter: Produktion monoklonaler Antikörper, CHO‑Zellkultur, Glykosylierung, bioprozesstechnische Fütterungsstrategie, NISTCHO