Clear Sky Science · de
StimVision: Smartphone-Video-Kinematik zur Optimierung der DBS‑Programmierung bei Parkinson
Alltägliche Telefone als Werkzeuge zur Feinabstimmung des Gehirns
Für Menschen mit Parkinson kann die tiefe Hirnstimulation (DBS) das Leben verändern, doch die Suche nach den optimalen Einstellungen für jede Person bleibt ein langsamer, trial‑and‑error‑Prozess. Diese Studie stellt „StimVision“ vor, eine Methode, die nur eine handelsübliche Smartphone‑Kamera und intelligente Algorithmen nutzt, um die Bewegungen eines Patienten zu beobachten und schnell vorzuschlagen, welche DBS‑Einstellung am besten wirkt. Der Ansatz verspricht, die Hirnstimulation präziser, objektiver und potenziell leichter in gewöhnlichen Kliniken oder sogar zu Hause anwendbar zu machen.
Warum das Feinabstimmen von Hirnimplantaten so schwierig ist
DBS wirkt, indem es winzige elektrische Impulse an tiefe Hirnregionen sendet, um Bewegungsprobleme wie Verlangsamung und Steifheit zu lindern. Heute passen Ärztinnen und Ärzte diese Impulse meist nach Augenmaß an und stützen sich auf kurze Untersuchungen und Bewertungsskalen, um einzuschätzen, ob sich die Bewegungen eines Patienten etwas verbessert oder verschlechtert haben. Da moderne DBS‑Systeme immer mehr einstellbare Parameter bieten, wird dieser Prozess zunehmend anspruchsvoll und subjektiv. Klinikerinnen und Kliniker fehlt eine einfache, quantitative Methode, um viele mögliche Programme innerhalb eines einzelnen Besuchs zu vergleichen und zu wissen, welches davon wirklich den größten Nutzen bringt.
Die Hand beobachten, um das Gehirn zu lesen
Die Forscherinnen und Forscher stellten das Problem als Auswahlaufgabe neu: Gegeben mehrere DBS‑Einstellungen, welche erzeugt in diesem Moment für diese Person die beste Bewegung? Fünfzehn Menschen mit Parkinson und DBS‑Implantaten führten eine einfache Handöffnungs‑ und -schließbewegung aus – dieselbe Bewegung, die bereits in klinischen Untersuchungen verwendet wird – während sie mit einer Smartphone‑Kamera mit 60 Bildern pro Sekunde gefilmt wurden. Mithilfe eines Open‑Source‑Computer‑Vision‑Werkzeugs verfolgte das Team die Position der Hand ohne Marker und verwandelte das Video in ein präzises Signal, das beschreibt, wie sich die Finger über die Zeit öffneten und schlossen. Aus diesem Signal extrahierten sie 23 numerische Merkmale, die erfassen, wie groß, wie schnell, wie regelmäßig und wie stabil die Bewegungen waren, etwa mittlere Geschwindigkeit, Zyklusfrequenz und wie sehr die Bewegung innerhalb der kurzen Sequenz verlangsamte.
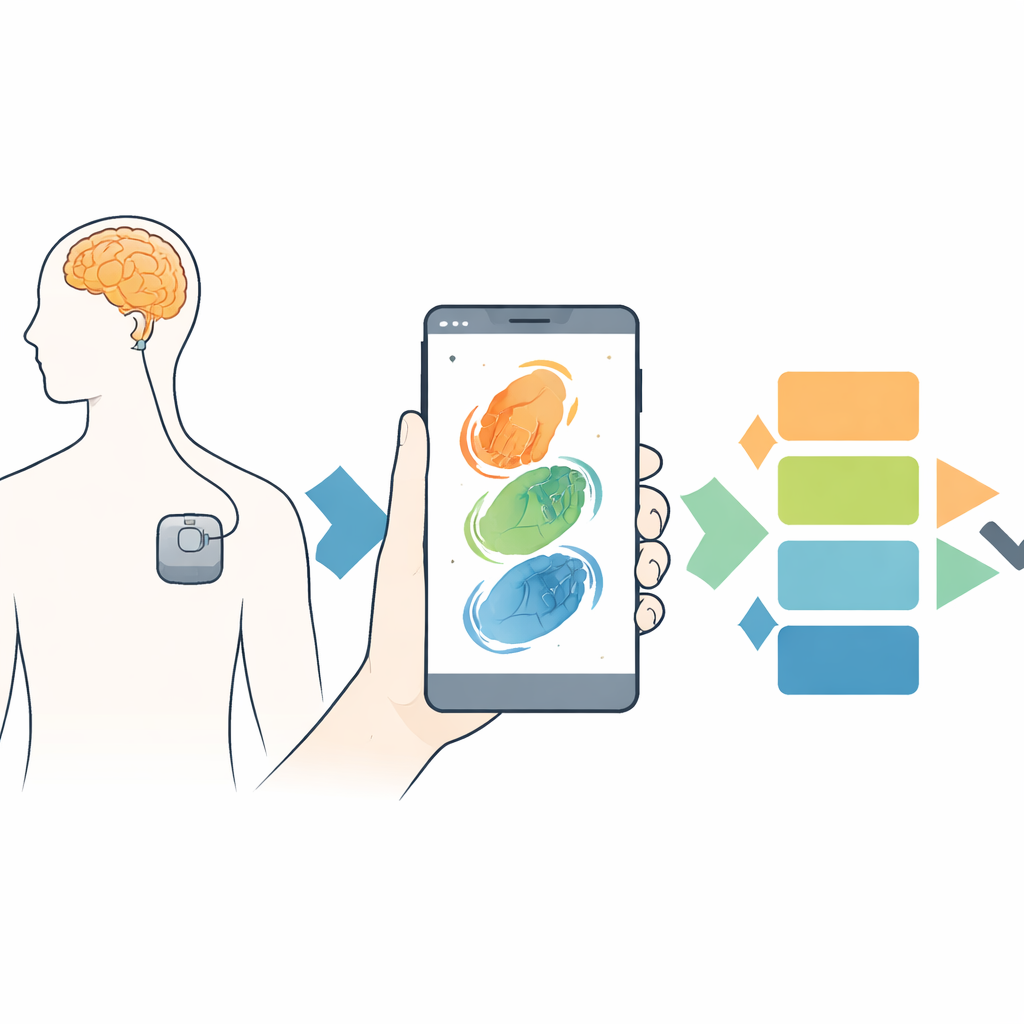
Bewegung in eine objektive Punktzahl verwandeln
Um DBS‑Einstellungen zu vergleichen, erfand das Team eine patientenspezifische Metrik namens Dynamically Weighted Improvement Score (DWIS). Für jede Person berechnete die Software zunächst, wie sehr sich jedes der 23 Bewegungsmerkmale im Vergleich zum ausgeschalteten DBS verbesserte oder verschlechterte, wobei die Werte immer so ausgerichtet wurden, dass höhere Zahlen bessere Bewegungen bedeuten. Anschließend identifizierte sie, welche Merkmale zwischen den Programmen am stärksten variierten — diese galten als am informativsten für den jeweiligen Patienten — und vergab ihnen automatisch ein größeres Gewicht. Durch Summieren der gewichteten Verbesserungen erzeugte das System für jede DBS‑Einstellung eine einzelne zusammengesetzte Punktzahl und ordnete alle Programme innerhalb der Sitzung. Bei allen Patientinnen und Patienten identifizierte StimVision jeweils ein deutlich bestes Programm, und diese Rangfolge blieb stabil, selbst wenn die Gewichtungsmethode verändert wurde, was darauf hindeutet, dass der Ansatz robust ist und nicht übermäßig empfindlich gegenüber Feinjustierungen reagiert.
Wie bessere Bewegung tatsächlich aussieht
Verglichen mit dem DBS‑aus‑Zustand fanden die Forschenden bei der bestbewerteten Einstellung eines jeden Patienten umfassende Verbesserungen. Die meisten getesteten Programme halfen in gewissem Maße, doch die am höchsten gerankten erzeugten ausgeprägte Effekte. Die stärksten Effekte betrafen eine Zunahme von Bewegungsgeschwindigkeit und Rhythmus: Hände öffneten und schlossen sich schneller, mit höherer mittlerer Geschwindigkeit und schnelleren Schließphasen, und die Bewegungen blieben über den kurzen Versuch hinweg konsistenter statt nachzulassen oder langsamer zu werden. Mittels einer statistischen Technik, die verwandte Merkmale gruppiert, stellte das Team fest, dass sich die vielen Messgrößen in drei Hauptthemen oder „Domänen“ verdichten lassen: Bewegungsgeschwindigkeit, Bewegungs‑Konsistenz und Rhythmus & Timing. Sie verglichen dieses DBS‑„Signatur“ anschließend mit Daten einer früheren Studie zum gängigen Parkinson‑Medikament Levodopa. Beide Behandlungen zeigten ähnliche Muster bei Geschwindigkeit und Konsistenz, unterschieden sich jedoch bei timingbezogenen Merkmalen, was darauf hindeutet, dass elektrische und medikamentöse Therapien teilweise über gemeinsame Pfade wirken, aber das feine Timing der Bewegung unterschiedlich formen.
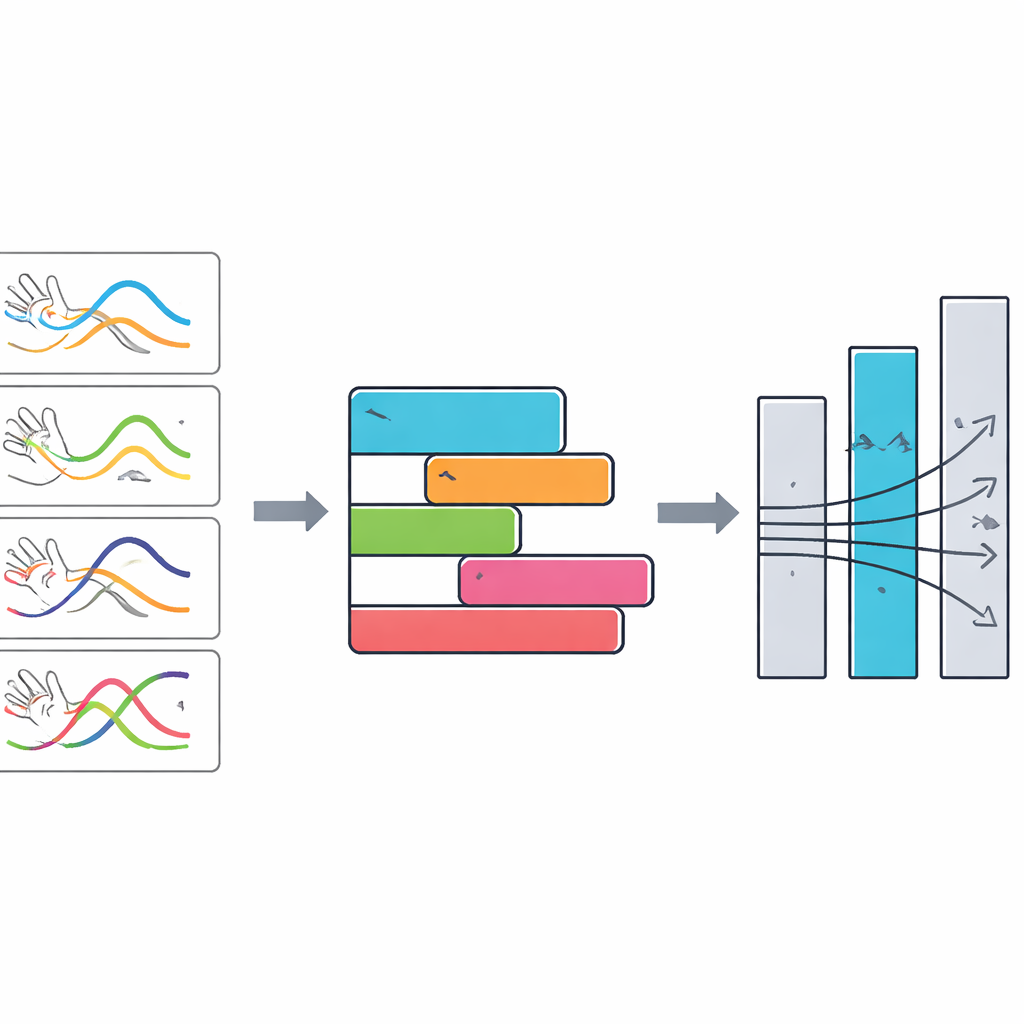
Den Computer an das Auge der Klinik anpassen
Damit eine neue Messung in der Medizin nützlich ist, muss sie mit dem übereinstimmen, was Klinikerinnen und Kliniker bereits als bedeutsame Verbesserung erkennen. Die Forschenden prüften daher, wie DWIS mit den Bewertungen einer standardisierten klinischen Skala für Handbewegungen zusammenhängt, beurteilt von Neurologinnen und Neurologen, die die Ergebnisse des Algorithmus nicht kannten. Über alle getesteten Programme hinweg korrelierten höhere DWIS‑Werte stark mit besseren klinischen Bewertungen, selbst nach Berücksichtigung des Ausgangsgrades der Handfunktion. Das deutet darauf hin, dass die smartphonebasierte Punktzahl nicht nur mathematischen Rauschen erfasst, sondern mit Expertenurteilen übereinstimmt und gleichzeitig eine feinere und reproduzierbarere Messung liefert, als das bloße Auge sehen kann.
Was das für Patientinnen und Patienten bedeuten könnte
Obwohl diese Machbarkeitsstudie nur 15 Personen umfasste und sich auf eine einzelne Handaufgabe konzentrierte, weist sie in eine Zukunft, in der die DBS‑Programmierung durch schnelle, objektive Messungen geleitet wird, die mit Alltagsgeräten erfasst werden. StimVision könnte Klinikerinnen und Klinikern helfen, sich im wachsenden Dschungel von Stimulationsparametern besser zurechtzufinden, die Zeit für trial‑and‑error‑Anpassungen zu verkürzen und schließlich Fernbewertungen außerhalb des Krankenhauses zu unterstützen. Indem es Ärztinnen und Ärzten ein klares, datenbasiertes Bild davon liefert, wie jedes DBS‑Programm Geschwindigkeit, Stabilität und Rhythmus der Bewegung beeinflusst — und indem es eine gemeinsame Sprache bietet, um Hirnstimulation mit Medikamenten zu vergleichen — könnte der Ansatz letztlich dazu beitragen, die Parkinson‑Behandlung präziser auf die Bedürfnisse des einzelnen Menschen abzustimmen.
Zitation: Lange, F., Köberle, P., Adaçay, G. et al. StimVision: smartphone video kinematics to optimize DBS programming in Parkinson’s disease. npj Parkinsons Dis. 12, 100 (2026). https://doi.org/10.1038/s41531-026-01335-6
Schlüsselwörter: Morbus Parkinson, Tiefe Hirnstimulation, Smartphone‑Video, motorische Kinematik, Computer Vision