Clear Sky Science · de
Glukoseabhängige Versauerungsstrategie von Nektarbewohnenden Bakterien vermittelt das Aufplatzen von Pollensäcken
Blütenzucker als verstecktes Schlachtfeld
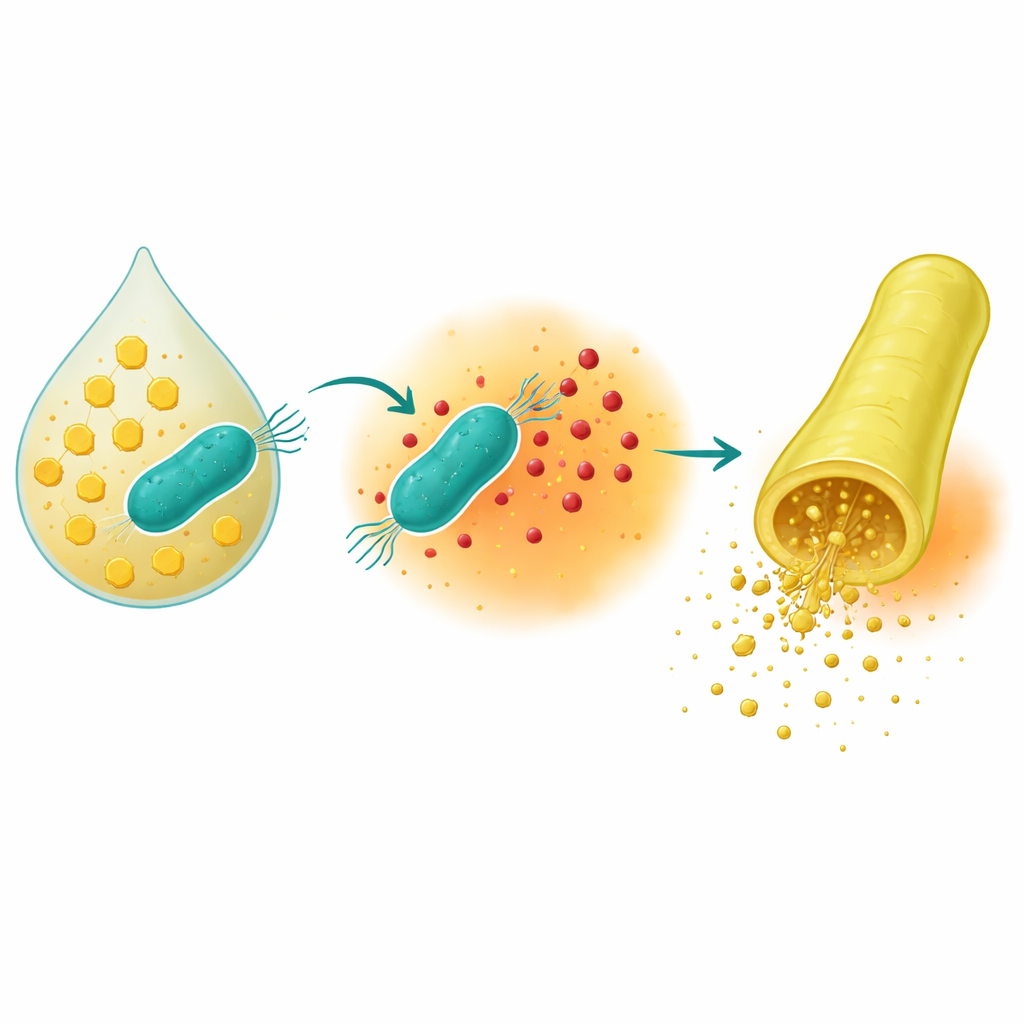
Blütennektar gilt meist als einfache süße Belohnung für Bestäuber, doch er ist zugleich ein dicht bevölkertes Habitat, in dem Mikroben heftig konkurrieren. Diese Studie zeigt, wie einige nektarbewohnende Bakterien den Zucker im Nektar nutzen, um dessen Chemie zu verändern, Pflanzenpollenröhren zum Aufplatzen zu bringen und so an eine reichhaltige Nahrungsquelle zu gelangen, die zuvor verschlossen war. Dadurch wird eine kleine, aber wichtige Ecke der Natur umgestaltet.
Süßer Nektar mit fehlendem Baustein
Nektar ist voller Zucker, die Bienen, Schmetterlinge und andere Besucher anlocken, enthält jedoch wenig Stickstoff, einen Schlüsselbaustein für den Proteinaufbau und Wachstum. Bakterien, die mit Bestäubern in den Nektar gelangen, können sich schnell vermehren und diesen zu einem Miniaturökosystem machen. Frühere Arbeiten zeigten, dass bestimmte blütenassoziierte Bakterien Pollen zum Keimen bringen und dann zum Platzen bringen können, sodass deren nahrhafte Inhalte in den Nektar auslaufen. Das deutete auf eine clevere Strategie hin: den eigenen Blütenpollen als Düngerquelle zu nutzen. Die vorliegende Studie wollte herausfinden, welche Substanz diese Bakterien produzieren, um das Platzen der Pollenröhren auszulösen, und wie dieser Trick in ihrer Biologie verankert ist.

Zucker in Säure verwandeln, um Pollen zu knacken
Die Forschenden isolierten Stämme von Acinetobacter-Bakterien aus den Nektardrüsen Zierpflanzen und mischten die Bakterienkulturflüssigkeit mit keimendem Pollen mehrerer Pflanzenarten. Wenn die Bakterien in Lösungen mit Saccharose oder Glukose gewachsen waren, ließ die zugegebene Flüssigkeit die Pollenröhren dramatisch aufreißen, während Lösungen ohne Zucker oder mit Fruktose das nicht taten. Messungen zeigten, dass die zuckergefütterten Bakterien das umgebende Medium stark ansäuerten, auf etwa pH 3, und dass das einfache Neutralisieren dieser Säure das Aufplatzen stoppte. Mittels Gaschromatographie–Massenspektrometrie identifizierte das Team Gluconsäure als die Hauptsäure, die nur vorhanden war, wenn Glukose oder Saccharose verfügbar waren. Die Zugabe gereinigter Gluconsäure allein, in Mengen, die den pH-Wert unter etwa 3,8 senkten, war ausreichend, um Pollenröhren zum Platzen zu bringen, womit bestätigt wurde, dass dieser säuregetriebene pH-Abfall der entscheidende Auslöser ist.
Eine eingebaute molekulare Maschine zur Säureproduktion
Um aufzudecken, wie die Bakterien Gluconsäure herstellen, sequenzierten die Autorinnen und Autoren das vollständige Genom eines Acinetobacter nectaris-Stamms. Sie konzentrierten sich auf Gene, die pyrrolochinolinchinon (PQQ)-abhängige Dehydrogenasen kodieren, eine Enzymfamilie, die in anderen Mikroben dafür bekannt ist, Glukose an der Zelloberfläche zu oxidieren. Durch Übertragung von Kandidatengenen in einen Laborstamm von Escherichia coli, der normalerweise ohne Hilfe keine Gluconsäure herstellen kann, fanden sie, dass ein A. nectaris-Gen die Fähigkeit wiederherstellte, Glukose in Gluconsäure zu verwandeln und das Medium zu versauern — jedoch nur, wenn das Cofaktor-Molekül PQQ zugeführt wurde. Das zeigte, dass das Nektarbakterium eine funktionelle PQQ‑abhängige Glukosedehydrogenase besitzt, die Glukose aus dem Nektar direkt mit Säureproduktion verknüpft. Weitere Genomvergleiche ergaben, dass viele Acinetobacter-Arten verwandte Enzyme besitzen, nektarbewohnende Stämme aber konsequent auch einen vollständigen Satz von PQQ-bildenden Genen tragen, was auf einen starken evolutionären Druck hindeutet, diesen Säureproduktionsweg intakt zu halten.
Schnelle Reaktion auf Zucker in einer konkurrenzbetonten Welt
Das Team untersuchte anschließend, ob die Bakterien dieses System je nach angetroffenem Zucker anpassen. Mit RNA-Sequenzierung maßen sie, wie stark die PQQ-bezogenen Gene in A. nectaris unter Wachstum mit verschiedenen Zuckern oder ohne Zucker hochreguliert wurden. Während die meisten Gene des Weges sich wenig veränderten, wurde das Gen, das das winzige PQQ-Vorläuferpeptid pqqA kodiert, deutlich stärker hochgefahren, wenn Glukose oder Saccharose vorhanden waren — am stärksten bei Glukose. Dieses Muster legt nahe, dass diese Bakterien, sobald sie in ein Nektarpool mit einfachen Zuckern eintreten, schnell die PQQ-Produktion hochfahren und damit die Glukosedehydrogenase befähigen, Gluconsäure zu produzieren. Die daraus resultierende Versauerung erschließt nicht nur Stickstoff und andere Nährstoffe aus dem Pollen durch das Aufplatzen seiner Röhren, sondern kann auch das Wachstum konkurrierender Mikroben verlangsamen und diesen Bakterien einen Vorsprung im Wettlauf um die Dominanz im Nektar verschaffen.
Warum dieses kleine Drama wichtig ist
Einfach gesagt zeigt diese Studie, dass einige im Nektar lebende Bakterien eine schnelle chemische Strategie entwickelt haben: Sie verwenden den Zucker der Blüte, um Säure zu bilden, die Säure sprengt Pollenröhren auf, und die ausgeschütteten Polleninhalte nähren die Bakterien und verändern zugleich die Nektarumgebung. Weil die Nektarchemie beeinflussen kann, welche Bestäuber kommen und wie sie sich verhalten, und weil ähnliche säurebildende Mikroben weit verbreitet sein könnten, könnte dieser mikroskopische Tauziehen Auswirkungen auf Pflanzenvermehrung, Bestäuberdiäten und sogar die Zusammensetzung von Honig haben. Was wie einfache Blütensüße aussieht, ist in Wahrheit die Bühne für eine hochentwickelte bakterielle Strategie, die darauf zugeschnitten ist, in einem einzigen Nektartropfen zu überleben und zu gedeihen.
Zitation: Kato, Y., Miura, H., Takayama, S. et al. Glucose-dependent acidification strategy by nectar-dwelling bacteria mediates pollen tube burst. Nat Commun 17, 4105 (2026). https://doi.org/10.1038/s41467-026-72617-z
Schlüsselwörter: Nektarmikroben, Aufplatzen von Pollenröhren, Gluconsäure, Acinetobacter-Bakterien, Blütenmikrobiom