Clear Sky Science · de
Die Vaults assoziieren in situ mit Membranen
Geheimnisvolle Zellkäfige bekommen eine neue Rolle
In unseren Zellen befinden sich zahllose winzige Maschinen, von denen viele gut verstanden sind. Eine der größten, die Vault genannt wird, hat Biologen seit Jahrzehnten ratlos gemacht. Sie ähnelt einem hohlen Fass und kommt bei vielen Organismen, einschließlich des Menschen, überraschend häufig vor, doch ihre Aufgabe blieb unklar. Diese Studie schaut Vaults direkt in lebenden Zellen nach und deckt zwei überraschende Verhaltensweisen auf: Einige Vaults heften sich an innere Membranen, und einige packen Ribosomen, die Proteinfabriken der Zelle, sorgfältig in ihr hohles Inneres.
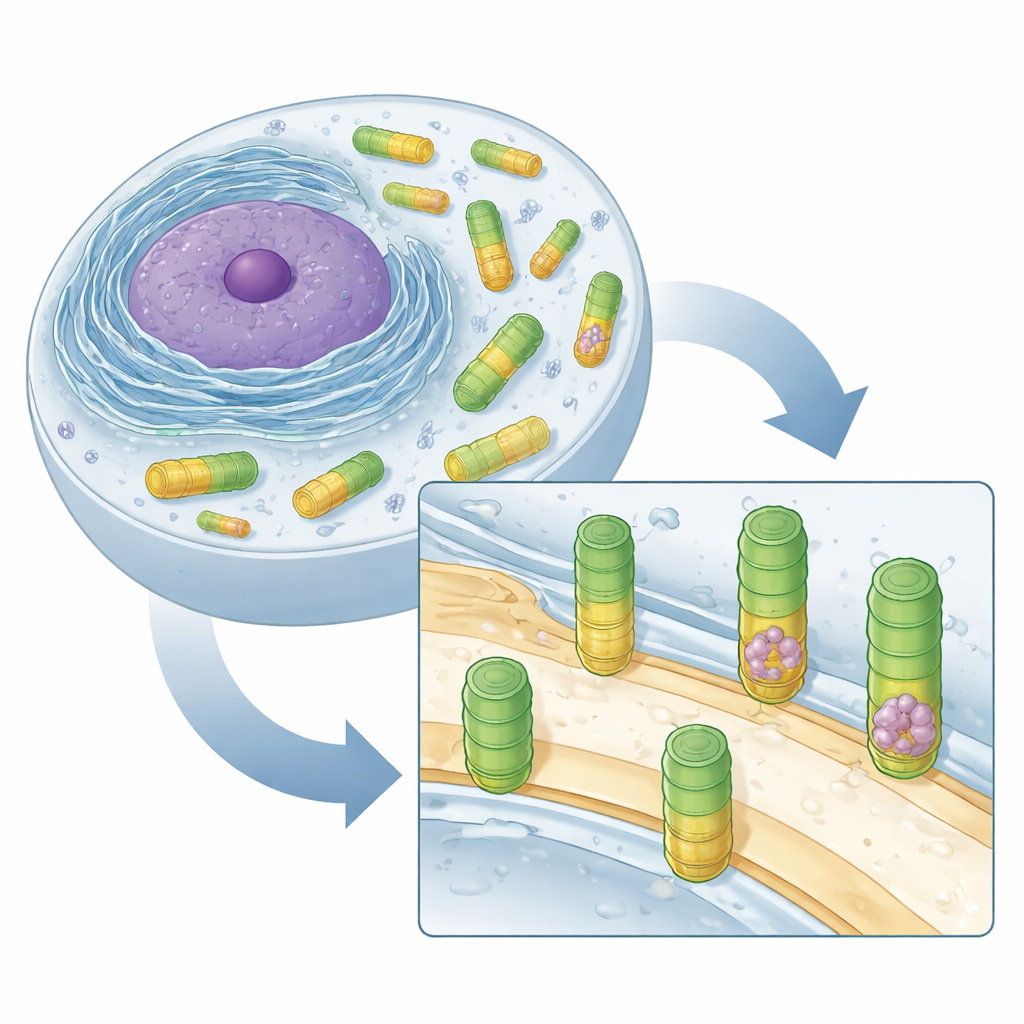
Verborgene Fässer im Zellinneren
Die Forscher konzentrierten sich auf amöbenähnliche Zellen von Dictyostelium discoideum, einem etablierten Modellorganismus, dessen Vaults denen von Tieren stark ähneln. Mithilfe der Kryo‑Elektronentomographie, einer Technik, die Zellen einfriert und in 3D mit Nanometerauflösung abbildet, durchsuchten sie Hunderte von Regionen rund um den Zellkern. Automatisierte Mustererkennung und detailliertes Mittelwertbilden vieler Aufnahmen zeigten Vaults als langgestreckte, fußballförmige Fässer im Zytosol, der Flüssigkeit, die die Zelle ausfüllt. Diese Fässer stimmten in Größe und Form mit zuvor in Ratten und Menschen beschriebenen Vaults überein, was darauf hindeutet, dass die Struktur der Vaults während der Evolution erhalten wurde und auf eine wichtige, wenn auch noch unbekannte Funktion hinweist.
Überraschung: Vaults haften an Membranen
Während die meisten Vaults frei schwammen, wurde eine kleine, aber auffällige Minderheit – etwa 1 bis 2 Prozent – an Membranen des endoplasmatischen Retikulums (ER) und der Kernhülle gefunden, den beiden großen Membransystemen, die den Zellkern umgeben und benachbart sind. Diese angehefteten Vaults standen stets aufrecht und berührten die Membran an einem spezifischen „Gürtel“ entlang des Fasses, nicht an den Enden. Die oberen zwei Drittel des Fasses ragten ins Zytosol hinein, während das untere Drittel in den Bildern umgeordnet oder weniger sichtbar schien, was darauf hindeutet, dass sich ein Teil des Vaults beim Binden an die Membran verformen könnte. Diese konsistente Andockhöhe spricht für eine definiert ausgeformte Kontaktstelle und nicht für zufälliges Festkleben.
Aufweichen und Formen der Membran
Membranen sind nicht bloß passive Hintergründe; ihre Dicke und Krümmung beeinflussen das Verhalten von Proteinen. Das Team maß diese Eigenschaften genau an den Stellen, an denen Vaults ansetzten. Sie fanden, dass der Membranbereich direkt unter dem Vault dünner war als die Umgebung und eine kreisförmige Zone verringerter Dicke bildete. An der Kante, wo das Vault anlag, bildete die Membran einen dickeren „Ring“ und ihre Oberfläche bog sich nach innen, als sei sie vom Fass leicht eingedrückt worden. Diese Merkmale ähneln speziellen Membran‑Mikrodomainen, die von anderen, verwandten Proteinen gebildet werden und dafür bekannt sind, Membranen umzubauen und ihre Qualität zu kontrollieren. Die Beobachtungen legen nahe, dass Vaults ungewöhnliche Membranabschnitte erkennen oder erzeugen könnten, etwa im Dienst der zellulären Instandhaltung.
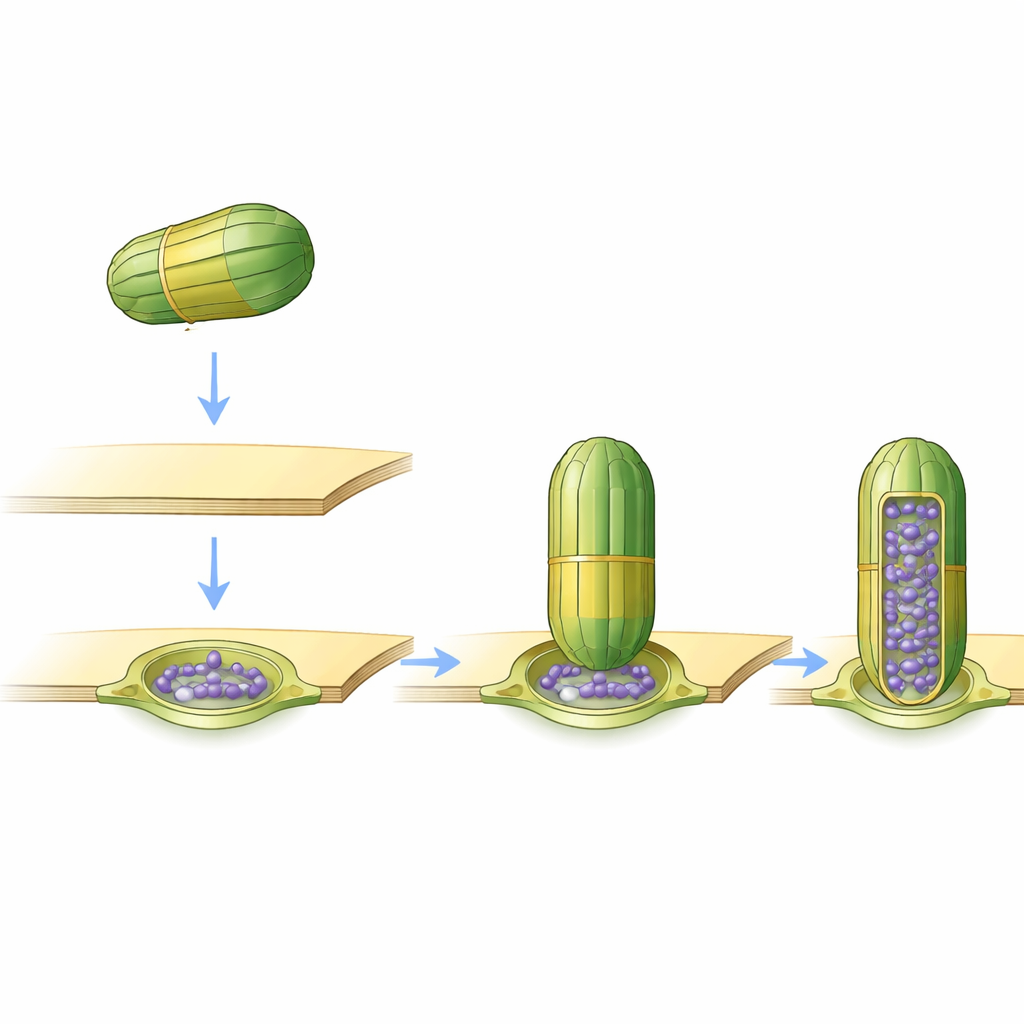
Vaults als Ribosomen‑Träger
Eine weitere Überraschung lag im Inneren der Vaults selbst. Viele Vaults enthielten Ribosomen – große Komplexe, die Proteine synthetisieren – ordentlich in dem Fass verstaut. Durch Überlagern der Vault‑Positionen mit zuvor in denselben Zellen kartierten Ribosomen fanden die Autoren 84 Ribosomen, die vollständig von Vaults umschlossen waren. Fast alle davon waren komplette 80S‑Ribosomen, die funktionale Form in eukaryotischen Zellen, und nicht nur Teiluntereinheiten. In frei schwimmenden Vaults waren die Ribosomen hochgradig geordnet ausgerichtet, wobei der Kanal, durch den neue Proteine freigesetzt werden, zur Innenwand des Vaults zeigte. In den wenigen Vaults, die sowohl membrangebunden als auch ribosomengefüllt waren, saßen einige Ribosomen in einer Orientierung, die an Ribosomen erinnert, die mit der ER‑Membran interagieren, was auf eine mögliche Verbindung zur Proteinsynthese nahe dem ER hindeutet.
Ein Netzwerk von Partnern nachzeichnen
Um zu prüfen, ob diese strukturellen Momentaufnahmen echte, wiederkehrende Partnerschaften widerspiegeln, verwendeten die Forscher einen Proximity‑Labeling‑Ansatz. Sie fusionierten ein Vault‑Protein mit einem Enzym, das nahegelegene Proteine mit Biotin markiert, zogen dann alle markierten Partner heraus und identifizierten diese mittels Massenspektrometrie. Hunderte Proteine waren in der Nähe von Vaults angereichert, darunter viele ribosomale Proteine und mehrere Bewohner der ER‑Membran oder ihres Innenraums. Bekannte Vault‑assoziierte Faktoren, wie bestimmte Enzyme und ein mit der Telomerase verknüpftes Protein, tauchten ebenfalls auf. Zusammen mit den Bilddaten stärkt diese biochemische Karte die Ansicht, dass zumindest eine Untergruppe von Vaults Zeit am ER verbringt und in engem Kontakt mit Ribosomen steht.
Hinweise auf ein langjähriges zelluläres Rätsel
Obwohl die Arbeit noch keine einzige, endgültige Funktion für Vaults enthüllt, liefert sie wichtige Hinweise. Vaults können selektiv an veränderte Membranabschnitte binden, dabei einen Teil ihrer Hülle umordnen und Ribosomen in präzisen Orientierungen verkapseln. Dieses Verhalten legt nahe, dass Vaults helfen könnten, die Proteinfertigungsmaschinerie am ER zu überwachen oder aufzuräumen, oder beim Entfernen beschädigter Komponenten aus spezifischen Membranbereichen assistieren. Da Vaults hochkonserviert sind und mit Krebsmedikamentenresistenz sowie Stressreaktionen in Verbindung gebracht wurden, könnte das Verständnis dieses neu entdeckten membrangebundenen und ribosomen‑tragenden Verhaltens schließlich aufklären, wie Zellen mit Schäden und Veränderungen umgehen – und wie Vaults in der Medizin genutzt oder gezielt werden könnten.
Zitation: Geißler, K., Kreysing, J.P., Wang, Y. et al. The vault associates with membranes in situ. Nat Commun 17, 3659 (2026). https://doi.org/10.1038/s41467-026-71837-7
Schlüsselwörter: Vault-Partikel, Zellmembranen, Ribosomen, Cryo-Elektronentomographie, Endoplasmatisches Retikulum