Clear Sky Science · de
Oxidation von Kohlenmonoxid erweitert die bekannte Stoffwechselkapazität in anaeroben methanotrophen Konsortien
Leben auf dem dunklen Meeresboden
Tief unter der Meeresoberfläche, in kaltem, sauerstofffreiem Schlamm, arbeiten winzige Partner-Mikroben zusammen, um zu verhindern, dass Methan – ein starkes Treibhausgas – ins darüber liegende Wasser gelangt. Diese Studie zeigt, dass diese Tiefseepartnerschaften noch vielseitiger sind, als Wissenschaftler bislang annahmen. Wenn ihr übliches Treibstoff, Methan, knapp wird, können sie auf ein anderes Gas zurückgreifen: Kohlenmonoxid, um zu überleben und den Kohlenstoffkreislauf unter wechselnden Bedingungen am Meeresboden aufrechtzuerhalten.
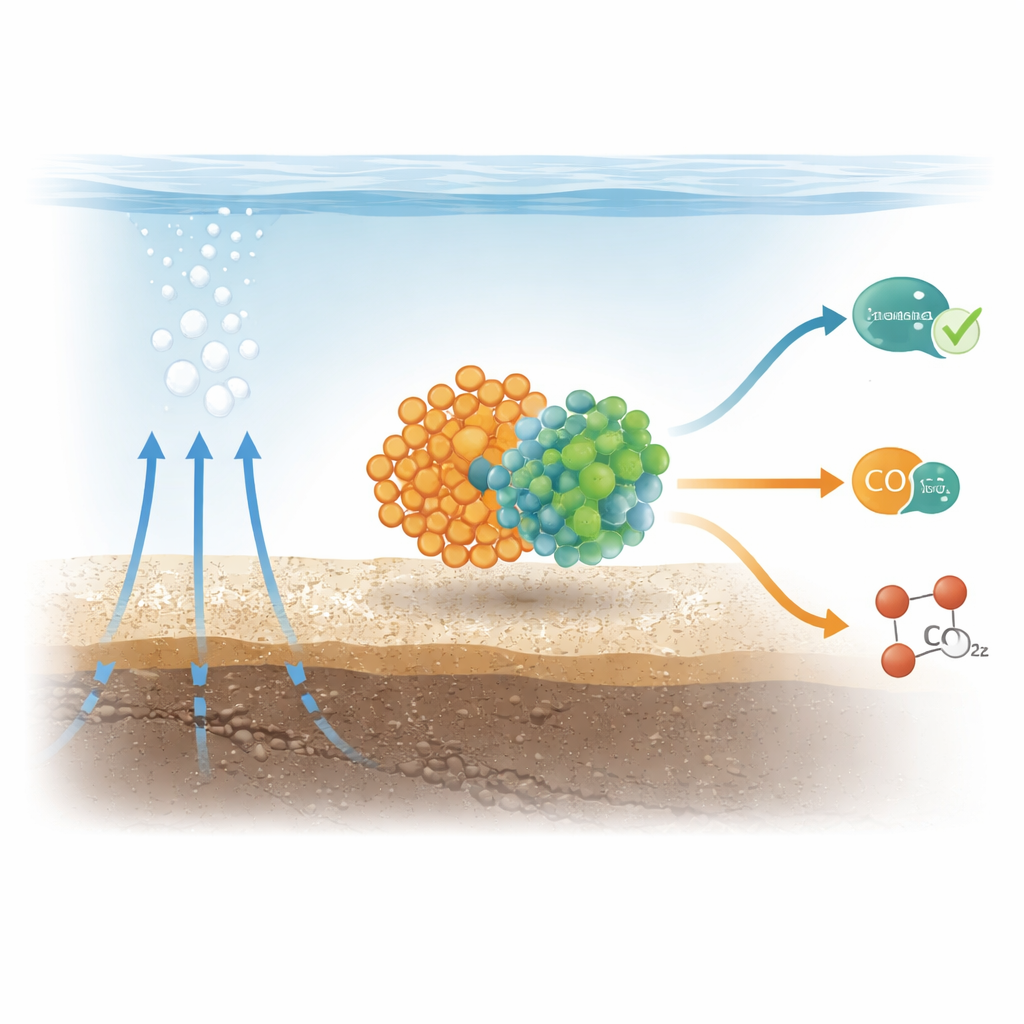
Versteckte Partnerschaften unter dem Meeresboden
An vielen methanreichen Austrittsstellen auf dem Meeresboden bilden zwei Mikrobenarten enge Verbünde: methanverzehrende Archaeen (als ANME-2b bezeichnet) und sulfatreduzierende Bakterien. Gemeinsam erfüllen sie normalerweise eine langsame, aber entscheidende Aufgabe: Die Archaeen verbrauchen Methan, übergeben die freigesetzte Energie und Elektronen an ihre bakteriellen Partner, und die Bakterien nutzen diese Elektronen, um Sulfat aus dem Meerwasser zu reduzieren. Durch diese Zusammenarbeit wird viel Methan gebunden, bevor es in Ozean und Atmosphäre entweichen kann. Die neue Arbeit fragte, ob dieselben Partner auch einen anderen Treibstoff nutzen können – Kohlenmonoxid, ein Gas, das in Sedimenten durch Hitze oder durch andere Mikroben erzeugt werden kann.
Ein neuer Treibstoff für alte Partner
Die Forschenden richteten versiegelte, sauerstofffreie „Mikrokosmen“ mit Schlamm von einem Methanaustritt vor Costa Rica ein und versorgten diese unter kontrollierten Bedingungen mit Kohlenmonoxid. Mithilfe isotopischer Markierungen in Kohlenstoff und Schwefel zeigten sie, dass die Konsortien Kohlenmonoxid oxidierten und gleichzeitig Sulfat zu Sulfid reduzierten. Wenn kein Sulfat vorhanden war, trieb die Oxidation von Kohlenmonoxid stattdessen die Produktion von Methan aus Kohlendioxid an. Die Rate der Methanproduktion aus Kohlenmonoxid war moderat – etwa ein Neuntel so schnell wie ihr üblicher methanverzehrender Stoffwechsel – aber klar messbar. Das zeigt, dass dieselben Gemeinschaften je nach verfügbaren Stoffen sowohl Methan verbrauchen als auch erzeugen können.
Einblick in einzelne Zellen
Um herauszufinden, welche Mikroben auf diesen neuen Treibstoff tatsächlich aktiv waren, nutzte das Team eine leistungsstarke Kombination aus Fluoreszenzbildgebung und nanoskaliger Massenspektrometrie. Sie fütterten die Gemeinschaften mit Stickstoff, der mit einem schweren Isotop markiert war, und maßen dann, wie viel dieses Labels in einzelnen Zellen eingelagert wurde. Selbst in Flaschen, in denen nur Kohlenmonoxid als Energiequelle bereitgestellt wurde, nahmen viele ANME-2b-Zellen und einige ihrer bakteriellen Partner den markierten Stickstoff auf – ein Hinweis darauf, dass sie grundlegende zelluläre Wartungsprozesse durchführten. Bei höheren Kohlenmonoxid-Konzentrationen nahm die Aktivität jedoch ab, was darauf hindeutet, dass zu viel dieses Gases toxisch sein kann und dass die Konsortien in der Natur vermutlich sanfteren, günstigeren Bedingungen ausgesetzt sind.
Das mikrobielle „Aktivitätsprotokoll“ lesen
Über Einzelzellmessungen hinaus untersuchten die Wissenschaftler, welche Gene eingeschaltet wurden, wenn die Gemeinschaften Methan beziehungsweise Kohlenmonoxid nutzten. Bei den Archaeen blieben Gene für das zentrale methanverarbeitende Enzym unter beiden Treibstoffen hochaktiv, während Gene, die mit ihren hauptsächlichen energieerhaltenden Schritten verbunden sind, bei Zufuhr von Kohlenmonoxid heruntergeregelt wurden. Dieses Muster deutet darauf hin, dass die Nutzung von Kohlenmonoxid genügend Energie liefert, um die Zellen am Laufen zu halten, aber nicht genug für starkes Wachstum. Die bakteriellen Partner schalteten dagegen Gene ein, die mit direkter Elektronenübertragung zwischen Zellen und mit eigenen Kohlenmonoxid-verarbeitenden Enzymen assoziiert sind, was darauf hindeutet, dass sie Energie sowohl von den Archaeen beziehen als auch Kohlenmonoxid selbst veratmen können.
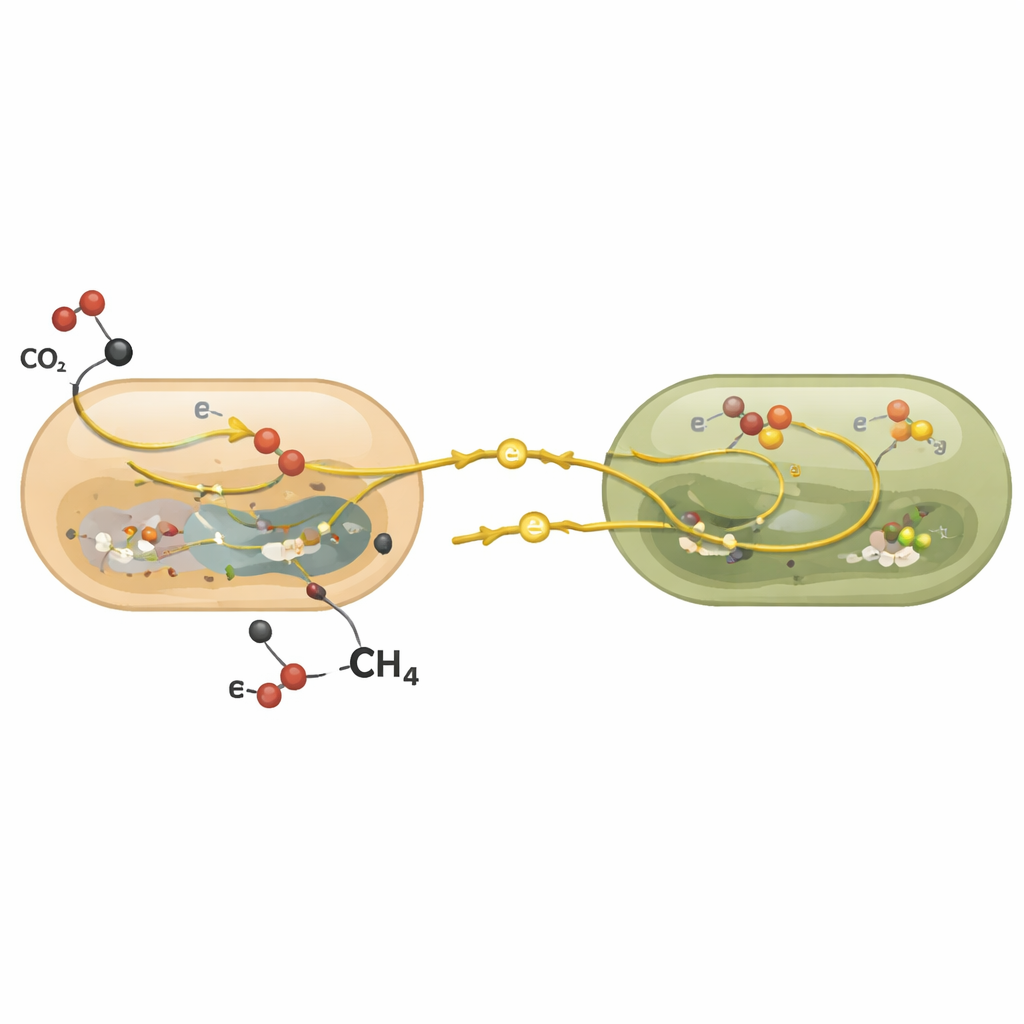
Warum das für den Kohlenstoffhaushalt der Erde wichtig ist
Für Nichtfachleute lautet die Kernbotschaft: Tiefsee-Methan-verbrennende Gemeinschaften sind keine Ein-Trick-Spezialisten. Sie können auf Kohlenmonoxid als alternativen Treibstoff umschalten und nutzen es hauptsächlich, um in mageren Zeiten zu überleben und ihren Stoffwechsel aufrechtzuerhalten, statt sich schnell zu vermehren. Diese Flexibilität hilft den Konsortien, bei schwankender Methanzufuhr zu bestehen und ermöglicht ihnen, ihre Hauptaufgabe – die Zerstörung von Methan – rasch wieder aufzunehmen, sobald Methan wieder verfügbar ist. Indem die Studie diese verborgene Überlebensstrategie aufdeckt, verfeinert sie unser Verständnis davon, wie Kohlenstoff und Schwefel im Meeresboden zirkulieren und wie widerstandsfähig der natürliche Methanfilter der Erde unter sich ändernden Umweltbedingungen sein könnte.
Zitation: Guo, Y., Utter, D.R., Murali, R. et al. Carbon monoxide oxidation expands the known metabolic capacity in anaerobic methanotrophic consortia. Nat Commun 17, 3461 (2026). https://doi.org/10.1038/s41467-026-71433-9
Schlüsselwörter: Methanquellen, Kohlenmonoxid, anaerobe Archaeen, sulfatreduzierende Bakterien, Tiefseesedimente