Clear Sky Science · de
Aptamere mit magnetisch einstellbarer Affinität für zweiwertige Kobalt-Ionen
Magnete zur Steuerung winziger Helfer
Stellen Sie sich vor, molekulare Erkennung ließe sich mit einem Drehknopf an- und ausschalten, so wie Sie ein Licht einschalten. Diese Studie zeigt, wie sehr starke Magnete beeinflussen können, wie kurze DNA-Stücke Metallionen erfassen, und deutet auf künftige Werkzeuge hin, die Medikamente freisetzen, medizinische Aufnahmen verbessern oder Chemikalien nur bei Anwesenheit eines Magnetfelds nachweisen könnten.
Warum Magnete in der Biologie relevant sind
Wissenschaftler fragen sich seit Langem, ob Magnetfelder biologische Aktivität zuverlässig steuern können. Manche ambitionierten Ideen, etwa Zellen im Gehirn mit „Magnetogenetik“-Proteinen zu lenken, stießen auf Skepsis, weil die Kräfte in Erdmagnetfeldstärke meist zu schwach sind, um thermisches Rauschen zu überwinden. Statt sich auf ganze Zellen oder Proteine in schwachen Feldern zu konzentrieren, richteten die Autoren den Blick auf ein einfacheres und besser kontrollierbares System: wie sich bestimmte Metallionen, die von Natur aus magnetempfindlich sind, mit DNA verhalten. Dieser Perspektivwechsel erlaubte eine klare Frage: Kann man gezielt DNA-Stränge auswählen, deren Griff an Metallionen nur in einem starken Magnetfeld stärker wird?
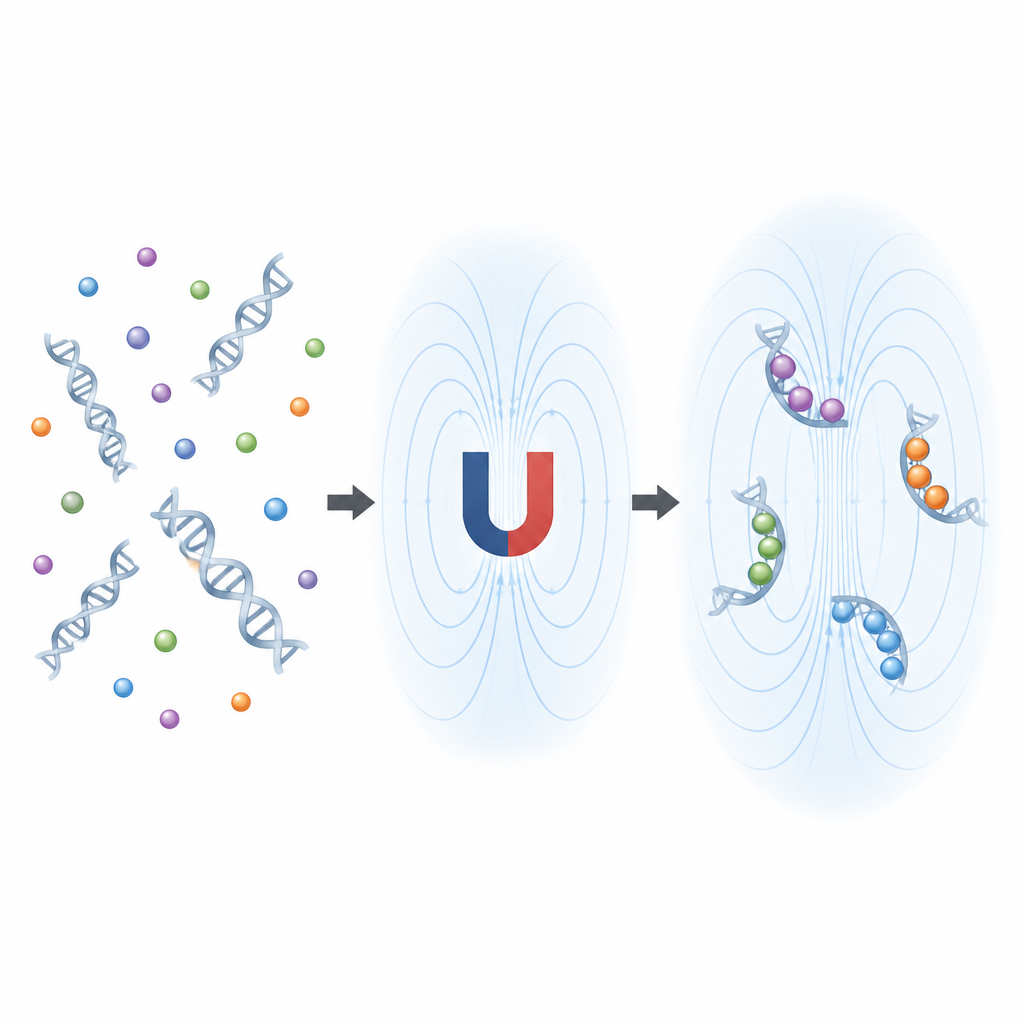
Designer-DNA, die Kobalt im Magneten fester packt
Das Team arbeitete mit Aptameren, kurzen DNA-Strängen, die sich so falten, dass sie spezifische Ziele erfassen können. Sie erzeugten einen großen Pool zufälliger DNA-Sequenzen und setzten ihn zweiwertigen Kobalt-Ionen in einem intensiven 9-Tesla-Magnetfeld aus — viel stärker als in Krankenhaus-Scannern. Mithilfe einer Methode namens HM SELEX behielten sie wiederholt die DNA, die im Magneten Kobalt band, und sortierten Sequenzen aus, die entweder an andere Metalle hafteten oder bereits im normalen Erdmagnetfeld Kobalt binden. Nach sieben Selektionsrunden entwickelte sich der Pool zu einer deutlich kleineren Menge von Aptameren, die für feldabhängige Bindung angereichert waren.
Zwei Arten magnetischer Reaktion
Tests an den zehn häufigsten Aptameren zeigten zwei unterschiedliche Verhaltensweisen. Eine Gruppe, vertreten etwa durch die Sequenz Co M3, band Kobalt bereits bei normaler Feldstärke, wurde aber 2–3-fach fester, wenn das Feld schrittweise von Umgebungsstärke auf 3, 6 und 9 Tesla erhöht wurde. Eine andere Gruppe, beispielhaft Co M8, verhielt sich eher wie ein echter Schalter: Unter normalen Bedingungen band sie kaum Kobalt, zeigte aber oberhalb von rund 6 Tesla plötzlich klare Bindung. Unabhängige Messungen mittels Fluoreszenz, Kalorimetrie, zirkulärer Dichroismus und Gel-Assays bestätigten, dass diese Änderungen real und reversibel waren und dass die Sequenzen eine gewisse Selektivität für Kobalt gegenüber vielen anderen Metallionen besaßen.
Wie Formänderung und Ladung den Effekt antreiben
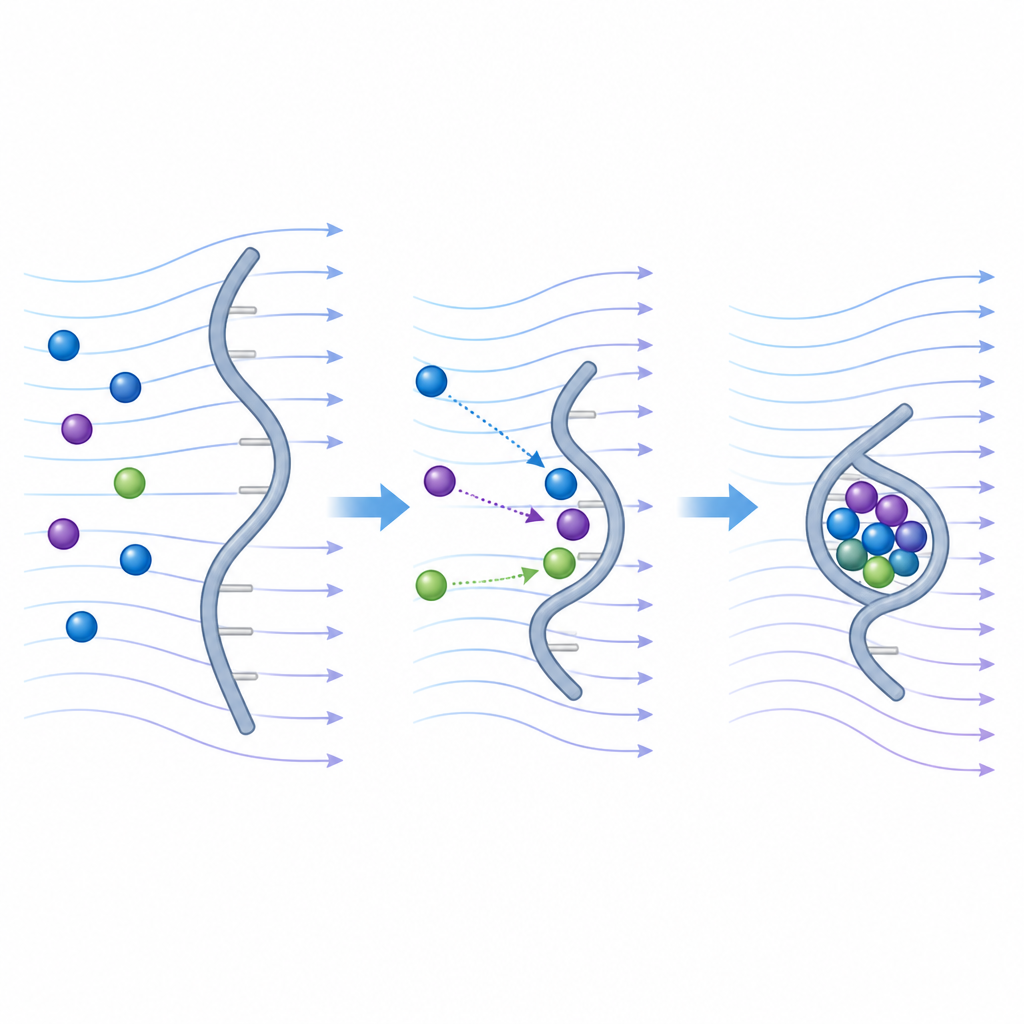
Um zu verstehen, was das Magnetfeld tatsächlich bewirkte, kombinierten die Forscher Computersimulationen mit chemischer Sondeprobe. Die Berechnungen modellierten, wie Kobalt-Ionen und das negativ geladene DNA-Rückgrat in Gegenwart eines Feldes, das auf die drei ungepaarten Elektronen von Kobalt wirkt, aufeinander ziehen. Sie fanden, dass ein stärkeres Feld die elektrostatischen Wechselwirkungen zwischen Ionen und Aptamer verstärkte und dazu anregte, dass mehr Ionen und mehr Basen in die Bindungstasche eintraten. Bei Co M8 etwa rekonfigurierten sich bestimmte Regionen des Strangs so, dass sich nur in starken Feldern ein Multi-Ion-Cluster öffnete. Chemische Footprinting-Experimente und Punktmutationen an Schlüsselbasen zerstörten diesen Cluster und löschten das Schaltverhalten aus, sodass der magnetische Effekt direkt an ein bestimmtes Faltungsbild und Koordinationsgeometrie gebunden wurde.
Vom Proof-of-Concept zu künftigen Werkzeugen
Die Studie kommt zu dem Schluss, dass diese Aptamere als magnetisch einstellbare molekulare Schalter fungieren: Ihr Griff an Kobalt lässt sich durch Anlegen eines starken Magnetfelds verstärken oder in manchen Fällen vollständig einschalten. Die vom Feld beigetragene Energie ist klein, reicht aber aus, um das Gleichgewicht für Mehrionen-Bindestellen zu kippen, die ohnehin in der Nähe eines Schwellenwerts liegen. Obwohl der heute beobachtete Effekt nur bei sehr hohen Feldern und nur für paramagnetische Ionen wie Kobalt auftritt, liefert die Arbeit ein klares Konzept für die Gestaltung von DNA-basierten Bauteilen, die direkt auf Magnete reagieren. Mit weiterer Verfeinerung und niedrigeren Schaltschwellen könnten ähnliche Systeme smarte MRI-Kontrastmittel, magnetisch ausgelöste Medikamententräger oder Sensoren ermöglichen, die ihre Ziele nur bei angelegtem Feld erkennen.
Zitation: Gao, S., Wang, L., Yao, L. et al. Aptamers with magnetically tunable affinity for divalent cobalt ions. Nat Commun 17, 4150 (2026). https://doi.org/10.1038/s41467-026-70871-9
Schlüsselwörter: Aptamere, Kobalt-Ionen, Magnetfeld, DNA-Schalter, Bioreognition