Clear Sky Science · de
Verbreitung mikrobieller Carrageen‑Abbauwege zeigt ein weitverbreitetes latentes Merkmal im Wiederkäuermikrobiom
Algen auf dem Speiseplan für Kühe
Bäuerinnen und Bauern suchen nach Futtermitteln, die sowohl nachhaltig als auch klimafreundlich sind. Algen sind attraktiv, weil sie ohne Süßwasser oder Dünger wachsen und manche sogar die von Kühen ausgestoßenen Methanemissionen verringern können. Über das Verhalten der Algenzucker im Rinderdarm wissen wir jedoch überraschend wenig. Diese Studie untersucht, wie Rinder und ihre Darmmikroben mit Carrageen umgehen — einem häufigen Gelier‑Zucker aus Rotalgen — und was das über verborgene Fähigkeiten im Verdauungssystem vieler Huftiere aussagt.
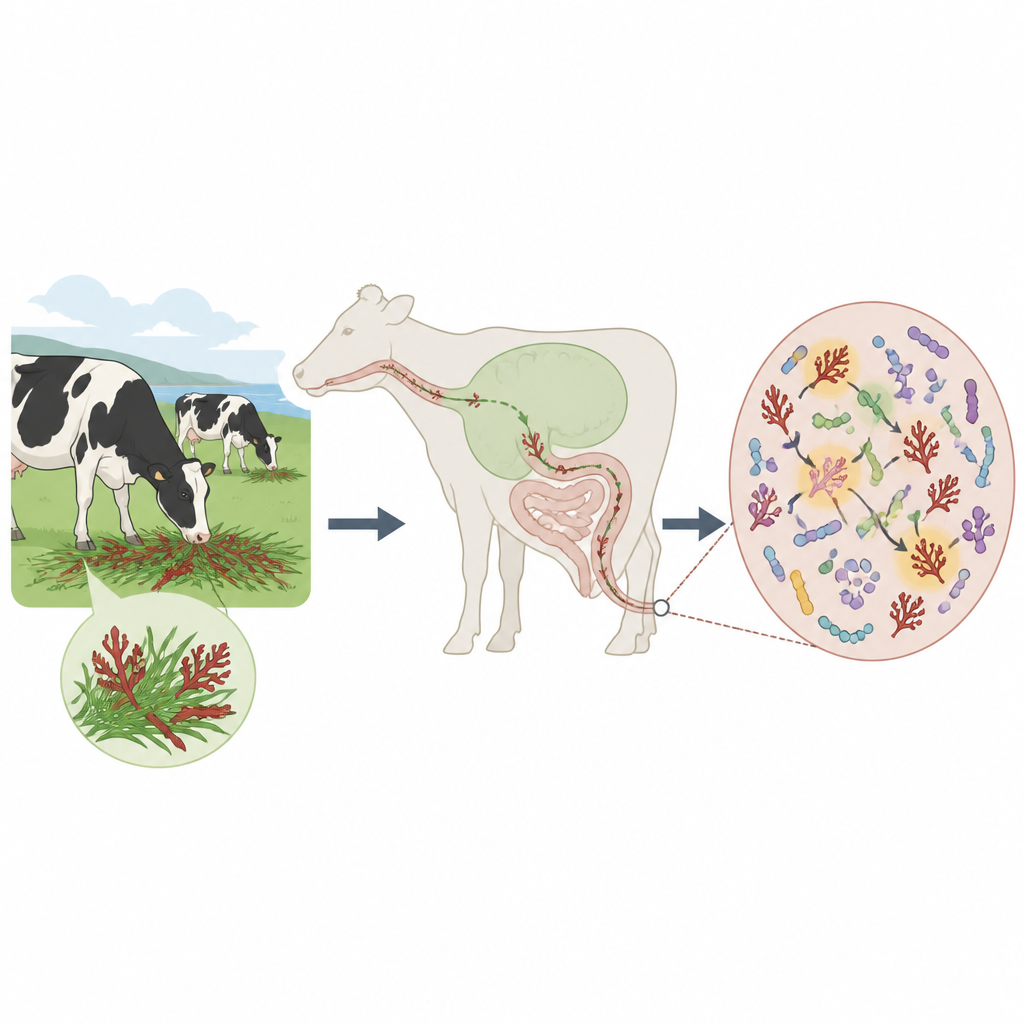
Wie Kühe und Mikroben sich die Arbeit teilen
Kühe, wie andere Wiederkäuer auch, sind auf große Gemeinschaften von Mikroben angewiesen, um zähe Pflanzenfasern zu verdauen, die ihr eigener Organismus nicht aufschließen kann. Diese Mikroben leben entlang des gesamten Darms, nicht nur im bekannten ersten Magen, dem Pansen. Das Team fütterte Rinder mit der Rotalge Mazzaella japonica, die reich an Carrageen ist, und verglich die Mikroben in ihren Mägen und im Kot mit denen von Kühen auf einer normalen Diät. Im Pansen zeigten sich nur geringe Veränderungen, während im unteren Darm, wo das Verdautematerial den Körper verlässt, dramatische Verschiebungen der mikrobiellen Gemeinschaft auftraten. Insbesondere wurden Bakterien der Gruppe Bacteroides bei Zugabe von Algenfutter deutlich häufiger.
Algen als Nahrung für spezialisierte Bakterien
Um zu prüfen, ob diese Mikroben tatsächlich von Algenzuckern leben können, züchteten die Forschenden Bakterien aus Rinderproben im Labor auf gereinigtem Carrageen und auf Extrakten der Rotalge. Mehrere Bacteroides‑Stämme gediehen allein mit Carrageen als Kohlenstoffquelle, was zeigt, dass sie es ohne zusätzliche Nährstoffe als Nahrung nutzen können. Als das Team die Algenzucker mit einem fluoreszierenden Marker kennzeichnete, beobachteten sie, dass diese Stämme das leuchtende Material in ihre Zellen aufnahmen. Das deutet auf einen ‚egoistischen‘ Fütterungsstil hin, bei dem Bakterien Algenfragmente direkt aufnehmen und verdauen, anstatt die Zucker frei mit Nachbarorganismen zu teilen.

Verborgene genetische Werkzeuge für die Algenverdauung
Bei der Analyse der DNA und Proteine dieser Mikroben entdeckten die Wissenschaftler Gencluster, die vollständige Werkzeugsätze zum Abbau von Carrageen bilden. Diese Cluster, sogenannte Polysaccharid‑Utilisierungs‑Loci, kodieren Enzyme, die lange Zuckerketten zerschneiden und Sulfatgruppen entfernen, die sonst die Verdauung blockieren würden. Die Studie untersuchte eingehend eine Familie zentraler Enzyme, die das Carrageenrückgrat angreifen, und zeigte, dass kleine strukturelle Unterschiede in ihren aktiven Zentren jede Enzymvariante auf unterschiedliche Carrageenarten einstellen. Manche wirken am besten auf stark sulfatierten Formen, andere sind auf teilweise bearbeitete ‚Hybrid‘‑Versionen spezialisiert; zusammen ermöglichen sie es den Bakterien, die komplexe Zellwand der Alge zu demontieren.
Ein weitverbreitetes, aber stilles Talent bei Huftieren
Die Autorinnen und Autoren durchsuchten anschließend große genetische Datenbanken von Rindern, Wasserbüffeln, Hirschen, Schafen, Ziegen und sogar Wildtieren wie Moschustieren und Giraffen. Sie fanden viele nahe Verwandte der in Rindern zuerst identifizierten Carrageen‑Gencluster, oft mit sehr ähnlichen Enzymsets und Genanordnungen. Diese Treffer tauchten bei Tieren auf verschiedenen Kontinenten und in unterschiedlichen Lebensräumen auf, selbst in Regionen, in denen die in den Versuchen verwendete Rotalge nicht natürlich vorkommt. Das spricht dafür, dass Carrageen‑abbaubare Wege in den Darmmikroben vieler Huftiere verbreitet, aber meist inaktiv sind und erst durch Algenzufuhr aktiviert werden.
Eine alte Verbindung zwischen Land und Meer zeichnen
Im Vergleich dieser landgebundenen Gencluster mit Sequenzen aus Meeresbakterien und von algenfressenden Fischen deutet die Studie auf eine alte und komplexe Evolutionsgeschichte hin. Einige der Carrageen‑Gene in Rindermikroben ähneln denen in Darmbakterien von Fischen, die auf Algenkost spezialisiert sind, und beide zeigen Anzeichen dafür, dass sie durch horizontalen Gentransfer erworben wurden und nicht nur durch langsame Mutation. Zusammengenommen deuten die Befunde auf eine lange Geschichte des Genaustauschs zwischen marinen und terrestrischen Mikroben hin, wahrscheinlich getrieben von Tieren, die Algen fraßen oder Beutetiere konsumierten, die Algen fressen.
Warum das für die Landwirtschaft wichtig ist
Für nichtfachkundige Leserinnen und Leser ist die wichtigste Erkenntnis, dass Kühe und ihre Verwandten bereits mikrobielle Partner in sich tragen, die Algenzucker verarbeiten können, selbst wenn die Tiere zuvor nie Algen gefressen haben. Diese ‚latenten‘ Merkmale bedeuten, dass sich Wiederkäuermägen schnell an neue Futtermittel anpassen können, ohne auf langwierige evolutionäre Veränderungen warten zu müssen. Zwar reduzierte die hier getestete Rotalge nicht maßgeblich die Methanemissionen, doch das Verständnis, wie ihre Zucker verarbeitet werden, eröffnet Möglichkeiten, klüger konzipierte Algenfuttermittel zu entwickeln. Solche Futtermittel könnten Nährstoffe gezielter in den unteren Darm liefern, als präbiotische Ansätze nützliche Bakterien fördern und das verborgene genetische Potenzial des Wiederkäuermikrobioms für eine nachhaltigere Tierhaltung nutzbar machen.
Zitation: Tingley, J.P., Andersen, T.O., Mihalynuk, L.G. et al. Distribution of microbial carrageenan foraging pathways reveals a widespread latent trait within the ruminant intestinal microbiome. Nat Commun 17, 4237 (2026). https://doi.org/10.1038/s41467-026-70776-7
Schlüsselwörter: Algenfutter, Wiederkäuermikrobiom, Carrageenverdauung, Bacteroides‑Bakterien, latente Merkmale