Clear Sky Science · de
Recycling von Lipiden alternder Zellen für gezielte Senotherapie
Aus Zellabfall wird Gelenkgold
Mit zunehmendem Alter steifen viele unserer Gelenke ein und schmerzen, oft mit dem Ergebnis einer Osteoarthritis — einer der Hauptursachen für Behinderung weltweit. Ein entscheidender Übeltäter sind beschädigte, «gealterte» Zellen, die sich im Knorpel ansammeln. Statt diese Zellen einfach zu töten, stellt diese Studie eine einfallsreichere Frage: Was, wenn man ihr schädliches Fett abschöpfen und als natürlichen Schmierstoff wiederverwenden könnte, um unsere Gelenke zu schützen?
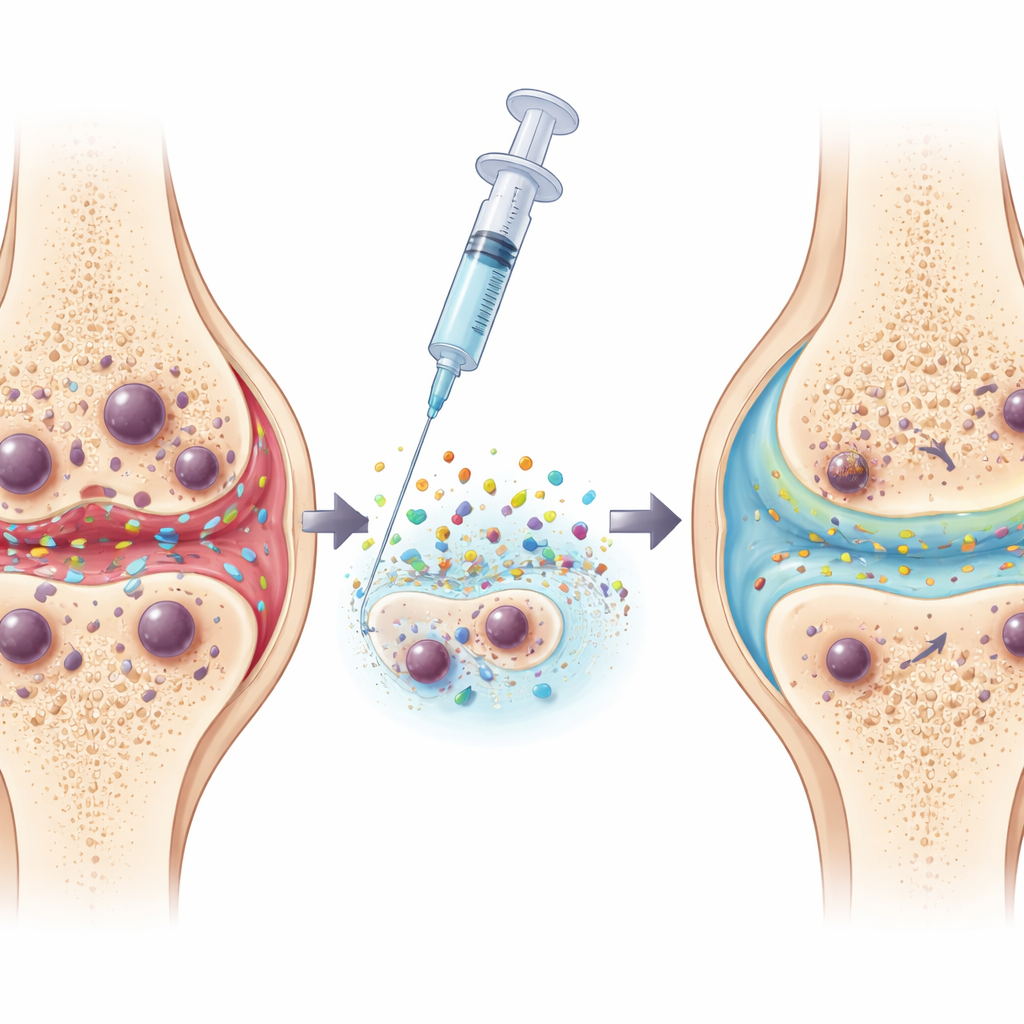
Warum alte Zellen in schmerzenden Gelenken zum Problem werden
Zellen, die in einen langfristig geschädigten Zustand eintreten, genannt Seneszenz, hören auf sich zu teilen, bleiben aber metabolisch aktiv. Im Knorpel sammeln sich diese seneszenten Zellen mit dem Alter und nach Verletzungen an und tragen zur Osteoarthritis bei. Sie setzen einen Cocktail aus entzündungsfördernden und Gewebe zersetzenden Molekülen frei, der benachbarte gesunde Zellen in denselben Zustand treiben kann und so ein sich ausbreitendes «schlechtes Viertel» im Gelenk schafft. Die Autoren fanden zudem eine weniger beachtete Eigenschaft dieser seneszenten Knorpelzellen: Sie sind mit Fetten überladen, insbesondere Cholesterin und bestimmten Membranlipiden, und verwandeln sich so in winzige Depots metabolischer Abfälle.
Vom Töten zum Schlankmachen: Eine neue Behandlungsphilosophie
Die meisten experimentellen Wirkstoffe gegen alternde Zellen, sogenannte Senolytika, versuchen, diese Zellen vollständig zu eliminieren. Zwar kann das einige schädliche Signale reduzieren, birgt aber auch das Risiko, Zellen zu entfernen, die noch nützliche Aufgaben bei der Gewebereparatur erfüllen, und beim Absterben entzündliche Trümmer freizusetzen. Das Team schlägt eine andere Strategie vor: Statt seneszente Zellen zu exekutieren, «schlankt» man sie ab. Durch das Anvisieren der charakteristischen Lipide, die sich in diesen Zellen ansammeln, wollen sie deren schädliche Sekrete verringern, während die Zellen am Leben bleiben. Die Autoren nennen dieses Konzept „Senorecycle“, weil es den metabolischen Abfall alter Zellen in eine Ressource zum Schutz des Gelenks verwandelt.
Ein intelligentes Hydrogel, das Nanoliposuktion durchführt
Um diese Idee in die Praxis umzusetzen, entwickelten die Forschenden ein injizierbares Material namens MINH, das im Gelenk verbleibt. Es kombiniert ein weiches Hydrogel, das am Knorpel haftet, mit medikamentenbeladenen Nanopartikeln. Diese Partikel sind mit einem Molekül versehen, das einen Oberflächenmarker, ICAM1, erkennt — den das Team als auffällig exprimiert auf seneszenten Knorpelzellen, nicht aber auf gesunden Zellen, identifizierte. Nach dem Andocken dringen die Partikel in die seneszenten Zellen ein und setzen dort langsam eine Verbindung frei, die gezielt Cholesterin und bestimmte Phospholipide herauszieht — genau jene Lipide, die sich auf problematische Mengen angesammelt hatten. Tatsächlich führt das System eine zielgerichtete «Nanoliposuktion» durch und entzieht alten Zellen überschüssiges Fett, ohne sie zu zerstören.
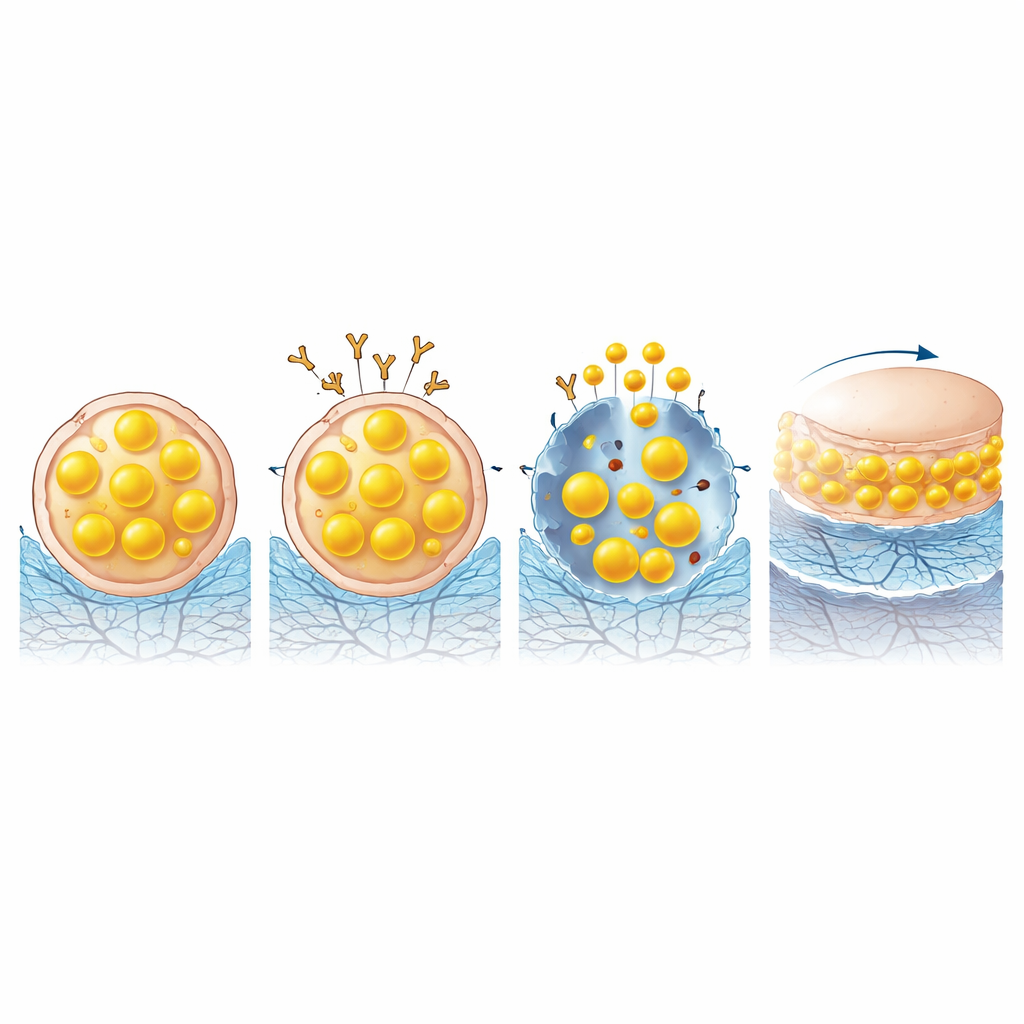
Wiederverwendung der gewonnenen Lipide als natürlicher Schmierstoff
Die Innovation endet nicht mit der Entfernung. Die aus den seneszenten Zellen extrahierten Lipide verschwinden nicht einfach; sie gelangen über die normalen Sekretionswege in die Gelenkhöhle und in das umgebende Hydrogel. Dort ordnen sich diese Moleküle unter der ständigen Reibung durch Gelenkbewegungen an der Oberfläche des Gels neu und bilden eine glatte, hydratisierte Schicht, die das natürliche Schmiersystem gesunden Knorpels imitiert. Laboruntersuchungen zur Reibung zeigten, dass mit recycelten Lipiden angereicherte Gele den Gleitwiderstand auf etwa die Hälfte im Vergleich zu herkömmlichen Hyaluronsäuregelen reduzieren konnten und so Knorpeloberflächen vor weiterem Verschleiß schützen.
Gesündere Gelenke in Tiermodellen
In Mausmodellen einer verletzungsinduzierten Osteoarthritis zeigten Gelenke, die mit dem MINH-System behandelt wurden, weniger Schmerzverhalten, weniger knöcherne Auswüchse und eine bessere Erhaltung des glatten, stoßdämpfenden Knorpels im Vergleich zu unbehandelten oder konventionell behandelten Tieren. Die «erschlankten» seneszenten Zellen setzten deutlich weniger entzündliche und gewebeabbauende Proteine frei und verringerten so ihre Fähigkeit, benachbarte gesunde Zellen in neue seneszente Problemzellen zu verwandeln. Gleichzeitig verbesserten die recycelten Lipide die Gelenkschmierung über Wochen nach einer einzigen Injektion. Wichtig ist, dass die Behandlung in großen Organen und Bluttests keine nachweisbare Toxizität zeigte.
Was das für die künftige Gelenkversorgung bedeuten könnte
Anstatt gealterte, beschädigte Zellen nur als Ziele zur Zerstörung zu betrachten, legt diese Arbeit nahe, dass sie umgestaltet werden können, um zu Verbündeten zu werden. Durch das Entziehen und Recyceln ihrer überschüssigen Lipide dämpft die MINH-«Senorecycle»-Plattform sowohl schädliche Signale als auch stärkt das eigene Schmiersystem des Gelenks. Für Patientinnen und Patienten könnte dies eines Tages in Behandlungen münden, die Schmerzen lindern und Gelenkschäden langsamer voranschreiten lassen — mit weniger Nebenwirkungen als zellvernichtende Medikamente. Darüber hinaus deutet der Ansatz auf eine neue Generation von Therapien hin, die alternde Gewebe nicht durch Abriss behandeln, sondern durch gezielte Umleitung und Wiederverwendung ihrer fehlgesteuerten Ressourcen.
Zitation: Ji, X., He, X., Cai, H. et al. Recycling senescent cell lipids for targeted senotherapy. Nat Commun 17, 3877 (2026). https://doi.org/10.1038/s41467-026-70486-0
Schlüsselwörter: Osteoarthritis, zelluläre Seneszenz, Nanopartikel, Gelenkschmierung, Lipidstoffwechsel