Clear Sky Science · de
Ein Bauplan für lokale und entfernte Invasionsprogramme bei Glioblastom
Warum diese Hirnkrebsstudie wichtig ist
Das Glioblastom gehört zu den tödlichsten Hirntumoren, weil seine Zellen nicht an Ort und Stelle bleiben. Selbst nachdem Chirurgen alle sichtbaren Tumoranteile entfernt haben, führen verstreute Krebszellen, die im Gehirn verborgen sind, fast immer zum Wiederauftreten des Tumors. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wie breiten sich Glioblastomzellen genau im Gehirn aus, und gibt es unterschiedliche „Stile“ der Invasion, die auf verschiedene Weise blockiert werden könnten?
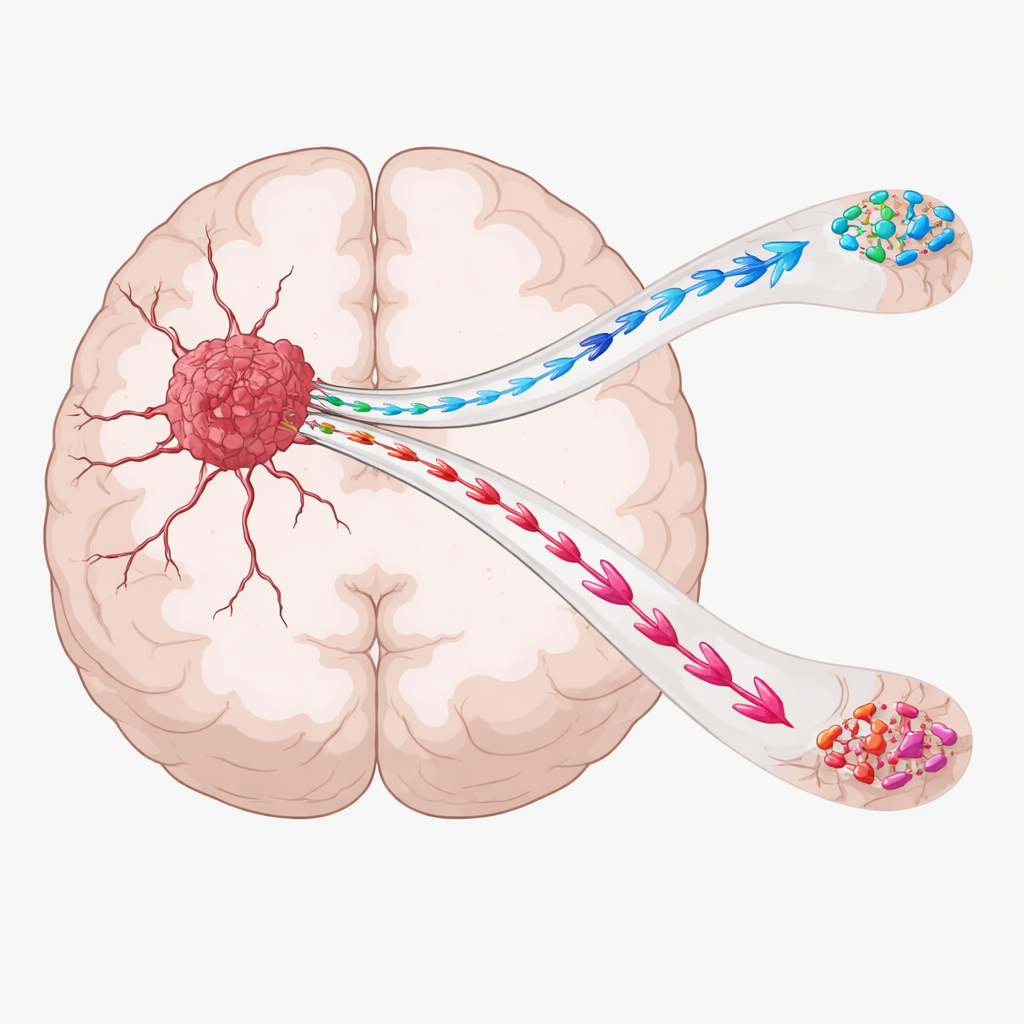
Zwei Hauptwege der Tumorausbreitung
Die Forschenden konzentrierten sich auf zwei grobe Muster der Ausbreitung, die Ärzte bei Patientinnen und Patienten beobachten. In einigen Fällen kriechen Krebszellen nur kurze Strecken rund um den ursprünglichen Tumor und bleiben auf derselben Hemisphäre des Gehirns. In anderen Fällen ziehen Zellen weiter und überqueren die großen Faserbündel, die die beiden Gehirnhälften verbinden, und sorgen auf der gegenüberliegenden Seite für neues Tumorwachstum. Diese beiden Wege, lokal und distal genannt, folgen bestehenden Gehirnstrukturen: Zellen können entlang langer Nervenfasern wandern oder bei der Bewegung Blutgefäße umschlingen.
Ein lebendes Labor in Mäusen aufbauen
Um diese Verhaltensweisen kontrolliert zu untersuchen, transplantierte das Team menschliche Glioblastom-Zelllinien, die im Labor als Sphäroiden gezüchtet wurden, in die Gehirne von Mäusen. Sie injizierten Mischungen aus 20 verschiedenen patientenabgeleiteten Modellen und trennten später die Gehirnhälften, um zu sehen, welche Modelle es auf die andere Seite geschafft hatten. Durch das Sequenzieren der genetischen Aktivität von Tausenden einzelner Tumorzellen und das Zurückverfolgen dieser Zellen zu ihren Ursprungsmodellen konnten die Wissenschaftler jede Neigung eines Tumors zur Ausbreitung mit den enthaltenen Zelltypen und den genutzten Routen verknüpfen.
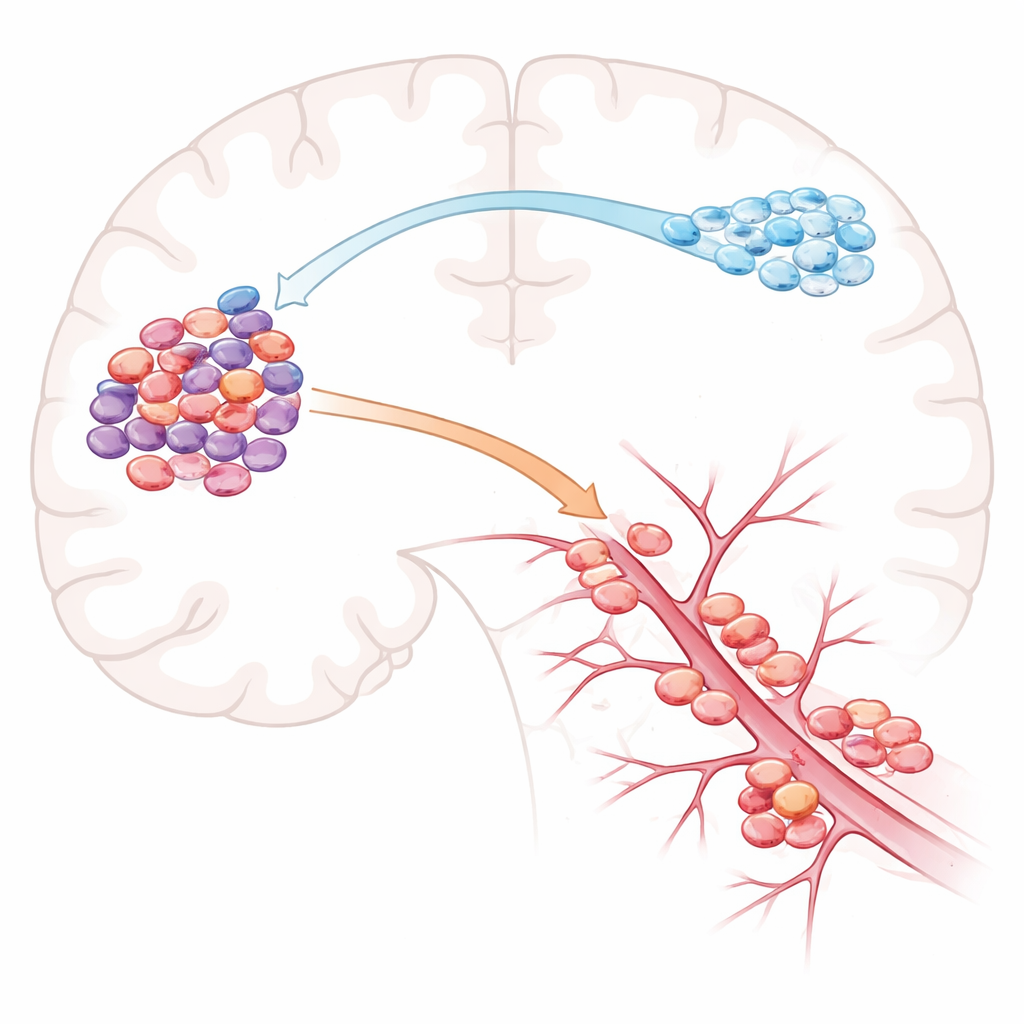
Zwei Invasions-„Persönlichkeiten“ innerhalb von Tumoren
Sie fanden eine klare Aufspaltung in der Tumor‑Persönlichkeit. Modelle, die häufig Zellen in die gegenüberliegende Hemisphäre schickten, enthielten viele Zellen, die unreifen Stütz‑/Vorläuferzellen des Gehirns ähneln, den sogenannten Oligodendrozyten‑Vorläufern. Diese Krebszellen neigten dazu, entlang von Nervenfasertrakten zu wandern – ein Muster, das als peri‑axonale Invasion bezeichnet wird. Im Gegensatz dazu waren Modelle, die auf ihrer Hirnseite blieben, aber lokal trotzdem streuten, von einem stressangepassten, narbenähnlichen Zustand dominiert, der oft als mesenchymal beschrieben wird. Diese Zellen wurden beim Eindringen entlang von Blutgefäßen beobachtet, was auf eine peri‑vaskuläre Route hindeutet. Anders gesagt: Die interne Mischung der Zelltypen in einem Glioblastom bestimmt mit, ob es lieber lange Strecken entlang von Nervenfasern zurücklegt oder in der Nähe entlang von Gefäßen streut.
Was passiert, wenn Zellen aktiv invadieren
Innerhalb jedes Tumors verglichen die Forschenden anschließend Zellen aus dem dichten Kern mit Zellen, die bereits entfernte Regionen erreicht hatten. Die invasiven Zellen schalteten spezifische Gen‑Sätze ein — temporäre „Programme“ der Aktivität — statt einfach nur einer von Anfang an vorhandenen festen Unterart anzugehören. Zellen auf der Fernroute erhöhten die Aktivität von Genen, die mit früher Hirnentwicklung, Bewegung und Zellteilung verknüpft sind; die Autoren nennen diese Konstellation ein distales Invasionsprogramm. Lokal invasivere Zellen entlang von Blutgefäßen aktivierten ein anderes Programm, das mit der Interaktion mit der umgebenden Matrix verbunden ist, dem biologischen Gerüst, das Blutgefäße umgibt. Räumliche Kartierungsmethoden, die Genaktivität direkt in dünnen Gewebeschnitten lesen, bestätigten, dass diese Programme speziell entlang von Nervenbahnen beziehungsweise Blutgefäßen aufleuchten.
Das umgebende Gehirn formt das Tumorverhalten
Die Studie zeigt außerdem, dass invasive Krebszellen nicht allein agieren. Mithilfe multiplexer Bildgebung und räumlicher Transkriptomik kartierte das Team, welche normalen Gehirn‑ und Immunzellen neben invasiven Zellen sitzen. In Bereichen mit Fernausbreitung begleiteten Tumorzellen spezialisierte Immunzellen mit einem entzündlichen und energiehungrigen Profil sowie Nervenzellen in unterschiedlichen Schichten der Großhirnrinde. Lokal invasivierende Zellen um Blutgefäße waren stattdessen mit gefäßauskleidenden Zellen und Proteinen verflochten, die das umgebende Gerüst umgestalten. Diese vielschichtige Sicht macht deutlich, dass Invasionsweg, Tumorprogramm und die lokale Nachbarschaft normaler Zellen eng miteinander verknüpft sind.
Was das für zukünftige Therapien bedeutet
Für Menschen mit Glioblastom ist die zentrale Botschaft, dass Invasion kein einzelner Prozess mit einem einzigen Schalter ist. Tumoren können je nach internen Zellzuständen eher zu lokaler oder zu fernreichender Ausbreitung neigen, und sobald Zellen zu wandern beginnen, übernehmen sie vorübergehend spezialisierte Invasionsprogramme, die auf die Strukturen abgestimmt sind, entlang derer sie reisen. Indem diese Arbeit einen detaillierten „Bauplan“ dieser Zustände und ihrer Nachbarschaften liefert, legt sie nahe, dass künftige Therapien zwei Dinge gleichzeitig angehen müssten: Tumoren aus hochinvasiven Zellzuständen herauszusteuern und die spezifischen Unterstützungssysteme zu stören, die Zellen beim Migrationsvorgang entlang von Nervenfasern oder Blutgefäßen helfen.
Zitation: Chanoch-Myers, R., Hara, T., Greenwald, A.C. et al. A blueprint for local and distal invasion programs in glioblastoma. Nat Commun 17, 4079 (2026). https://doi.org/10.1038/s41467-026-70470-8
Schlüsselwörter: Glioblastom, Invasion von Hirntumoren, Krebszellzustände, räumliche Transkriptomik, Tumor-Mikroumgebung