Clear Sky Science · de
BamA-Selbstinsertion treibt die Umgestaltung der inneren zur äußeren Membran bei didermen Firmicutes voran
Wie schlafende Bakterien kampfbereit erwachen
Bakteriensporen sind die Überlebenskapseln der Natur: winzige, ruhende Lebensformen, die Kochen, Austrocknen und lange Zeiträume überdauern können. Diese Studie stellt eine auf den ersten Blick einfache Frage zu einem solchen sporulierenden Bakterium, Acetonema longum: Wenn eine Spore erwacht, wie verwandelt sich eine ihrer inneren Membranen in eine robuste äußere Hülle, die die aktive Zelle schützt? Durch Verfolgen wichtiger Membranproteine und Experimente in künstlichen Membranen zeigen die Forscher einen selbststartenden Mechanismus, der diesem Bakterium hilft, seine Schutzschicht von innen nach außen wiederaufzubauen.
Rüstungsschichten um eine winzige Zelle
Viele Vertreter der Bakteriengruppe Firmicutes überdauern harte Bedingungen, indem sie Sporen bilden—ruhend eingehüllte Zellen mit mehreren Schutzschichten. Bei bekannten Arten wie Bacillus subtilis besitzt die wachsende Zelle eine einzige Membran, die von einer dicken Wand umgeben ist. Acetonema longum gehört jedoch zu einem selteneren Zweig, den didermen Firmicutes, deren aktive Zellen zwei Membranen tragen, eine innere und eine äußere. Während der Sporulation dieser Organismen entstehen sowohl die „innere Sporenmembran“ als auch die „äußere Sporenmembran“ aus der inneren Membran der Mutterzelle. Wenn die Spore später keimt, muss sie die äußere Sporenmembran auf irgendeine Weise in eine voll funktionsfähige äußere Membran umbauen—eine Membran, die Gifte abblockt, spezialisierte Kanäle enthält und einzigartige Moleküle namens Lipopolysaccharide beherbergt.
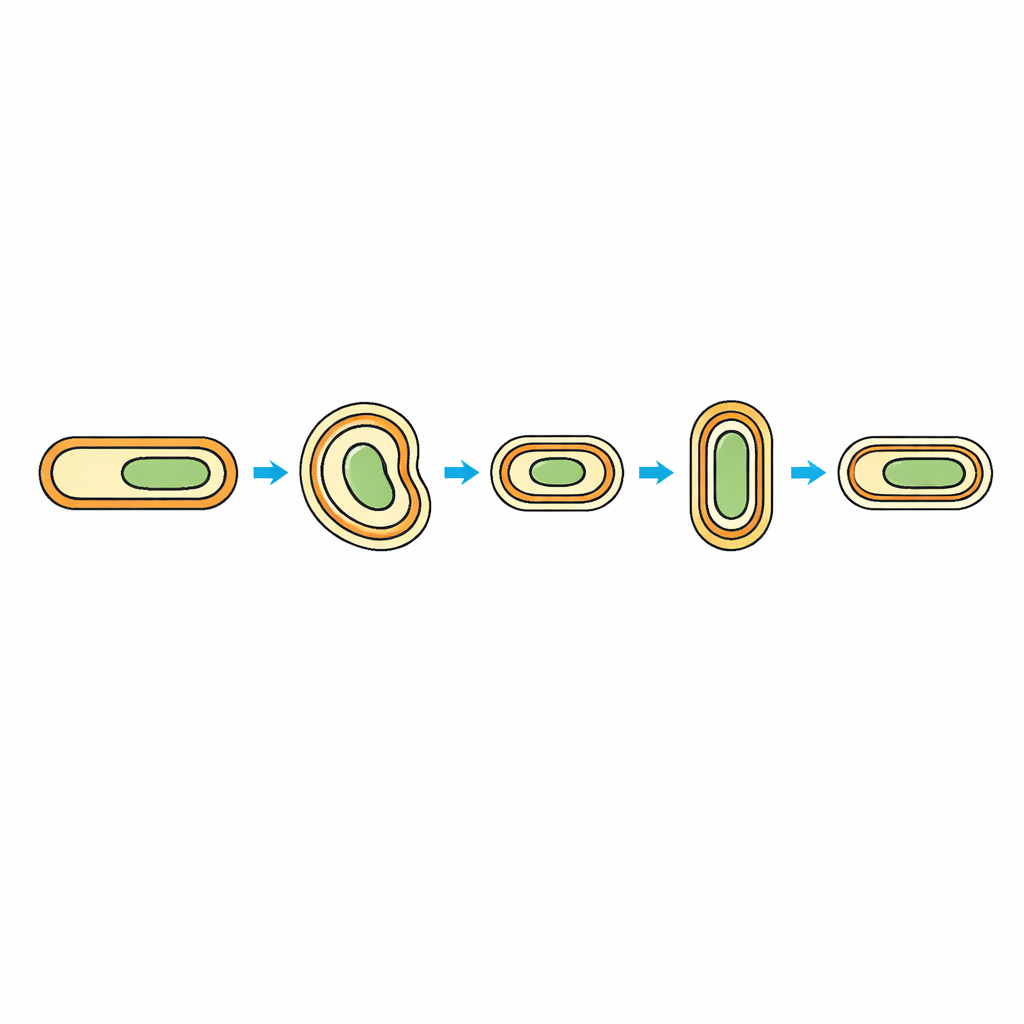
Die fehlenden Teile in der Sporenschale finden
Das Team kombinierte Genomanalysen, Proteom‑Untersuchungen und RNA‑Sequenzierung, um membranbezogene Moleküle über den Lebenszyklus des Bakteriums hinweg zu verfolgen: wachsende Zellen, Zellen in Sporulation, vollständig ruhende Sporen und Sporen im Keimungsbeginn. Sie konzentrierten sich auf äußere Membranproteine, die fassförmige Kanäle bilden, und auf die Maschinerie zum Zusammenbau von Lipopolysacchariden (LPS). In aktiv wachsenden und keimenden Zellen detektierten sie zentrale Komponenten der äußeren Membran, darunter das Kanalbaubioprotein BamA und den LPS‑Transporter LptD. Bemerkenswerterweise fehlten diese Proteine in ausgereiften Sporen. Auch andere Kennzeichen einer typischen äußeren Membran, wie Brückenproteine, die LPS durch die Zellhülle transportieren, waren in diesem ruhenden Zustand nicht vorhanden. Das zeigt, dass die äußerlich wie eine äußere Membran wirkende Schicht der Spore tatsächlich eine innere‑Membran‑ähnliche Doppelschicht ist, die darauf wartet, wieder aufgebaut zu werden.
Ein schlankes, aber leistungsfähiges Membran‑Werkzeugset
Obwohl Acetonema longum in seinem aktiven Zustand eindeutig über eine echte äußere Membran verfügt, ist die dafür notwendige Maschinerie im Vergleich zu Lehrbuchbakterien wie Escherichia coli reduziert. Die Forscher fanden nur eine vereinfachte Version des β‑Barrel‑Assembly‑Machinery (BAM)‑Komplexes: BamA selbst ist vorhanden, die üblichen Helfer‑Lipoproteine fehlen jedoch. Ebenso ist das LPS‑Transportsystem nicht vollständig und nutzt eine modifizierte Pumpe an der inneren Membran. Der übliche Weg, der Lipoproteine zur äußeren Membran führt, fehlt vollständig. Trotz dieses minimalistischen Werkzeugsatzes baut der Organismus weiterhin eine funktionelle äußere Membran auf, was darauf hindeutet, dass er eher auf ältere, eigenständige Mechanismen angewiesen ist statt auf große Multi‑Protein‑Komplexe.
Neue Mitspieler und ein selbststartender Insertionstrick
Im genomischen Umfeld von bamA entdeckten die Autoren zwei zuvor nicht charakterisierte Proteine, die sie SonA und SonB nannten und die in vielen didermen Firmicutes konserviert sind. SonA ähnelt einem kleineren Verwandten von BamA—ein fassförmiges äußeres Membranprotein mit drei flexiblen „POTRA“‑Domänen, die vermutlich beim Umgang mit anderen Proteinen helfen—während SonB als äußeres Membranlipoprotein vorhergesagt wird. Beide werden koexprimiert mit BamA, insbesondere während der Keimung. Um zu testen, ob BamA und SonA sich ohne Hilfe in Membranen einbauen können, faltete das Team gereinigte Versionen dieser Proteine in einfache künstliche Liposomen um. Anhand von Protease‑Verdauungsmustern und veränderten Mobilitäten in Gelen zeigten sie, dass sich beide Proteine spontan falten und sich bei moderaten Temperaturen, die den Keimungsbedingungen des Bakteriums entsprechen, in Lipid‑Doppelschichten einbetten.
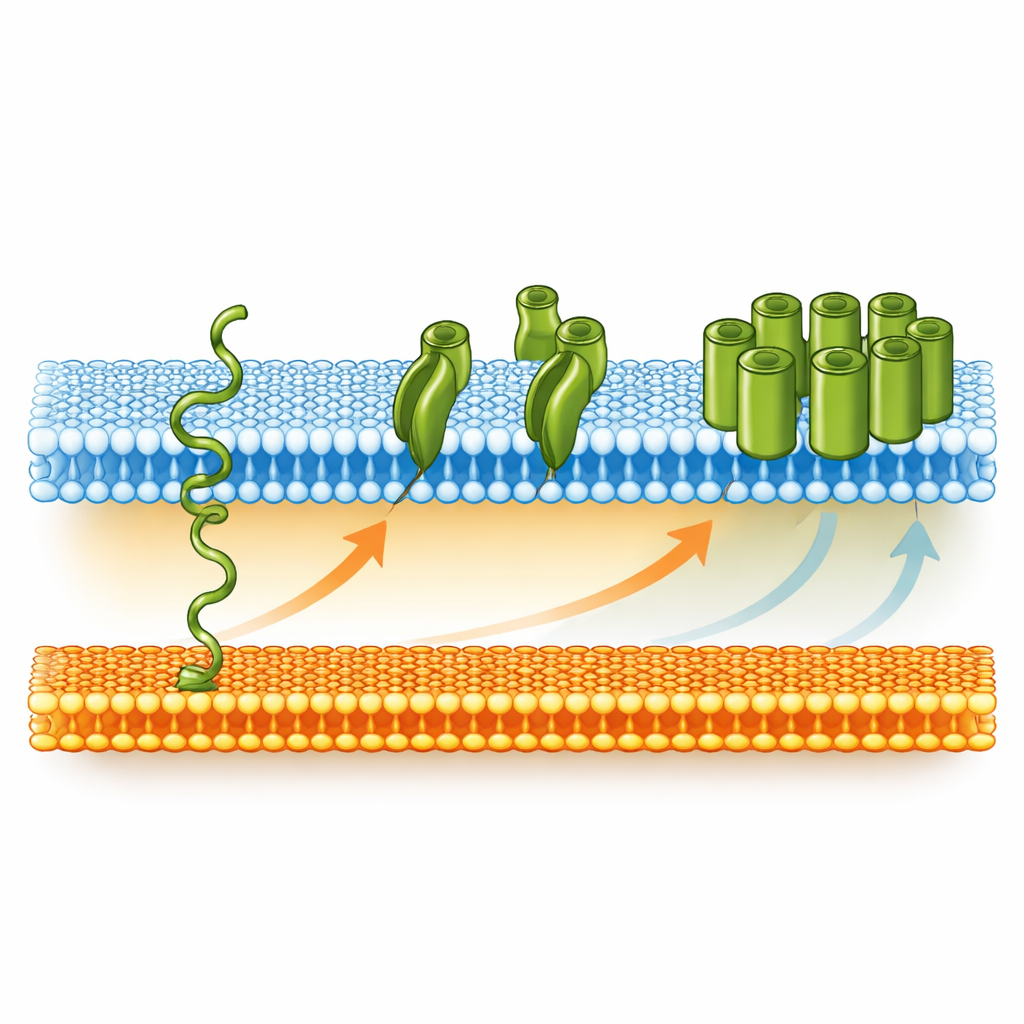
Von der schlafenden Hülle zur funktionalen Rüstung
Aus diesen Bausteinen schlagen die Autoren ein schrittweises Modell vor, wie die innerlich‑ähnliche äußere Sporenmembran während der Keimung in eine echte äußere Membran verwandelt wird. Wenn die Spore rehydriert und der Stoffwechsel wieder startet, beginnt die Zelle, BamA (und vermutlich SonA) zu produzieren, die über die innere Sporenmembran in den Raum zwischen den beiden Membranen transportiert werden. Dort setzen sich diese Proteine allmählich ohne die üblichen Helfer in die äußere Sporenmembran ein. Sobald genügend BamA vorhanden ist, übernimmt es die Rolle einer eigenen Assemblierungsmaschine und setzt weitere äußere Membranproteine wie LptD ein. LptD bringt dann LPS‑Moleküle in das äußere Blatt der Membran, wodurch die Umwandlung in eine voll funktionsfähige äußere Membran abgeschlossen wird. Vereinfacht gesagt nutzt das Bakterium ein selbststartendes Kanalprotein, um den Wiederaufbau seiner Rüstung in Gang zu setzen und eine einfache Lipidschicht beim Erwachen der Spore in eine ausgeklügelte Schutzbarriere zu verwandeln.
Zitation: Beskrovnaya, P., Hashimi, A., Sexton, D.L. et al. BamA self-insertion drives inner-to-outer membrane remodelling in diderm Firmicutes. Nat Commun 17, 2756 (2026). https://doi.org/10.1038/s41467-026-69191-9
Schlüsselwörter: bakterielle Sporen, äußere Membran, BamA, Acetonema longum, Membranumbau