Clear Sky Science · de
Der cGAS‑STING‑Signalweg bei Krebs: Freund oder Feind
Wenn unsere Zellen einen Virusalarm gegen Krebs auslösen
Der Körper besitzt einen mächtigen Einbrecheralarm, der normalerweise eindringende Viren erkennt, indem er fehlplatziertes DNA‑Material wahrnimmt. Dasselbe Alarmsystem, das um zwei Moleküle namens cGAS und STING aufgebaut ist, reagiert auch auf beschädigte DNA in Krebszellen. Manchmal hilft diese Reaktion dem Immunsystem, Tumoren aufzuspüren; andere Male schützt sie stillschweigend den Krebs und fördert seine Ausbreitung. Dieser Übersichtsartikel untersucht, warum dieser Signalweg sowohl als Beschützer als auch als Komplize wirken kann und wie Ärzte lernen könnten, ihn zum Vorteil des Körpers umzuschalten.
Wie eine zelluläre Stolperdraht‑Falle Gefahr erkennt
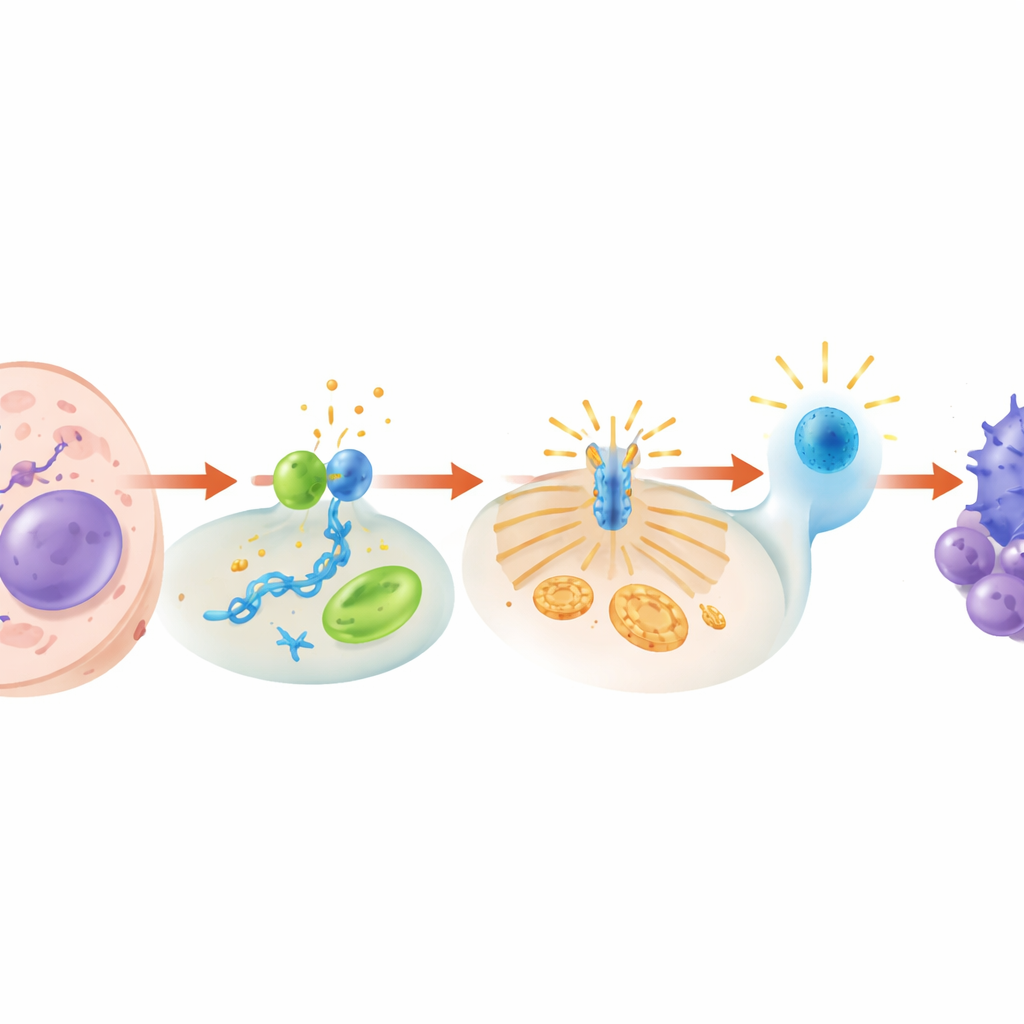
In gesunden Zellen ist DNA sicher im Zellkern und in den Mitochondrien verpackt. Wenn doppelsträngige DNA lose im Zytoplasma auftaucht, signalisiert das meist eine Infektion oder schwere Schädigung. Das Protein cGAS sitzt bereit, um solche DNA‑Fragmente zu erkennen. Wenn es an sie bindet, produziert es ein kleines ringförmiges Botenmolekül namens cGAMP. cGAMP aktiviert dann ein anderes Protein, STING, das an inneren Membranen sitzt. Aktiviertes STING startet zwei große Alarmwege: einen, der Typ‑I‑Interferone produziert — zentrale immunverstärkende Signale — und einen anderen, der entzündungsfördernde Faktoren einschaltet. Zusammen rufen und aktivieren sie Immunzellen, die virusinfizierte oder entartete Zellen angreifen können.
Warum der Sensor unser eigenes Genom nicht angreift
Da jede Zelle voller DNA ist, stellt sich die zentrale Frage, wie cGAS vermeidet, das körpereigene Erbgut für einen Eindringling zu halten. Der Artikel beschreibt mehrere Schutzebenen. Physische Barrieren halten die meiste DNA im Kern oder in den Mitochondrien fern von cGAS, das häufig an der Zellmembran verankert ist. Wenn DNA‑Brüche auftreten, räumen Reparatursysteme und Verdauungsenzyme lose Fragmente schnell weg, bevor sie ein gefährliches Niveau erreichen. Selbst im Zellkern, wo sich ebenfalls cGAS findet, ist es eng an verpackte DNA gebunden und daran gehindert, aktiviert zu werden. Während der Zellteilung, wenn die Kernhülle vorübergehend verschwindet, schalten zusätzliche chemische Mechanismen cGAS und seine nachgeschalteten Partner ab, um unbeabsichtigte Selbstangriffe zu verhindern.
Wie derselbe Alarm Krebs bekämpfen oder befeuern kann
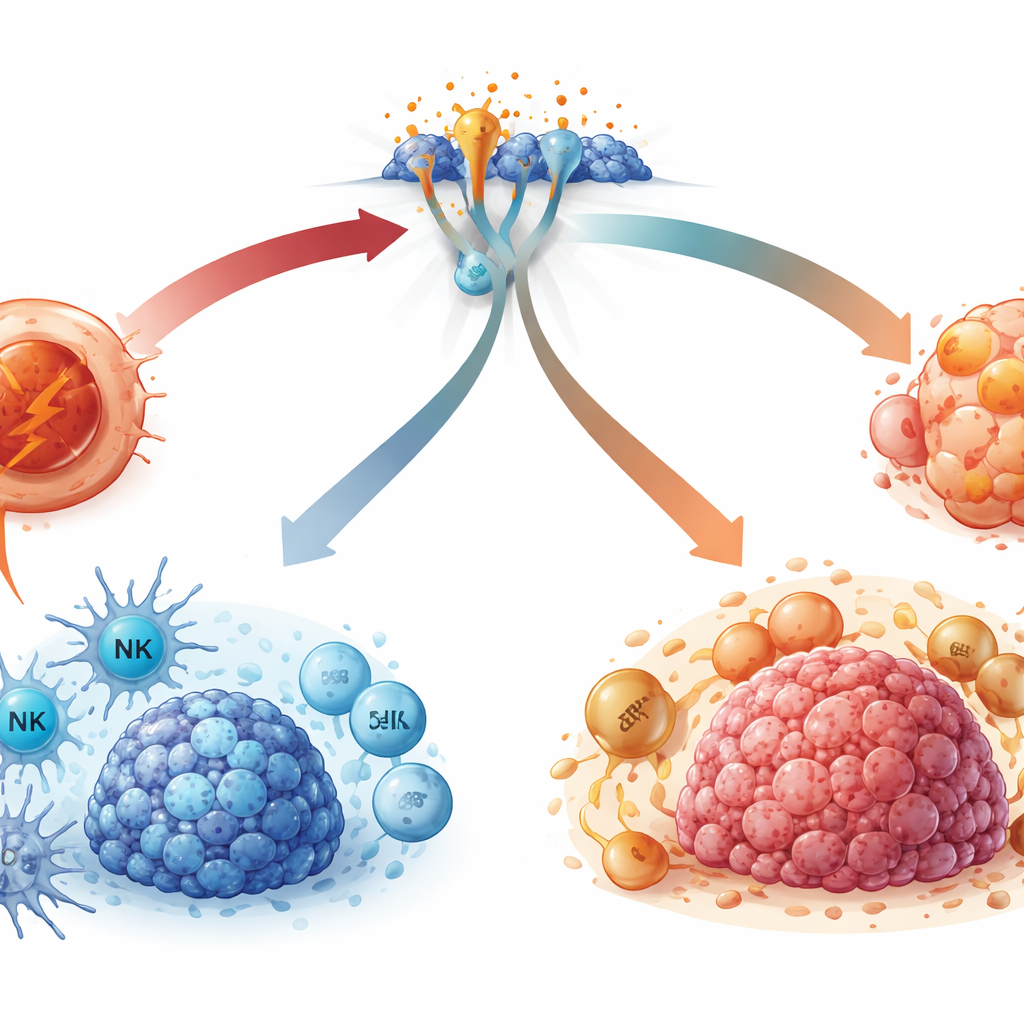
In Tumoren sind Chromosomen oft instabil, es entstehen Mikrokerne und DNA tritt ins Zytoplasma über. Das kann den cGAS‑STING‑Alarm chronisch aktivieren. Unter den richtigen Bedingungen — starke, kurzzeitige Aktivierung in und um tumorbekämpfende Immunzellen — fördert dies die Freisetzung von Interferonen, unterstützt dendritische Zellen bei der Präsentation von Tumormaterial und hält Killer‑T‑Zellen sowie natürliche Killerzellen aktiv. Es begünstigt auch, dass beschädigte, präkanzeröse Zellen das Teilen einstellen, altern oder absterben. Wenn das Signal jedoch schwach, aber dauerhaft in Krebszellen präsent ist, können diese sich anpassen, indem sie den nützlichen Interferon‑Ast dämpfen und alternative Verzweigungen des Weges bevorzugen. Diese alternativen Routen erhöhen Faktoren wie PD‑L1 auf Tumorzellen, ziehen regulatorische Immunzellen an, die Attacken abschwächen, und aktivieren nicht‑klassische entzündliche Programme, die Invasion und Metastasierung unterstützen.
Den Alarm für Therapien umverdrahten
Da cGAS‑STING das Immunsystem wecken kann, versuchen viele experimentelle Behandlungen, ihn gezielt zu stimulieren. Synthetische Botenstoffe und metallbasierte Partikel werden erprobt, um die STING‑Aktivität zu steigern, häufig kombiniert mit Strahlung oder Medikamenten, die Tumor‑DNA schädigen und mehr erkennbare Fragmente erzeugen. Andere Ansätze zielen darauf ab, Enzyme zu blockieren, die cGAMP außerhalb von Zellen abbauen, damit dieser Bote den Alarm an benachbarte Immunzellen weitergeben kann. Zugleich warnt die Übersicht, dass das bloße Einschalten des Weges nicht ausreicht: Lang anhaltende oder fehlplatzierte Aktivierung kann suppressive T‑ und B‑Zellen ausbreiten, PD‑L1 erhöhen oder schädliche Entzündungen verursachen. Erfolgreiche Strategien werden wahrscheinlich präzise Liefermechanismen mit Checkpoint‑blockierenden Antikörpern koppeln und Patienten sorgfältig auswählen, deren Tumoren noch eine ansprechbare Version des Signalwegs besitzen.
Den Sweet Spot zwischen Hilfe und Schaden finden
Die Autoren kommen zu dem Schluss, dass cGAS‑STING bei Krebs weder von Natur aus gut noch schlecht ist. Stattdessen verhält es sich wie ein fein justierter Regler, dessen Wirkungen davon abhängen, wo das Signal entsteht, wie stark es ist, wie lange es anhält und welche Zellen es empfangen. In schnell veränderlichen Tumoren mit instabilen Chromosomen kann derselbe Alarm, der einst Krebs unterdrückt haben könnte, umverdrahtet worden sein, sodass er dessen Wachstum und Ausbreitung fördert. Zukünftige Therapien müssen diesen Kontext lesen und den Weg dann zu kurzen, fokussierten Impulsen bewegen, die Immunverteidiger mobilisieren, während chronische Aktivierung vermieden wird, die tumorfreundliche Entzündung nährt. Zu lernen, dieses zweischneidige Alarmsystem zu kontrollieren, könnte sowohl Krebsbehandlungen als auch in anderen Kontexten Therapien zur Gewebeheilung verbessern.
Zitation: Li, Q., Song, Q., Ma, L. et al. The cGAS-STING pathway in cancer: friend or foe. Cell Death Dis 17, 374 (2026). https://doi.org/10.1038/s41419-026-08607-2
Schlüsselwörter: cGAS‑STING, Krebsimmunität, Tumormikroumgebung, angeborene Immunerkennung, Immuntherapie