Clear Sky Science · de
Pellino1-mTOR/S6K1-Signalachse ist ein zentraler Pathogeneseweg bei der Entwicklung der polyzystischen Nierenerkrankung
Wenn Nierenzysten und Krebs einen verborgenen Schalter teilen
Polyzystische Nierenerkrankung und Nierenkrebs wirken wie sehr unterschiedliche Erkrankungen, doch sie teilen ein gefährliches Merkmal: unkontrolliertes Wachstum innerhalb der Niere. Diese Studie deckt einen molekularen „Schalter“ auf, der offenbar sowohl das Wachstum der mit Flüssigkeit gefüllten Zysten bei der autosomal-dominanten polyzystischen Nierenerkrankung (ADPKD) als auch die Aggressivität eines häufigen Nierenkrebses antreibt. Das Verständnis dieses gemeinsamen Wachstumsmotors könnte neue Behandlungsansätze eröffnen, die das Fortschreiten zur Niereninsuffizienz verlangsamen und möglicherweise das Krebsrisiko bei gefährdeten Patientinnen und Patienten senken.
Eine verbreitete Nierenerkrankung mit stillen, aber schweren Folgen
ADPKD gehört zu den häufigsten vererbten Nierenerkrankungen und betrifft etwa einen von tausend Menschen. Im Laufe vieler Jahre knospen zahllose kleine, mit Flüssigkeit gefüllte Bläschen oder Zysten von den Nierentubuli ab und vergrößern sich allmählich. Beim Wachstum quetschen diese Zysten das gesunde Gewebe, schwächen die Nierenfunktion und führen bei etwa der Hälfte der Betroffenen schließlich zu Nierenversagen, das Dialyse oder Transplantation erfordert. Menschen mit ADPKD entwickeln zudem häufiger ein Nierenzellkarzinom, eine Form von Nierenkrebs, doch die biologischen Verknüpfungen zwischen Zystenwachstum, Entzündung und Tumorbildung blieben bislang unklar.
Entzündungssignale, die die Niere in Richtung Schaden treiben
Die Autorinnen und Autoren konzentrierten sich auf ein Protein namens Pellino1 (Peli1), das Teil des zellulären Systems ist, andere Proteine mit kleinen Ubiquitin-Molekülen zu markieren und so ihr Schicksal zu beeinflussen. Peli1 wird durch Toll‑like‑Rezeptoren aktiviert, Wächter auf Nierenzellen, die Gefahrensignale von Infektionen oder Gewebeschäden erkennen. Sind diese Rezeptoren aktiviert, lösen sie Entzündungswege aus, die kurzfristig schützen, bei andauernder Aktivierung jedoch zu chronischem Schaden beitragen können. Bei der Auswertung öffentlicher Krebsdatenbanken und von Gewebeproben aus Patientinnen und Patienten mit klarem Nierenzellkarzinom fanden die Forschenden auffällig erhöhte Peli1‑Spiegel in Tumoren im Vergleich zu normalem Nierengewebe. Patientinnen und Patienten mit Peli1‑reichen Tumoren hatten eine schlechtere Überlebensrate und ein schnelleres Fortschreiten der Erkrankung, was darauf hindeutet, dass dieses Protein schädliches Wachstum fördert.
Wie zusätzliches Peli1 gesunde Nieren zystisch werden lässt
Um zu untersuchen, was Peli1 in lebenden Nieren bewirkt, erzeugten die Forschenden Mäuse, bei denen humanes Peli1 mit dem Antibiotikum Doxycyclin eingeschaltet werden konnte. Nach Aktivierung von Peli1 entwickelten die Tiere vergrößerte, zystengefüllte Nieren, starke Proteinurie und steigende Blutwerte, die Niereninsuffizienz anzeigen. Die mikroskopische Analyse zeigte eine weitverbreitete Aufblähung der Tubuli, Vernarbung dazwischen und einen Einstrom von Immunzellen. Gene, die auf den Entzündungsregulator NF‑κB ansprechen, darunter mehrere Zytokine und Chemokine, waren stark erhöht. Wichtig ist, dass das Absetzen von Doxycyclin und damit das Absinken der Peli1‑Spiegel zu einer deutlichen Verbesserung des Nierenbildes führten, was zeigt, dass übermäßiges Peli1 allein ausreicht, zystische Schäden auszulösen, und sein Entfernen deren Besserung ermöglicht.
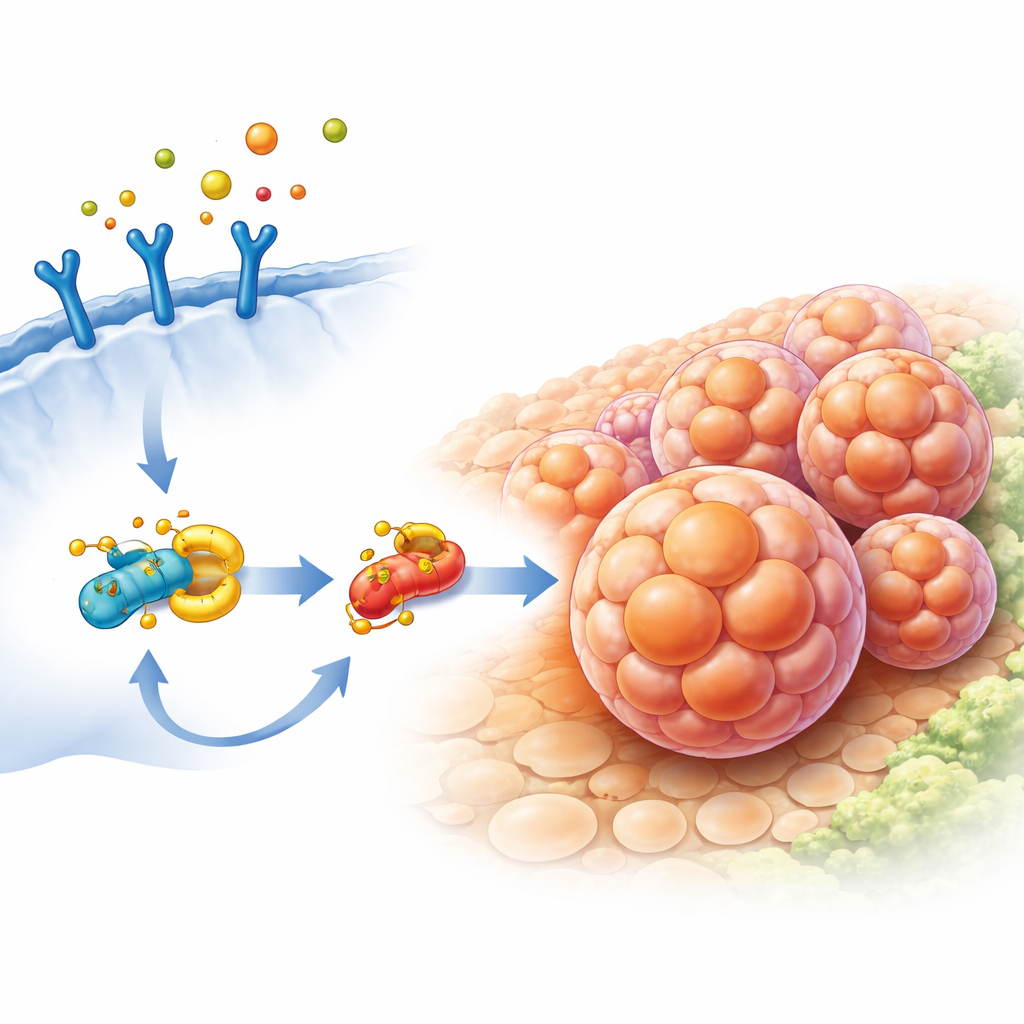
Der Wachstumsweg, der Zysten und Krebs verbindet
Bei tiefergehenden Untersuchungen erforschte das Team, wie Peli1 das Wachstum der zystenauskleidenden Zellen fördert. Sie entdeckten, dass Peli1 physisch an ein Protein namens S6K1 bindet, einen Schlüsselkomponenten des bekannten mTOR‑Wachstumswegs, der Zellen sagt, wann sie sich teilen und neue Proteine herstellen sollen. Anstatt S6K1 für den Abbau zu markieren, heftete Peli1 eine spezifische Form von Ubiquitin‑Ketten an, die S6K1 stabilisierte und aktiv hielt. Nieren von Mäusen mit Peli1‑Überexpression zeigten eine verstärkte Aktivierung des S6K1‑Targets, des S6‑Proteins, insbesondere in zystenauskleidenden Zellen. In menschlichen Nierenzelllinien beschleunigte eine Erhöhung von Peli1 die Zellteilung und -bewegung, während eine Reduktion von Peli1 S6K1 weniger stabil machte. Zusammen zeichnen diese Ergebnisse eine Abfolge: Entzündungsrezeptoren aktivieren Peli1, Peli1 stärkt S6K1 und mTOR‑Signale, und dies treibt das Überwachsen und die Migration von Tubuluszellen voran, die Zysten bilden und sich potenziell zu Tumoren entwickeln können.
Was das für Patientinnen und Patienten und künftige Therapien bedeutet
Diese Arbeit positioniert Peli1 als entscheidende Verbindung zwischen Entzündung und unkontrolliertem Wachstum in der Niere. Indem es S6K1 stabilisiert und mTOR‑Signale verstärkt, verwandelt Peli1 offenbar chronischen entzündlichen Stress in expandierende Zysten und in manchen Fällen in Malignität. Zwar gibt es bereits Wirkstoffe, die mTOR bremsen, doch ihre Nebenwirkungen begrenzen die Langzeitanwendung bei chronischen Nierenerkrankungen. Das direkte Anvisieren von Peli1 oder seiner Interaktion mit S6K1 könnte einen selektiveren Weg bieten, diesen schädlichen Pfad zu dämpfen und gleichzeitig andere lebenswichtige Zellfunktionen zu erhalten. Obwohl weitere Forschung, insbesondere beim Menschen, nötig ist, stellt die Peli1–mTOR/S6K1‑Achse nun ein vielversprechendes Ziel für Therapien dar, die das Fortschreiten der ADPKD verlangsamen und die Ergebnisse für Patientinnen und Patienten mit erhöhtem Nierenkrebsrisiko verbessern sollen.
Zitation: Kim, S., Kim, MH., Ko, BK. et al. Pellino1-mTOR/S6K1 signaling axis is a key pathogenesis for the development of polycystic kidney disease. Cell Death Dis 17, 296 (2026). https://doi.org/10.1038/s41419-026-08479-6
Schlüsselwörter: polyzystische Nierenerkrankung, Nierenkrebs, Entzündung, mTOR-Signalübertragung, Ubiquitin-Ligase Peli1