Clear Sky Science · de
Mineralisierte DNA-Tetraeder-hydrogels: ein dual funktionales Gerüst zur Immunmodulation und Knochenregeneration
Brüche auf klügere Weise heilen
Knochenverletzungen durch Unfälle, Infektionen oder Operationen können Lücken hinterlassen, die der Körper allein nur schwer repariert. Ärzte verwenden oft Knochen aus anderen Körperbereichen oder von Spendern, doch diese Optionen sind begrenzt und können Komplikationen verursachen. Diese Studie beschreibt ein neues, im Labor hergestelltes Material aus DNA und Mineralien, das darauf ausgelegt ist, sowohl schädliche Entzündungen zu dämpfen als auch neues Knochengewebe anzuregen — und damit möglicherweise eine schonendere und wirksamere Möglichkeit bietet, schwierige Defekte zu schließen.
Ein weiches Gerüst aus DNA
Die Forschenden begannen mit einem ungewöhnlichen Baustoff: DNA, geformt zu winzigen, pyramidenähnlichen Gerüsten, sogenannten Tetraedern. Diese DNA-Rahmen bilden von selbst ein weiches, wasserreiches Netzwerk, bekannt als Hydrogel, das der körpereigenen Matrix um Zellen ähnelt. Ein DNA-Hydrogel kann zwar biologische Signale transportieren, baut sich im Körper aber häufig zu schnell ab und beeinflusst das Immunsystem nur wenig. Um dem entgegenzuwirken, entwickelten die Wissenschaftler eine neue Version namens Cap-gel, indem sie gezielt Calciumphosphat-Mineralien — der gleichen Mineralfamilie wie im Knochen — im gesamten DNA-Netzwerk wuchsen ließen. Das ergab ein widerstandsfähigeres, stabileres Gel, das Mineralionen speichert und die DNA-Strukturen in einem präzisen, dreidimensionalen Muster präsentiert. 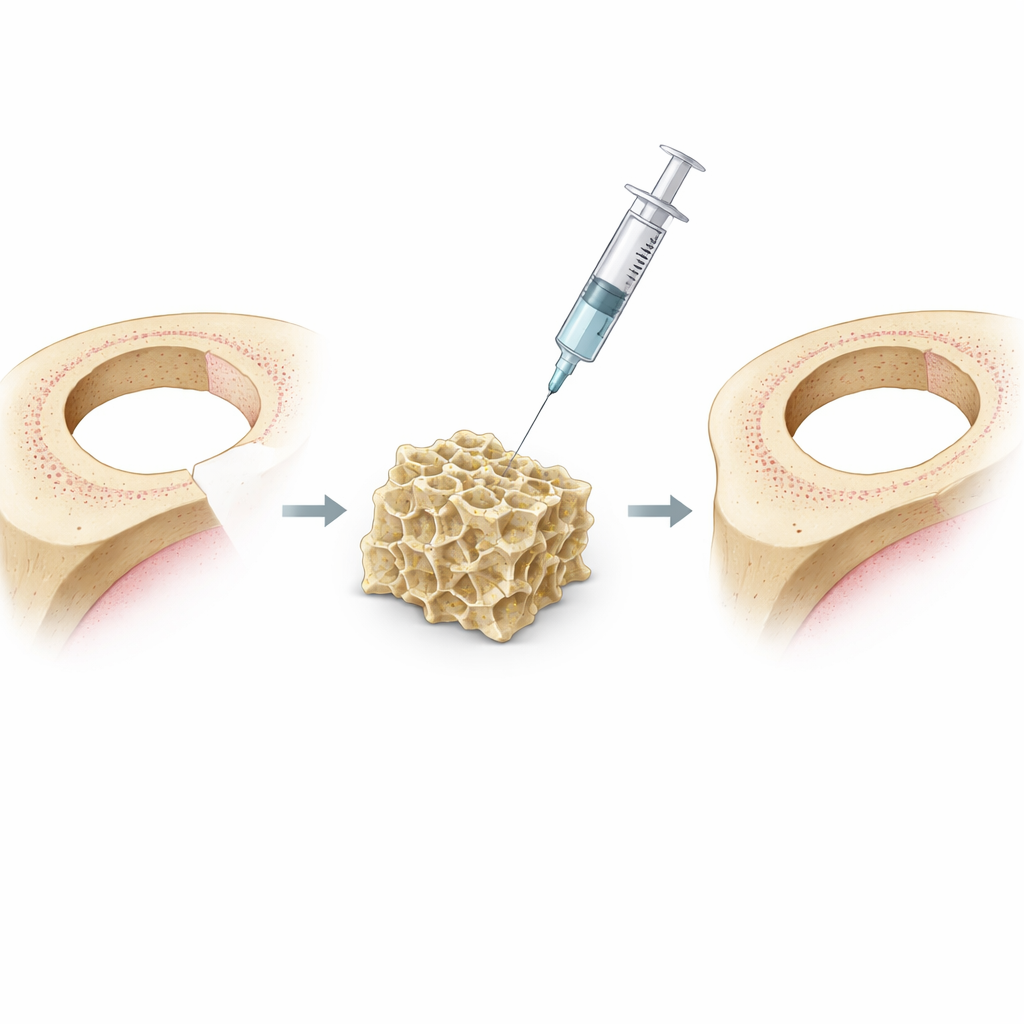
Stärkere, mineralreiche Stütze für Knochenwachstum
Detaillierte Labortests zeigten deutliche Unterschiede zwischen dem mineralisierten Cap-gel und dem einfachen DNA-Hydrogel. Mit Methoden, die chemische Bindungen und Kristallstrukturen untersuchen, bestätigten die Forschenden, dass das Gel knochenähnliche Calciumphosphat-Kristalle in der weichen DNA-Matrix enthält. Unter leistungsstarken Mikroskopen zeigte Cap-gel raue, kristallverzierte Oberflächen und winzige Mineraldomänen, die in den Poren des Gels wuchsen, während die nicht mineralisierte Variante glatt und strukturlos erschien. Mechanische Messungen ergaben, dass Cap-gel deutlich höhere Druckkräfte aushält und daher weniger leicht in einem Defekt kollabiert. Wichtig ist, dass das Material Calciumionen über drei Wochen gleichmäßig freisetzte — passend zum verlängerten Bedarf an Mineralversorgung während der Knochenheilung — und den Abbau des zugrunde liegenden DNA-Netzwerks verlangsamte.
Das Immunsystem beruhigen und gleichzeitig Reparatur anstoßen
Die Knochenheilung steht in engem Zusammenhang mit dem Immunsystem, insbesondere mit einer weißen Blutzellart, den Makrophagen, die entweder eine zerstörerische, entzündliche Rolle oder eine heilungsfördernde „aufräumen und wiederaufbauen“-Rolle einnehmen können. In Zellkulturen schoben sowohl das einfache DNA-Hydrogel als auch Cap-gel Makrophagen weg von einem aggressiven Zustand und hin zu diesem reparativen Modus, senkten entzündliche Signale und stärkten schützende, antiinflammatorische Faktoren. Cap-gel ging einen Schritt weiter und veranlasste Makrophagen, ein kraftvolles knochenwachstumsförderndes Signal namens BMP2 freizusetzen. Gleichzeitig schalteten Knochenvorläuferzellen, die direkt mit Cap-gel in Kontakt kamen, wichtige knochenbezogene Gene ein, produzierten mehr Knochenmatrixproteine und bildeten zahlreiche Mineralnodule. Die Befunde sprechen für einen doppelten Wirkmechanismus: Das aus dem Gel freigesetzte Calcium aktivierte einen Wachstumsweg innerhalb der Zellen, während Immun‑Signale von umprogrammierten Makrophagen einen zusätzlichen Anstoß zur Knochenbildung gaben. 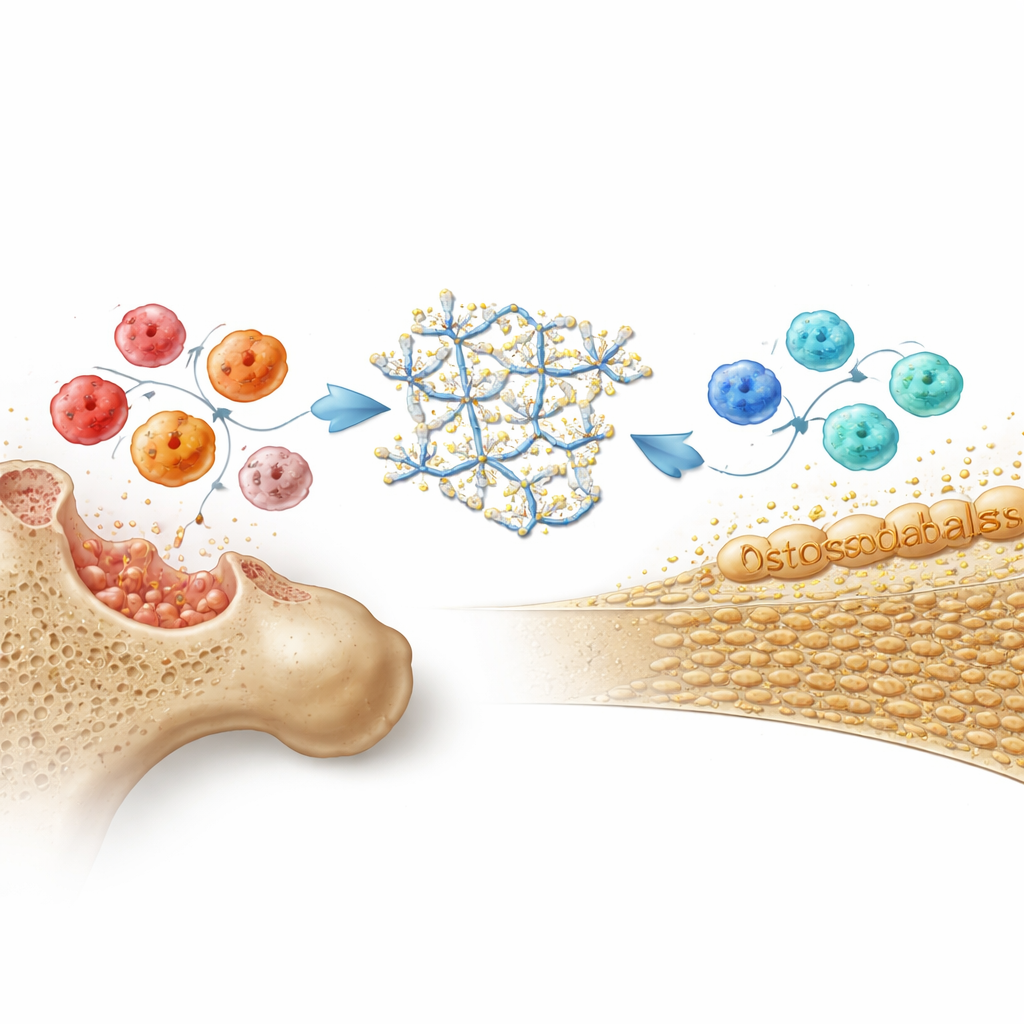
Knochenregeneration in lebenden Tieren unterstützen
Um zu prüfen, ob sich die Laborergebnisse in echte Heilung umsetzen lassen, testete das Team Cap-gel an Ratten mit kleinen kreisförmigen Löchern in ihren Schädelknochen — ein Standardmodell für einen „kritisch großen“ Defekt, der von selbst nicht verschließt. Das Material erwies sich in Bluttests als sicher und schädigte keine wichtigen Organe. Wurde Cap-gel in die Defekte eingebracht, zeigten Scans über mehrere Wochen mehr neu gebildeten Knochen, der die Lücken füllte, verglichen mit unbehandelten Stellen oder solchen, die nur DNA- oder nicht-mineralisiertes Hydrogel erhielten. Frühzeitig reduzierte Cap-gel Marker schädlicher Entzündung und erhöhte das Vorkommen pro-heilender Makrophagen sowie BMP2 am Verletzungsort. Mit der Zeit zeigten Gewebefärbungen dichtere Kollagennetzwerke, stärkere Expression knochenbildender Enzyme und zusammenhängenderes, plattenartiges neues Knochengewebe in der Cap-gel-Gruppe — Hinweise darauf, dass das Material sowohl die frühe Aufräumphase als auch die spätere Wiederaufbauphase der Heilung unterstützte.
Auf dem Weg zu Knochenreparaturmaterialien der nächsten Generation
Insgesamt zeigt die Studie, dass sorgfältig entworfene DNA-basierte Hydrogele mehr sein können als passive Füllstoffe: Durch die Kombination eines programmierbaren DNA-Gerüsts mit knochenähnlichen Mineralien beruhigt Cap-gel gleichzeitig die lokale Immunantwort und versorgt das Gewebe mit Bausteinen für neues Knochenwachstum. Für Patientinnen und Patienten könnte ein solches „dual funktionales“ Gerüst eines Tages die Abhängigkeit von Spenderknochen verringern und eine besser vorhersagbare Möglichkeit bieten, komplexe kraniale oder faziale Defekte zu heilen. Zwar sind weitere Tests in größeren, belasteten Knochen und Langzeitsicherheitsstudien noch erforderlich, doch diese Arbeit skizziert eine vielversprechende Strategie für zukünftige Materialien, die sowohl mit dem Immunsystem als auch dem Skelett kommunizieren, um den körpereigenen Reparaturprozess zu lenken.
Zitation: Yao, L., Sun, J., Liu, Z. et al. Mineralized DNA tetrahedron-structured hydrogels: a dual-functional Scaffold for immunomodulation and bone regeneration. Bone Res 14, 50 (2026). https://doi.org/10.1038/s41413-026-00530-8
Schlüsselwörter: Knochenregeneration, DNA-Hydrogel, Biomaterialien, Immunmodulation, Calciumphosphat