Clear Sky Science · de
Faktor VIII stellt Knochenparameter wieder her und moduliert Proteo‑Metabolom der Muskulatur bei männlichen Faktor‑VIII‑Knockout‑Mäusen
Warum ein Gerinnungsprotein für Knochen und Muskeln wichtig ist
Menschen mit Hämophilie A sind vor allem für Blutungsprobleme bekannt, viele entwickeln jedoch auch brüchige Knochen und schwache Muskulatur. Diese Studie stellt eine einfache, aber wichtige Frage: Beeinflusst das in der Hämophilie fehlende Gerinnungsprotein, genannt Faktor VIII, direkt das Wachstum und die Gesundheit von Knochen und Muskeln? Anhand von Mäusen, denen Faktor VIII vollständig fehlt, und indem einige dieser Tiere rekombinantes Protein erhalten, verfolgen die Forschenden, wie dieses einzelne Molekül das Skelett, die Blutgefäße im Knochen und sogar die Chemie der Muskelzellen beeinflussen kann.
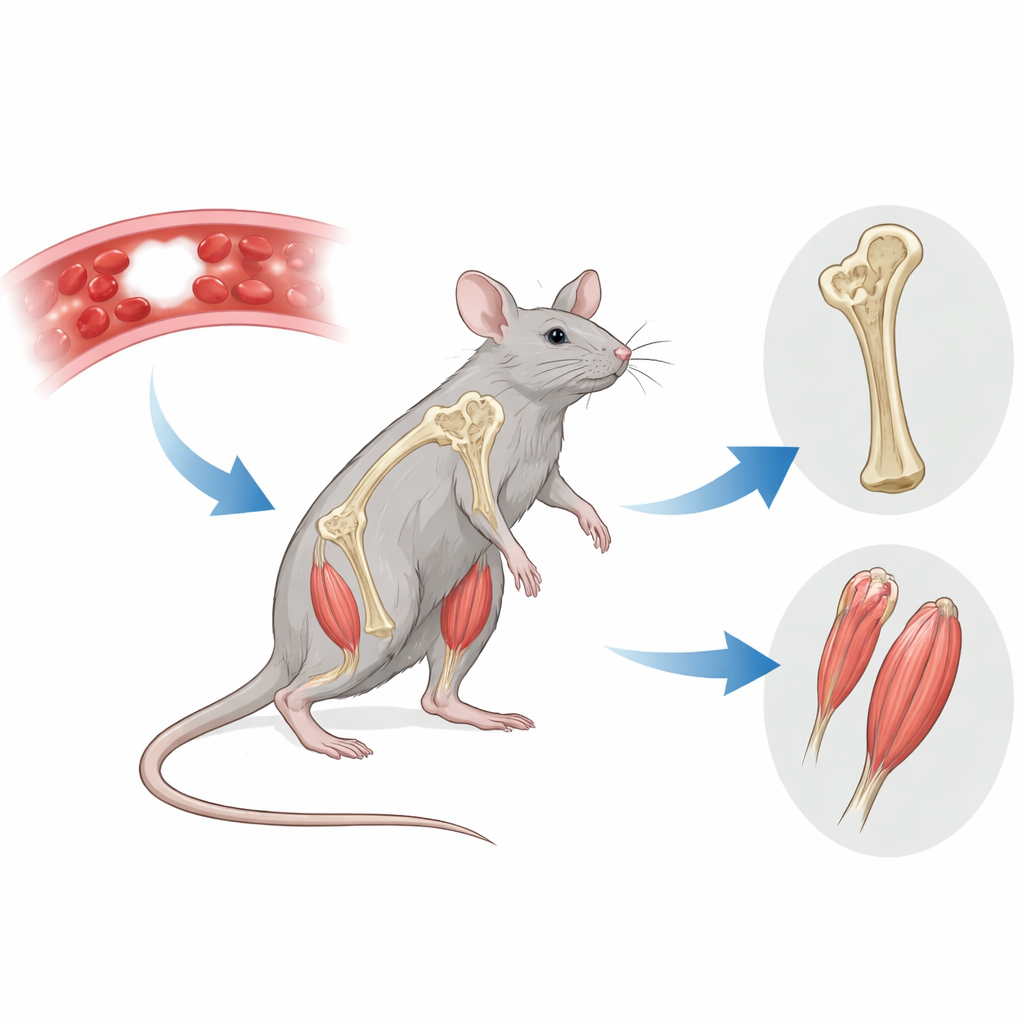
Schwache Knochen in Abwesenheit eines Schlüsselproteins
Das Team untersuchte zunächst die Knochen junger und junger erwachsener männlicher Mäuse ohne Faktor VIII. Mit hochauflösenden Röntgenscans zeigte sich bei diesen Tieren ein osteoporoseähnliches Knochenbild: weniger spongiöse Knochenmasse, weniger feine Stützbalken im Inneren des Knochens und größere Hohlräume. Die Knochenmineraldichte war tendenziell ebenfalls niedriger. Bei genauerer mikroskopischer Betrachtung fiel auf, dass das feine Netz kleiner Blutgefäße in der Nähe der wachsenden Knochenenden reduziert war, besonders die Venen und Kapillaren, die das Knochengewebe versorgen. Gleichzeitig war die Zahl der knochenaufbauenden Zellen (Osteoblasten) bei jungen Tieren deutlich vermindert, was darauf hindeutet, dass das Skelett während der wichtigen Wachstumsphase Schwierigkeiten hat, ausreichend neuen Knochen aufzubauen.
Wiederherstellung von Faktor VIII baut Knochen und Gefäße wieder auf
Um zu klären, ob dieser Schaden umkehrbar ist, behandelten die Forschenden die Faktor‑VIII‑defizienten Mäuse mehrere Wochen lang mit wöchentlichen Infusionen eines rekombinanten Faktor‑VIII‑Proteins. Nach der Behandlung verbesserte sich die innere Struktur der langen Knochen deutlich: Es gab mehr spongiöse Substanz, mehr der feinen Stützbalken und kleinere Abstände zwischen ihnen. Das Kleingefäßnetz im Knochenmark erholte sich ebenfalls annähernd normal, insbesondere Venen und Kapillaren. Die Zahl der knochenaufbauenden Zellen nahm zu, während die der knochenabbauenden Zellen abnahm. Wichtig ist, dass ähnliche Vorteile sowohl mit pegylierten als auch mit nicht‑pegylierten Varianten des Proteins beobachtet wurden, was darauf hindeutet, dass die positiven Effekte vom Faktor VIII selbst und nicht von chemischen Modifikationen des Wirkstoffs ausgehen. Zusammengenommen deuten diese Ergebnisse darauf hin, dass Faktor VIII hilft, ein gesundes Gleichgewicht zwischen Knochenaufbau, Knochenabbau und Blutversorgung im Skelett aufrechtzuerhalten.
Unerwartete Muskelveränderungen und veränderte Zellchemie
Das Bild in der Muskulatur war komplexer. Junge Faktor‑VIII‑defiziente Mäuse hatten tatsächlich schwerere Beinscheiben mit größeren Muskelfasern als normal, doch im Verlauf der Reifung verschoben sich ihre Fasertypen in Richtung eines Typs, der schnelle, kraftvolle Kontraktionen bevorzugt, aber leicht ermüdet. Detaillierte Protein‑ und Metabolitenanalysen zeigten, dass Muskeln ohne Faktor VIII eine gedämpfte Aktivität in den Energiezentralen (Mitochondrien) und in der Maschinerie der Proteinbiosynthese aufwiesen, begleitet von Verschiebungen in energierelevanten Molekülen und Antioxidantien. Diese Veränderungen deuten auf Muskeln hin, die mehr Treibstoff benötigen und mit einer geringeren „metabolischen Ökonomie“ arbeiten, was letztlich in früher Ermüdung und Schwäche resultieren könnte — ähnlich dem, was viele Menschen mit Hämophilie erleben.
Partielle Wiederherstellung von Muskel‑ und Immunreaktionen
Erhielten die Mäuse rekombinantes Faktor VIII, bewegte sich ein Teil der abnormen Muskelchemie wieder in Richtung Normalwerte, und die Muskelfasern wurden etwas kleiner und homogener. Die Grundzusammensetzung der Fasertypen kehrte jedoch nicht vollständig zurück, und strukturelle Muskelveränderungen ließen sich nur teilweise korrigieren. In einem separaten Experiment verletzten die Forschenden die Beinmuskulatur mit einem Toxin, um schwere Schäden zu simulieren. Mäuse ohne Faktor VIII zeigten eine reduzierte frühe Rekrutierung pro‑inflammatorischer Makrophagen — Immunzellen, die beim Entfernen von Trümmern helfen und die Reparatur anstoßen —, doch dieser Defekt wurde durch die Faktor‑VIII‑Behandlung teilweise behoben. Selbst so unterschieden sich vollständig regenerierte Muskeln in behandelten Mäusen weiterhin von denen normaler Tiere, was darauf hindeutet, dass einmal eingetretene frühe entwicklungs‑ oder gefäßbedingte Veränderungen nicht vollständig später im Leben rückgängig gemacht werden können.
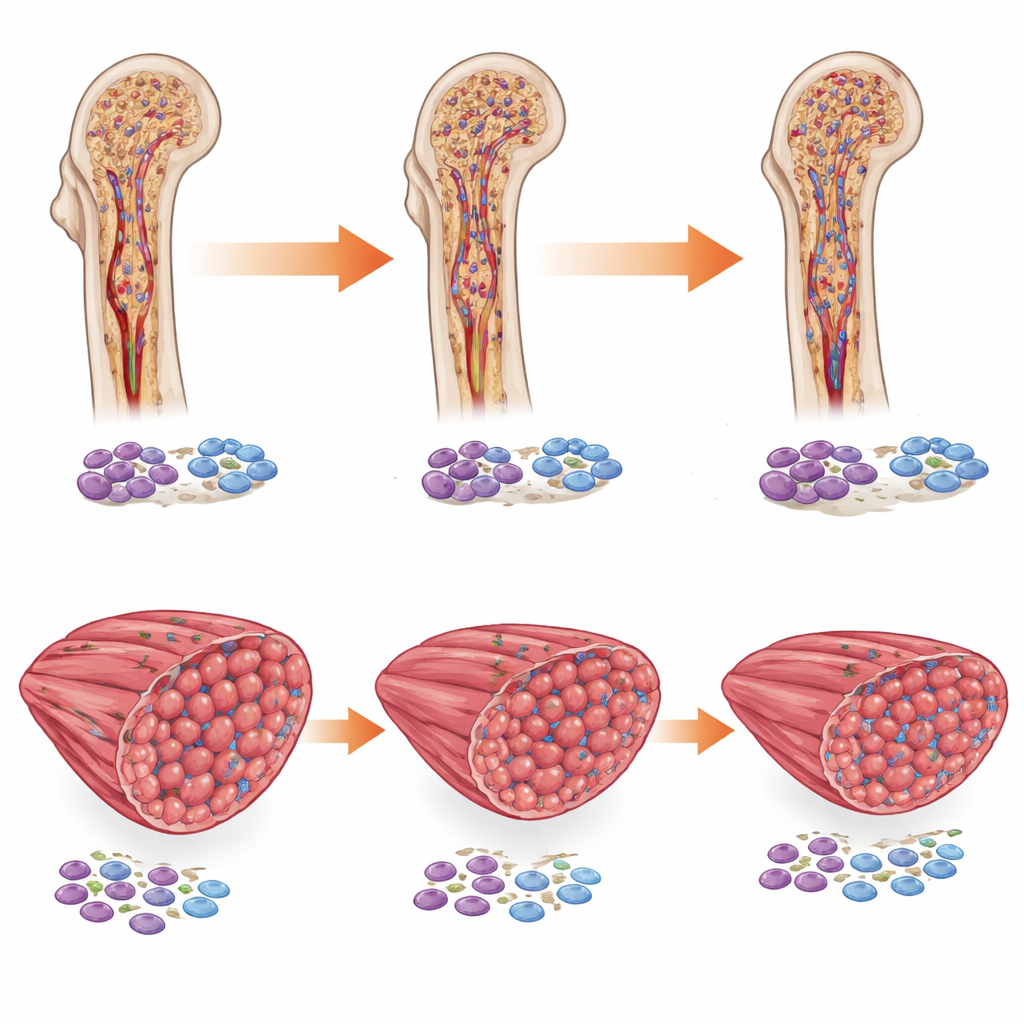
Was das für Menschen mit Hämophilie bedeutet
Insgesamt zeigt die Studie, dass Faktor VIII mehr ist als ein Gerinnungsfaktor: Er prägt die Knochenstruktur, unterstützt die feinen Blutgefäße, die wachsende Knochen versorgen, und beeinflusst, wie Muskeln Energie nutzen und sich von Verletzungen erholen. Die Zufuhr von Faktor VIII bei Mäusen kann Knochenschwäche weitgehend reparieren und die Blutversorgung der Knochen verbessern, während die Muskelparameter nur teilweise normalisiert werden. Für Menschen mit Hämophilie A stützen diese Befunde eine frühe und kontinuierliche Faktor‑VIII‑Substitution zum Schutz der Knochengesundheit und legen nahe, dass zusätzliche Strategien nötig sein könnten, um Muskelschwäche und frühe Gebrechlichkeit vollständig zu adressieren.
Zitation: Babuty, A., Muñoz-Garcia, J., Christophe, O.D. et al. Factor VIII restores bone parameters and modulates muscle proteo-metabolome in Factor VIII knockout male mice. Bone Res 14, 30 (2026). https://doi.org/10.1038/s41413-025-00485-2
Schlüsselwörter: Hämophilie A, Faktor VIII, Knochengesundheit, Skelettmuskulatur, rekombinante Therapie