Clear Sky Science · de
Perineurale Netze in Neuronen der Kleinhirnkerne orchestrieren soziales Verhalten durch Regulierung der neuronalen Aktivität in vom Kleinhirn innervierten Schaltkreisen
Wie ein „Gerüst“ im Gehirn das Sozialleben formen kann
Warum führen Veränderungen in einem kleinen Hirnareal zu weitreichenden Effekten auf das Sozialverhalten von Tieren? Die vorliegende Studie untersucht ein feines Protein-„Gerüst“, das bestimmte Nervenzellen im Kleinhirn umhüllt – einer Region, die lange Zeit vor allem mit Bewegungskontrolle in Verbindung gebracht wurde, inzwischen aber auch mit sozialem Verhalten. An Hand von Mäusen, die Autismus-ähnliche Merkmale zeigen, erforschen die Autorinnen und Autoren, wie Schäden an diesem Gerüst die neuronale Aktivität stören und zu sozialen Schwierigkeiten führen könnten.
Ein verstecktes Netz um Nervenzellen
Einige Neurone sind von einer zuckerreichen, netzartigen Hülle umgeben, den perineuronalen Netzen. Man kann sie sich als flexibles Geflecht vorstellen, das Verbindungen zwischen Nervenzellen stabilisiert. Das Team konzentrierte sich auf diese Netze in den tiefen Kleinhirnkernen, dem wichtigsten Ausgangszentrum des Kleinhirns, das Signale an viele andere Hirnregionen sendet, die an Emotionen, Motivation und sozialer Interaktion beteiligt sind. In zwei verschiedenen Mausmodellen mit Autismus-assoziierten Merkmalen – eines mit vorgeburtlicher Valproinsäure-Exposition und eines mit einer Mutation im Chd8-Gen – war die Zahl der von diesen Netzen umgebenen Neurone in den Kleinhirnkernen deutlich reduziert, während die meisten anderen Hirnareale unverändert wirkten.
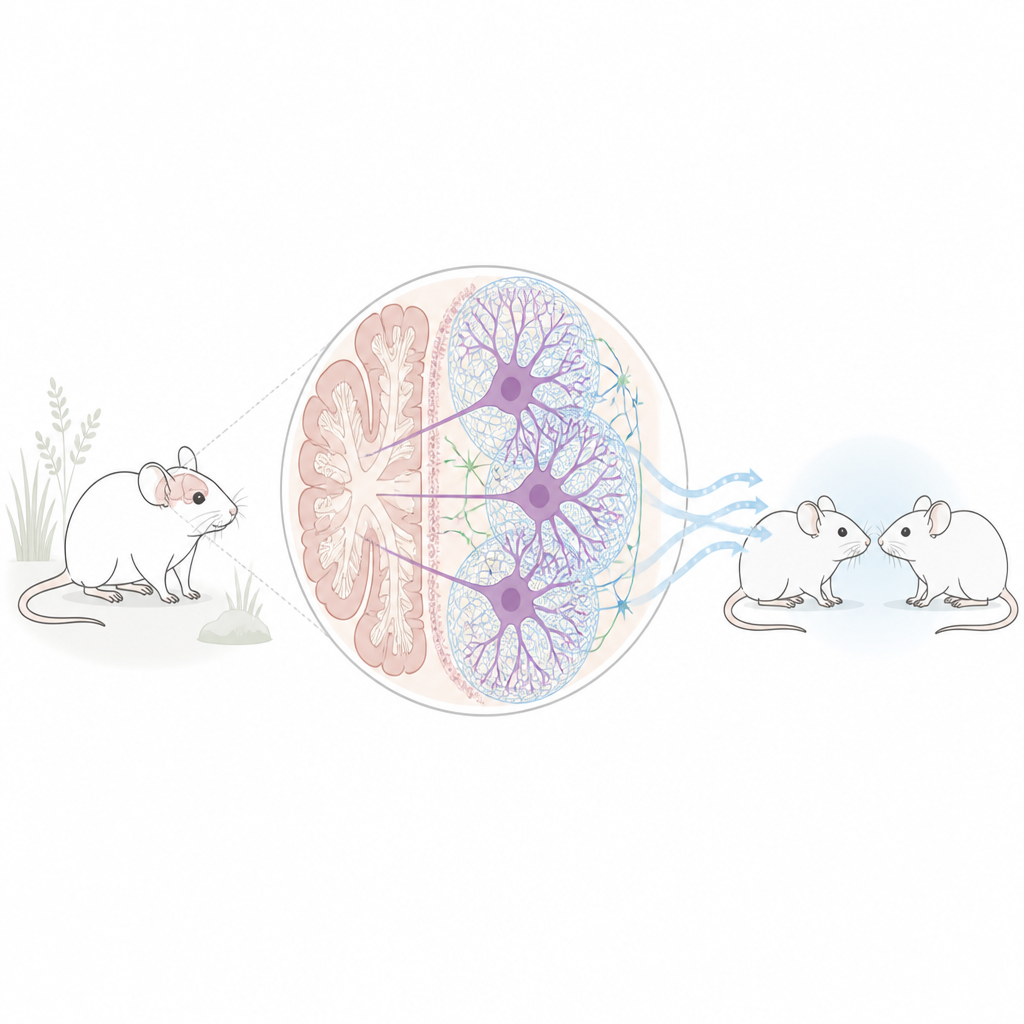
Die Netze auflösen und Verhalten beobachten
Um zu prüfen, ob der Verlust dieser Netze tatsächlich soziale Probleme verursachen kann, setzten die Forschenden ein Enzym ein, das die Netze gezielt in den tiefen Kleinhirnkernen sonst typischer Mäuse verdaut. Nach dieser lokalen Behandlung wurden die Tiere verschiedenen Verhaltensaufgaben unterzogen. In einem standardisierten Drei-Kammer-Test bevorzugen gesunde Mäuse üblicherweise die Gesellschaft eines anderen Mäuses gegenüber einem Objekt und zeigen Neugier gegenüber einem neuen Artgenossen gegenüber einem vertrauten. Mäuse mit beschädigten Netzen zeigten ein vermindertes Interesse am ersten Fremden und eine abgeschwächte Präferenz für einen neuen Sozialpartner – Hinweise auf reduzierte Geselligkeit und soziale Neugier. In einem zweiten Test, bei dem ein Käfiggenosse leichte Fußschocks erhielt, zeigten normale Mäuse vermehrt tröstendes oder überprüfendes Verhalten dem gestressten Partner gegenüber, während netzgeschädigte Mäuse weniger interagierten, was auf eine verringerte soziale Reaktionsbereitschaft hindeutet. Andere Fähigkeiten, wie grundlegende Beweglichkeit und räumliches Gedächtnis, blieben weitgehend intakt.
Von der Zellaktivität zu großräumigen Hirnschaltkreisen
Die Forscherinnen und Forscher untersuchten anschließend, wie der Netzentzug die elektrische Aktivität der Kleinhirnneurone verändert. Sie überwachten Kalziumsignale – einen Proxy für neuronales Feuern – in exzitatorischen Zellen der Kleinhirnkerne, während Mäuse einen Artgenossen erkundeten. In unbehandelten Tieren leuchteten diese Neurone auf, wenn sozialer Kontakt begann. Nach der Netzentfernung verschwand dieser Aktivitätsschub nahezu vollständig. Ein zentraler molekularer Schalter für aktivitätsgesteuerte Genexpression, das Protein CREB1, wurde bei sozialer Interaktion normalerweise in diesen exzitatorischen Neuronen aktiviert, versagte aber, wenn die Netze entfernt wurden. Gleichzeitig stieg das Niveau eines anderen Proteins, ARNT2, in diesen Zellen ungewöhnlich an, selbst in Ruhe. Diese Veränderung war auch in den autismusbasierten Mausmodellen zu beobachten. Nachgeschaltete Hirnregionen, die Eingänge von den Kleinhirnkernen erhalten – etwa der Ruber und Teile des Thalamus sowie des Belohnungssystems – zeigten bei sozialen Tests eine verringerte Aktivierung, wenn kleinhirnare Netze gestört waren, was darauf hindeutet, dass geschwächtes kleinhirnales Output einen weiten sozialen Schaltkreis dämpft.
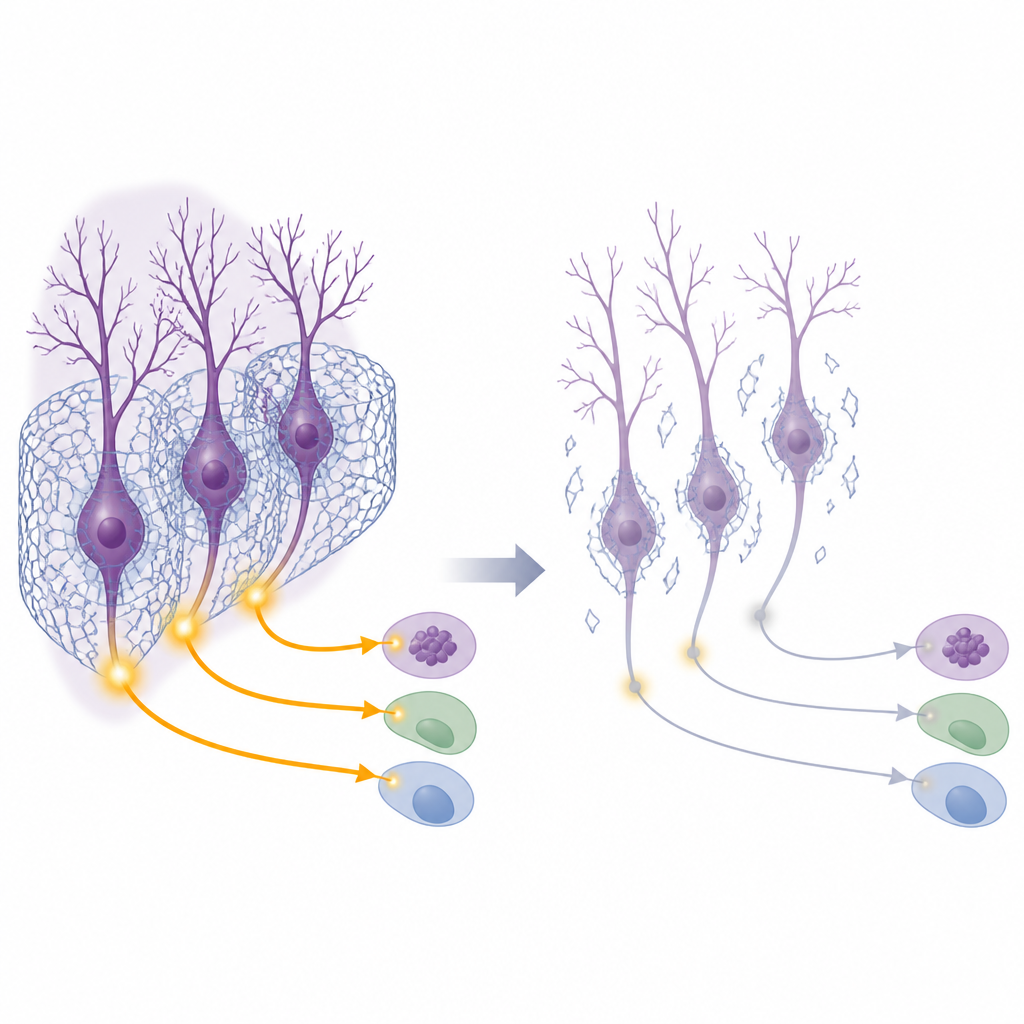
Eine molekulare Bremse einstellen, um soziales Verhalten wiederherzustellen
Da ARNT2 anstieg, wenn die Netze verloren gingen, vermuteten die Forschenden, dass es als Bremse auf Kleinhirnneurone wirken könnte. Sie verwendeten ein virales Werkzeug, um ARNT2 gezielt in Neuronen der Kleinhirnkerne zu reduzieren, und zwar gleichzeitig mit dem Abbau der Netze. Bemerkenswerterweise stellte diese ARNT2-Reduktion die normale soziale Präferenz im Drei-Kammer-Test wieder her und belebte Aktivitätsmarker in entfernten Zielregionen. Wichtig ist, dass die Verringerung von ARNT2 die Netze selbst nicht veränderte, was nahelegt, dass Netze und ARNT2 in unterschiedlichen Schritten desselben Pfades wirken: Die Netze helfen Neuronen, angemessen auf soziale Reize zu reagieren, und ARNT2 kann diese Reaktion je nach Menge unterstützen oder unterdrücken.
Was das für das Verständnis sozialer Schwierigkeiten bedeutet
Für eine nicht-wissenschaftliche Beobachterin oder einen Beobachter legt die Arbeit nahe, dass fragile Protein-Geflechte um spezifische Kleinhirnneurone soziale Hirnschaltkreise im Gleichgewicht halten. Wenn diese Geflechte ausgedünnt sind, wie in autismusbezogenen Mausmodellen, schwächt sich das kleinhirnale Ausgangssignal ab, eine molekulare Bremse wird aktiviert und Hirnregionen, die normalerweise soziales Verhalten koordinieren, werden unteraktiv. Obwohl diese Befunde an Mäusen gewonnen wurden und nicht direkt auf Menschen übertragbar sind, liefern sie eine konkrete biologische Kette, die kleine strukturelle Veränderungen um Zellen mit großräumigen Veränderungen im Sozialverhalten verbindet. Zukünftige Studien beim Menschen sind nötig, um zu klären, ob ähnliche Veränderungen in perineuronalen Netzen und ARNT2 zu sozialen Herausforderungen bei Autismus beitragen.
Zitation: Fujita, K., Zhu, H., Tsuji, C. et al. Perineuronal nets in cerebellar nuclei neurons orchestrate social behaviour via regulation of neuronal activity in circuits innervated by the cerebellum. Transl Psychiatry 16, 242 (2026). https://doi.org/10.1038/s41398-026-03952-4
Schlüsselwörter: perineuronale Netze, Kleinhirn, soziales Verhalten, Autismus-Modelle, neuronale Schaltkreise