Clear Sky Science · de
Definition subzellulärer synovialer Reaktionen beim Beginn der Kiefergelenk‑Arthrose (TMJ) mittels Modelle für mechanische Belastung und Diskusfehlstellung
Warum Abnutzung des Kiefergelenks wichtig ist
Das Kiefergelenk, oder temporomandibuläre Gelenk (TMJ), ermöglicht Kauen, Sprechen und Gähnen. Wenn es zu degenerieren beginnt — eine Erkrankung, die als TMJ‑Arthrose bezeichnet wird — leiden Betroffene oft unter chronischen Schmerzen, Ess‑einschränkungen und verminderter Lebensqualität. Im Vergleich zu Knie‑ oder Hüftgelenken wurde dieses kleine, aber komplexe Gelenk jedoch deutlich seltener untersucht. Diese Studie nutzt moderne genetische Kartierungswerkzeuge in Mausmodellen, um in bisher unerreichter Detailtiefe aufzuzeigen, was sich in der weichen Auskleidung des Gelenks abspielt, wenn TMJ‑Arthrose beginnt.
Zwei Wege, ein Kiefergelenk zu überlasten
Um gängige Probleme bei Patienten nachzubilden, erzeugten die Forschenden zwei Arten von TMJ‑Schädigung in Mäusen. In einem Modell veränderten sie die Verzahnung der Zähne, sodass der Kiefer schief schloss und das Gelenk wiederholt überlastet wurde — dies steht für mechanische Belastung durch eine fehlerhafte Okklusion. Im anderen Modell zogen sie die dämpfende Diskusstruktur im Gelenk nach vorne und befestigten sie an einer falschen Stelle, was eine verschobene Scheibe nachahmt, die oft mit TMJ‑Schmerzen verbunden ist. Beide Modelle wurden über drei Wochen mit gesunden Kontrollen verglichen, während Knochenstruktur und Gewebeveränderungen mithilfe von 3D‑Röntgenaufnahmen und Mikroskopie gemessen wurden. 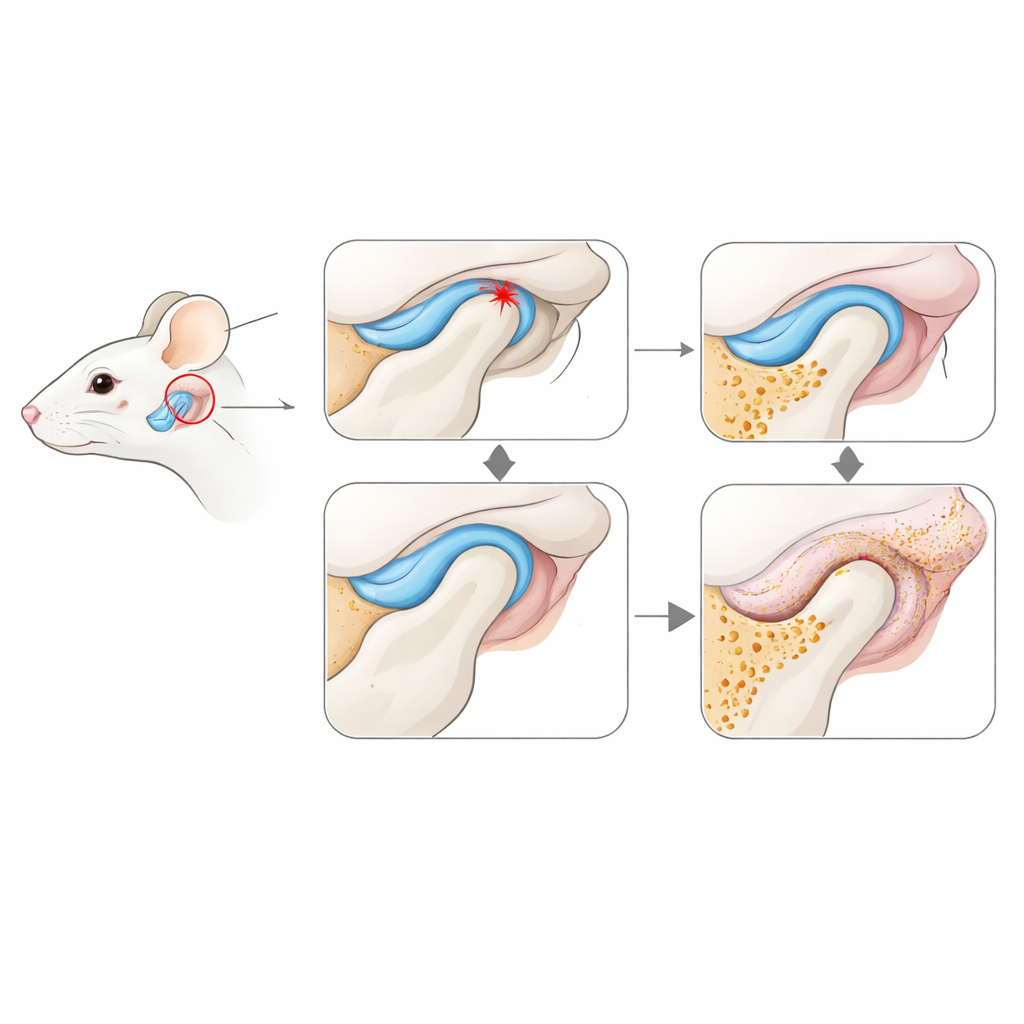
Frühe Schäden in Knochen, Knorpel und Gelenkauskleidung
Sowohl überlastete als auch diskusverschobene Gelenke zeigten rasch typische Zeichen früher Arthrose. Der knöcherne Kopf des Kiefers verlor Mineraldichte und entwickelte Grübchen, überschüssige Knochenanbauten sowie vermehrt aktive Osteoklasten, was auf eine beschleunigte Umgestaltung des inneren Gelenkgerüsts hinweist. Der Knorpel, der normalerweise eine glatte Gleitfläche bildet, begann zu dünnern, zu rissigen Veränderungen und verlor schützenswerte Moleküle, besonders im Diskusverlagerungs‑Modell. Gleichzeitig verdickte sich das Synovium — die dünne, weiche Auskleidung, die das Gelenk ernährt — füllte sich mit mehr Zellen und wurde in manchen Bereichen fettig oder fibrös. Diese strukturellen Veränderungen deuten darauf hin, dass die Gelenkauskleidung kein passiver Beobachter ist, sondern eine Schlüsselrolle beim Einleiten der Gelenkdegeneration spielt.
Die molekularen Signale des Gelenks Zelle für Zelle lesen
Um über die Anatomie hinauszugehen und zu sehen, was einzelne Zellen tun, untersuchte das Team, welche Gene in Tausenden von Zellen aktiviert waren, mithilfe von Bulk‑RNA‑Sequenzierung, Einzelzell‑RNA‑Sequenzierung und hochauflösender spatialer Transkriptomik. Diese Methoden erlaubten ihnen, genau zu bestimmen, wann und wo verschiedene Zelltypen ihr Verhalten änderten. Am knöchernen Ende des Gelenks wurden Gene, die normalerweise den Knorpel erhalten, herunterreguliert, während Gene, die mit Gewebeabbau und osteoklastischer Aktivität verbunden sind, besonders im Diskusverlagerungsmodell erhöht waren. Im Synovium steigerten Zellen die Produktion entzündlicher Botenstoffe, gewebsverdauender Enzyme und Moleküle, die mit Narbenbildung und Fibrose assoziiert sind. Ein besonders wichtiger Hotspot war der hintere (posterior) Teil der Diskusauskleidung, wo Entzündung, Fettablagerung und fibrotische Verdickung frühzeitig zusammenkamen.
Zelluläre Kommunikation und eine neue Karte des Kiefergelenks
Indem sie Genaktivität auf Einzelzellebene analysierten und diese Zellen zurück an ihre exakten Positionen im Gewebe kartierten, identifizierten die Autoren unterschiedliche Nachbarschaften von Fibroblasten (Stütz‑/Bindegewebszellen), Immunzellen und vaskulären Zellen innerhalb des Synoviums. Diese Zelltypen scheinen über Signalwege miteinander zu kommunizieren, die auf mechanische Belastung und Entzündung reagieren. Beispielsweise waren Signale der Notch‑Pathway — bekannt für die Regulation von Blutgefäßen und Gewebeumbau — besonders aktiv in endothelialen (gefäßauskleidenden) Zellen in geschädigten Gelenken, wahrscheinlich beeinflusst durch benachbarte Fibroblasten. Dieselben Regionen zeigten außerdem hohe Konzentrationen von Enzymen, die Knorpel abbauen, und Markern der Fibrose, was die Idee stützt, dass gestresste synoviale Zellen Knorpelverlust und Schmerz vorantreiben können. 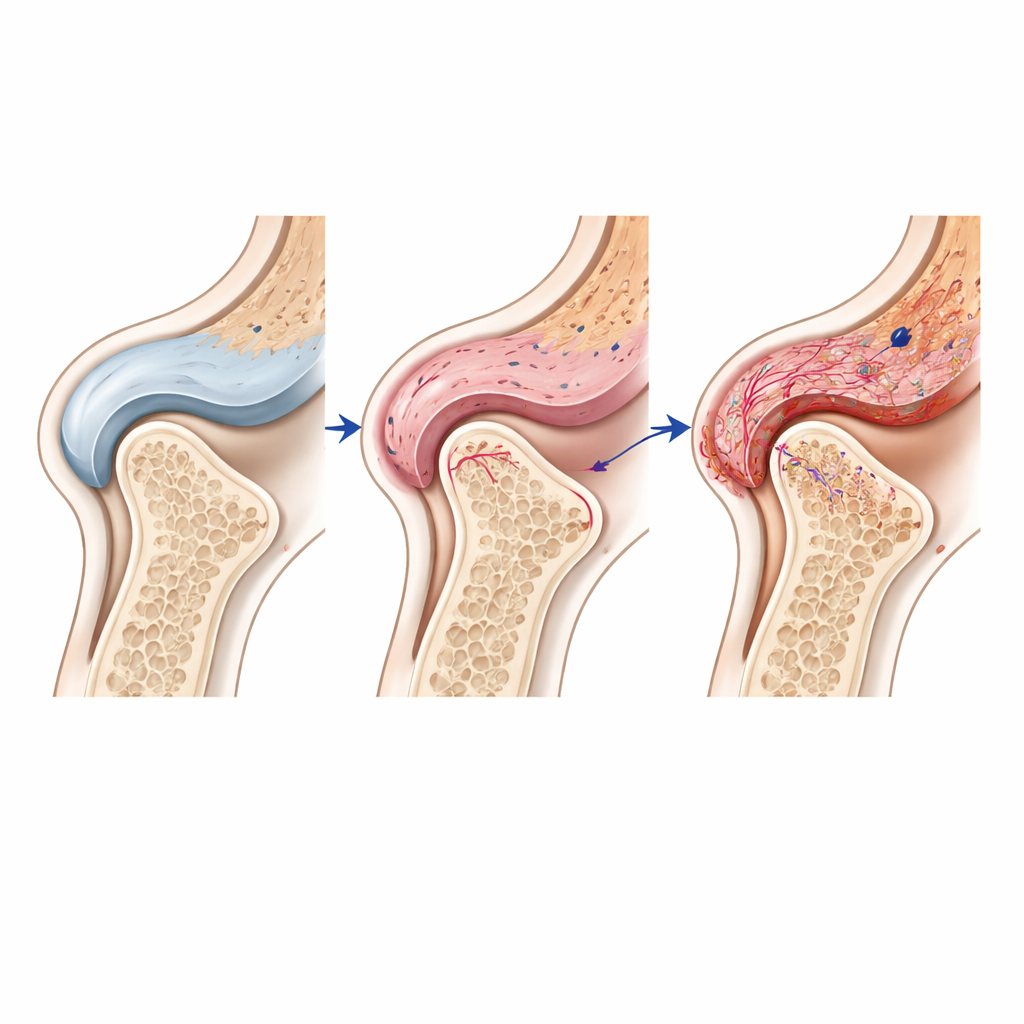
Wie diese Arbeit künftige Behandlungen prägen könnte
Anstatt ein spezifisches Medikament zu testen, liefert diese Studie einen detaillierten Atlas darüber, wie die weiche Auskleidung und der Knorpel des TMJ in den frühesten Stadien auf schädliche Kräfte reagieren. Sie zeigt, dass frühe TMJ‑Arthrose von koordinierten Veränderungen in Knochen, Knorpel und insbesondere synovialen Zellen gekennzeichnet ist, die entzündlich und fibrös werden und schädliche Signale ins Gelenk senden. Indem diese Veränderungen präzisen Zelltypen und Orten zugeordnet werden, hebt die Arbeit neue potenzielle Therapieziele hervor — etwa Signalwege der Notch‑Signalgebung, Chemokin‑Signale und matrixabbauende Enzyme — die blockiert werden könnten, bevor Gelenkschäden irreversibel werden. Kurz: Die Studie liefert einen kraftvollen Plan, um die Abfolge von Ereignissen zu verstehen und schließlich zu unterbrechen, die alltägliche Kieferbewegung in chronische TMJ‑Schmerzen verwandelt.
Zitation: Shibusaka, K., Negishi, S., Terashima, A. et al. Defining subcellular synovial responses in TMJ osteoarthritis onset via mechanical stress and articular disk derangement models. Int J Oral Sci 18, 28 (2026). https://doi.org/10.1038/s41368-025-00411-6
Schlüsselwörter: temporomandibulargelenk, Arthrose, Synovium, mechanische Belastung, Einzelzell‑Transkriptomik