Clear Sky Science · ar
تحليل مسارات الإشارات المخصص لأورام الجهاز الهضمي لتصنيف المرضى وتقييم أهداف الأدوية باستخدام خزعات أساسية مشتقة من المريض
لماذا يهم هذا البحث المرضى
يحاول أطباء الأورام بشكل متزايد مطابقة العلاجات مع البيولوجيا الفريدة لورم كل مريض. بالنسبة لأورام الجهاز الهضمي—مثل البنكرياس والقولون والكبد والقنوات الصفراوية—تزداد الحاجة لذلك، إذ إنها شائعة وغالبًا ما تُشخّص متأخرًا ويصعب علاجها. يستكشف هذا البحث طريقة مختبرية جديدة يمكنها قراءة نشاط عدد كبير من البروتينات المرتبطة بالسرطان من عينات خزعة صغيرة جدًا، بهدف مساعدة الأطباء على اختيار علاجات أكثر دقة للمرضى الفرديين.
من قوائم الحمض النووي إلى إشارات حية
في الوقت الحاضر، يعتمد معظم الرعاية «المخصصة» للسرطان على قراءة تغيّرات الحمض النووي في الورم. ورغم قوة هذه المقاربة، فإن الحمض النووي وحده لا يظهر أي الإشارات داخل الخلية تعمل فعليًا وتدفع النمو. تنتقل تلك الإشارات بواسطة البروتينات، والعديد منها يمكن استهدافه مباشرة بالأدوية. استخدم الباحثون تقنية عالية الإنتاجية تسمى DigiWest، وهي تطوير عصري لتقنية Western blot الكلاسيكية، لقياس نحو 130–200 بروتين وأشكالها المفعّلة في آن واحد. والأهم أن هذه الطريقة تحتاج إلى كمية قليلة مماثلة لما تحتويه خزعة إبرة واحدة، ما يجعلها مناسبة للاستخدام في سياق الرعاية السريرية الواقعية.
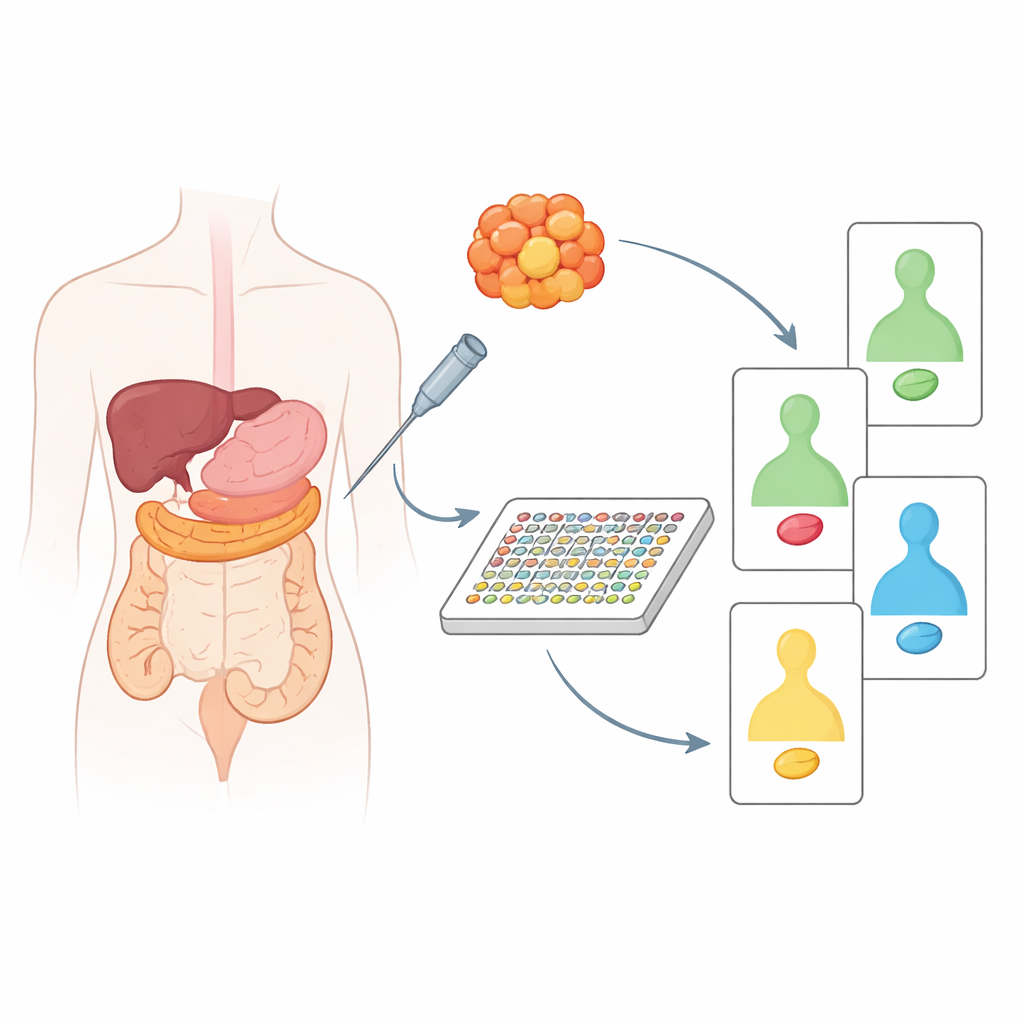
مقارنة نسيج الورم بجواره السليم
حلّل الفريق أولًا أنسجة مخزنة من 20 مريضًا بسرطان البنكرياس أو القولون، دائمًا مصحوبة بنسيج غير سرطاني مجاور من نفس الشخص. من خلال مقارنة الأورام بنظيراتها السليمة داخل ذات المريض، تمكنوا من رؤية أي البروتينات تغيرت بالفعل بفعل السرطان بدلاً من أن تعكس فروقًا طبيعية بين الأعضاء. كشفت هذه المقارنة فروقًا واضحة في سلوك حراس ودافعي السرطان المعروفين، مثل p53 وRas وPTEN وآخرين. فعلى سبيل المثال، أظهرت أورام البنكرياس ميلاً لوجود إشارات محفزة للنمو مع فقدان بروتينات وقائية، بينما كان لأورام القولون نمط مميز خاص بها من المسارات المضطربة. عندما جمع الباحثون العينات عن طريق العنقود بناءً على تغيّرات البروتين هذه، استطاعوا تقسيم سرطانات البنكرياس إلى مجموعتين بيولوجيتين مختلفتين واكتشاف فروق ذات معنى بين سرطانات القولون مرتبطة بعمر المريض وموقع الورم في الأمعاء.
"بصمات شريطية" فردية لنشاط الإشارات في الورم
تجاوزًا لمتوسطات المجموعات، بنى العلماء ملف بروتيني مفصّل لكل ورم. أبرزت هذه الملفات أي الطرق الإشارية—مثل تلك المتضمنة mTOR وMAPK/Erk وWnt أو عوامل متعلقة بالمناعة—كانت نشطة بشكل خاص أو معطلة. العديد من البروتينات المقاسة هي أهداف مباشرة لأدوية موجودة، أو تقع مباشرة بعد أهداف كهذه، مما أتاح للفريق استنتاج أي الأدوية قد تتداخل مع المحركات الرئيسية لنمو الورم. في ثلاثة أرباع الحالات الاستعادية، تمكنوا من الإشارة إلى واحد أو أكثر من المسارات التي من المحتمل أنها غذّت تقدم الورم. كما حدّدوا أورامًا غنية بعلامات الخلايا المناعية، مما يشير إلى سرطانات "ساخنة" قد تستجيب للعلاج المناعي، وحالات غير عادية ذات تواقيع فريدة لافتة.
تطبيق الطريقة على مرضى حقيقيين
لاختبار فائدتها سريريًا، طبّق الباحثون بعد ذلك DigiWest على خزعات إبرة طازجة من 14 مريضًا يعانون أنواعًا مختلفة من سرطانات الجهاز الهضمي كانت قضاياهم قيد مراجعة من قبل لوحة أورام جزيئية. كان لدى هؤلاء المرضى تاريخ مرضي معقد وفي كثير من الأحيان علاجات سابقة. وبما أن نسيجًا سليمًا مطابقًا لم يكن متاحًا، قورن مستوى البروتين في كل ورم بمستوى الوسيط عبر المجموعة لتحديد ما يُعد مرتفعًا أو منخفضًا بشكل غير طبيعي. حتى مع هذا الإعداد الأكثر تشددًا، أظهرت 12 من أصل 14 ورمًا أنماطًا واضحة ذات صلة بالعلاج لنشاط المسارات. في مثالين مفصّلين، أكدت بيانات البروتين تضخيمًا على مستوى الحمض النووي لجين FGFR2 في سرطان القولون وفقدان قيد على mTOR في سرطان الكبد، مما دعم بشدة نظر مجلس المراجعة في استخدام أدوية تحظر FGFR أو تعيق mTOR. عمومًا، اتفقت نتائج DigiWest مع محركات جينية رئيسية واقترحت أهدافًا دوائية في معظم الحالات القابلة للتقييم.
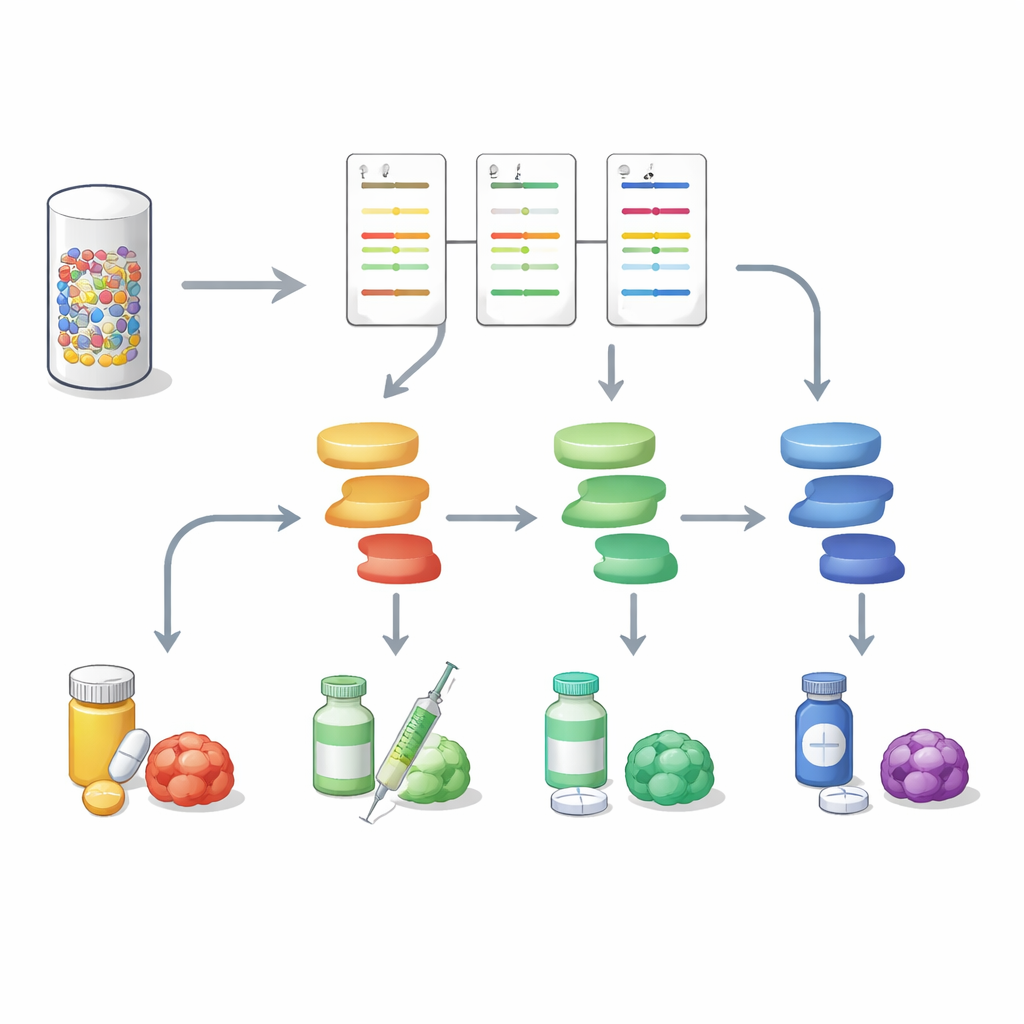
نحو صور أورام أكثر اكتمالًا
تُظهر هذه الدراسة أن تحليل إشارات البروتين بالتوازي مع تسلسل الحمض النووي يمكن أن يمنح صورة أكثر ثراءً وقابلة للتطبيق عمليًا لأورام الجهاز الهضمي. من خلال تحويل خزعة صغيرة إلى خريطة نشاط متعددة المسارات، يساعد DigiWest على التمييز أي مفاتيح جزيئية هي فعلاً في وضع التشغيل في سرطان معين وأي الأدوية قد تضربها بشكل أفضل، وربما يشير أيضًا إلى مسارات مقاومة ناشئة. وبينما لا تزال هناك حاجة لدراسات أكبر، فإن المنهجية تقدم وسيلة عملية لإدخال بروفيليغ عالي المحتوى للبروتينات في طب الأورام الدقيق اليومي والاقتراب أكثر من خطط علاج مصممة لورم المريض الحي، وليس فقط لمخططه الجيني.
الاستشهاد: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
الكلمات المفتاحية: الطب الدقيق في الأورام, سرطان الجهاز الهضمي, البروتيوميات, تشكيل ملف الخزعات, العلاج الموجّه