Clear Sky Science · ar
الأستازانثين يثبط سرطان الكبد الخلوي عن طريق استهداف مسار Wnt/Β-catenin: دراسة تجريبية على سرطان كبد محرض كيميائياً في الجرذان
لماذا يهم صباغ أحمر من مأكولات البحر
يعد سرطان الكبد الأساسي واحداً من أخطر السرطانات عالمياً، والأدوية الحالية قد تكون قاسية على الجسم وتفقد فعاليتها مع تطور مقاومة الأورام. تستقصي هذه الدراسة ما إذا كان الأستازانثين — الصباغ الأحمر الذي يعطي السلمون والروبيان لونهما — يمكن أن يعزز فعالية العلاج الكيميائي القياسي ويحمي الكبد في الوقت نفسه. باستخدام نموذج جرذان لسرطان الكبد، يوضح الباحثون كيف يتعاون هذا المركب الطبيعي مع دواء مضاد للسرطان شائع لتقليص الأورام، وتخفيف تلف الكبد، وتعطيل إشارات داخل الخلايا تقود السرطان.
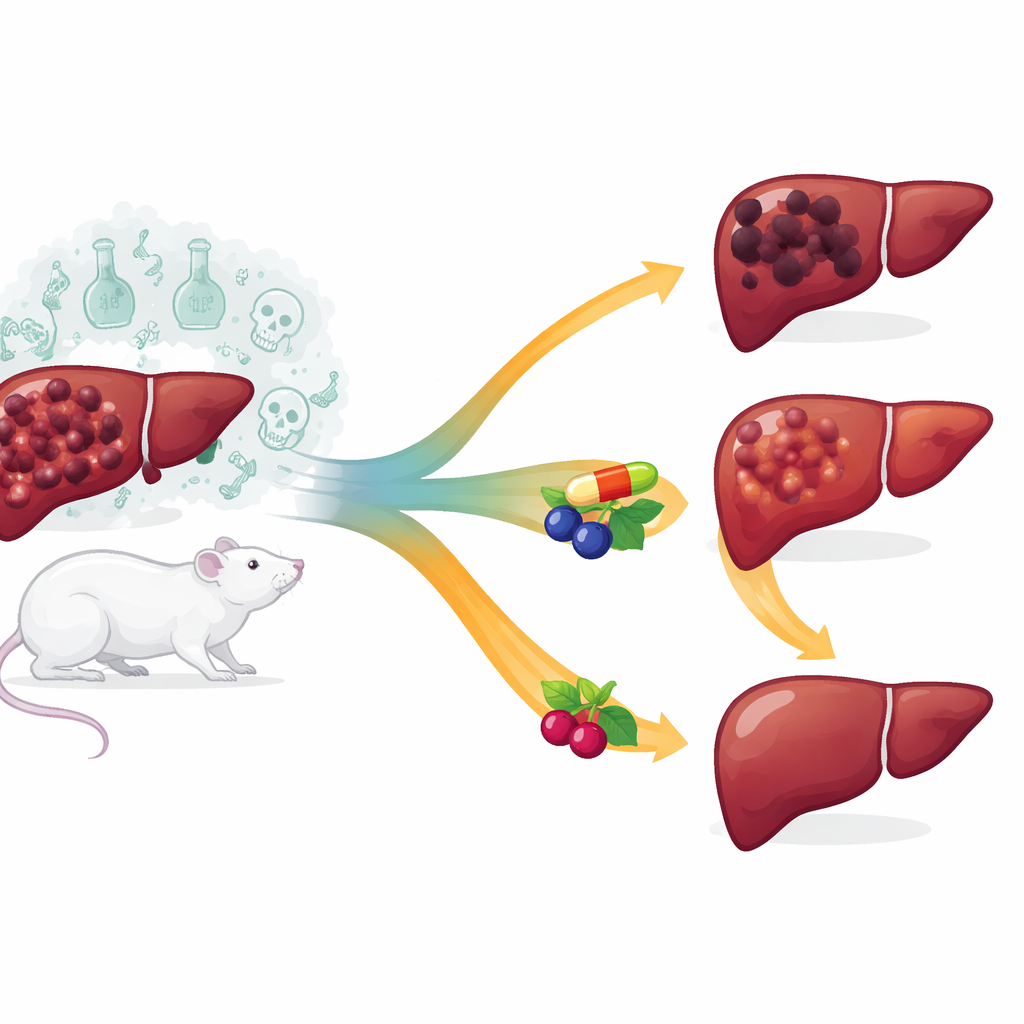
اختبار مساعد طبيعي للعلاج الكيميائي
لمحاكاة سرطان الكبد البشري، عرّض الفريق أولاً الجرذان لمادتين كيميائيتين تضرّان الكبد وتحفزان تكوّن الأورام. ثم قسّموا الحيوانات إلى مجموعات: ضوابط سليمة، سرطان دون علاج، سرطان عولج بالأستازانثين وحده، سرطان عولج بعقار الدوكسوروبيسين وحده، وسرطان عولج بالمزيج معاً. على مدى أربعة أسابيع، قاسوا مؤشرات دموية لضرر الكبد وعبء الورم، وفحصوا نسيج الكبد ميكروسكوبيًا، وحللوا جزيئات تتحكم في نمو الخلايا، ومقاومة الدواء، وتوازن الخلية بين التلف والإصلاح.
تنظيف كبد مجهد ومتضرر
في الجرذان السرطانية غير المعالجة، أظهر الكبد إصابة شديدة: ارتفعت إنزيمات تسرّب إلى الدم — AST وALT — بعدة أضعاف، وتضاعف ألفا-فيتو بروتين، وهو بروتين غالبًا ما يرتفع في سرطان الكبد. كان نسيج الكبد مليئاً بعقيدات سرطانية وببنيوية مشوهة. حسن الأستازانثين وحده هذه المقاييس، لكن أقوى تأثير سجّل مع الجمع مع الدوكسوروبيسين. في مجموعة المزيج، انخفضت إنزيمات الكبد وألفا-فيتو بروتين بشكل حاد مقارنةً بالحيوانات غير المعالجة، واختفت العقيدات السرطانية لتحلّ محلها أنسجة كبدية بدت أقرب إلى الطبيعية مع احتقان وريدي طفيف فقط.
إسكات مفتاح نمو رئيسي داخل الخلايا
غالباً ما تختطف الخلايا السرطانية مسار تواصل داخلي يعرف بمسار Wnt/β-catenin، الذي يعمل كمفتاح نمو. عندما يكون في وضع التشغيل، يثبّت بروتيناً يسمى β-catenin الذي ينتقل إلى نواة الخلية ويشغل جينات تدفع الانقسام الخلوي والبقاء ومقاومة الأدویة المتعددة. في الجرذان المصابة بسرطان الكبد، كان هذا المفتاح عالقاً بوضوح في وضع "تشغيل": زادت مستقبلات سطح الخلية التي تستقبل إشارات Wnt بشكل كبير، ارتفعت مستويات β-catenin، وكُبِح إنزيم الحماية GSK3β — الذي يساعد عادة على تفكيك β-catenin. ونتيجة لذلك، نُشّطت جينات مرتبطة بالنمو السريع (cyclin D1، c-Myc) ومقاومة الدواء (MDR1) بشدة.
الأستازانثين يعيد التوازن
عالج الأستازانثين، وخاصة عند دمجه مع الدوكسوروبيسين، هذا النمط عند عدة نقاط حاسمة. انخفضت مستويات مستقبلات Wnt، وتراجعت مستويات β-catenin بشكل ملحوظ، وتعافى GSK3β نحو الوضع الطبيعي، ما يشير إلى أن إشارة النمو كانت تُغلق سواء على سطح الخلية أو داخلها. وفي المسارات اللاحقة، انخفض تعبير cyclin D1 وc-Myc، مما كبح الدافع نحو الانقسام غير المسيطر عليه. ومن الجدير بالذكر أن الدوكسوروبيسين وحده رفع جين MDR1 — إحدى الطرق التي تطرد بها الخلايا السرطانية الدواء وتصير مقاومة — لكن إضافة الأستازانثين خففت هذا الاستجابة وعادت مستويات MDR1 أقرب إلى الطبيعي. بعبارة أخرى، بدا أن الأستازانثين يحافظ على مزيد من الدواء داخل الخلايا السرطانية بينما يخفض دوائر بقائها.
استعادة نظام دفاع الكبد
تُظهر الدراسة أيضاً أن الكبد السرطاني كان تحت إجهاد تأكسدي كبير: استُنفدت مخازن الغلوتاثيون الواقية، وزاد شكله المؤكسد، وتراكمت نواتج ضارة لتفكك الدهون مثل مالونالديهايد. أعاد الأستازانثين وحده مستويات الغلوتاثيون، وحسّن نسبة الغلوتاثيون المختزل إلى المؤكسد، وأعاد مالونالديهايد إلى الوضع الطبيعي. وعند اقترانه بالدوكسوروبيسين، كانت هذه الفوائد أكثر وضوحاً، مما يشير إلى أن الأستازانثين لا يحمي خلايا الكبد من الإصابة الكيميائية فحسب، بل يهدئ أيضاً بشكل غير مباشر إشارات النمو التي تعتمد على الجزيئات المؤكسدة للبقاء نشطة.
ماذا قد يعني هذا للعلاجات المستقبلية
للقارئ العادي، الخلاصة أن صباغاً أحمرَ طبيعياً يمكن أن يفعل أكثر من كونه مضاد أكسدة: في نموذج الجرذان هذا، ساعد دواء علاج سرطاني قياسي على العمل بشكل أفضل ضد سرطان الكبد مع تقليل الضرر للكبد نفسه. من خلال قطع مسار نمو مركزي ومنع قدرة السرطان على طرد الدواء، عمل الأستازانثين كمعزّز للحساسية الكيميائية، مما جعل خلايا الورم أكثر عرضة. وبينما لا تزال هذه النتائج بحاجة إلى تأكيد في دراسات بشرية، فإنها تشير إلى مستقبل يُضمَّن فيه مركبات طبيعية مختارة بعناية مع الأدوية القائمة لجعل علاجات السرطان أكثر فعالية ولطفاً على الأعضاء السليمة.
الاستشهاد: Kortam, M.A., Ismail, M.S., Kamel, M.A. et al. Astaxanthin suppresses hepatocellular carcinoma via targeting Wnt/Β-catenin pathway: Experimental study on chemically induced HCC in rats. Sci Rep 16, 12928 (2026). https://doi.org/10.1038/s41598-026-45680-1
الكلمات المفتاحية: سرطان الكبد, الأستازانثين, مقاومة العلاج الكيميائي, الإجهاد التأكسدي, Wnt بيتا-كاتينين